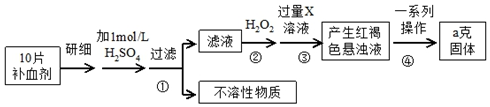
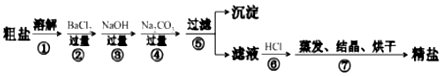
12.下列说法中正确的是( )
| A. | 过量的铜与浓硝酸反应有一氧化氮生成 | |
| B. | Al、Fe、Cu的单质放置在空气中均只生成氧化物 | |
| C. | SiO2与酸、碱均不反应 | |
| D. | 向一定浓度的Na2SiO3溶液中通入适量CO2气体,出现白色沉淀,则H2SiO3的酸性比H2CO3的酸性强 |
10.乙醇是重要的化工产品和液体燃料,可以利用下列反应制取乙醇:
2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g)①298K时,K1=2.95×1011
2CO(g)+4H2(g) CH3CH2OH(g)+H2O(g)②298K时,K2=1.71×1022
(1)条件相同时,反应①与反应②相比,转化程度更大的是②.
(2)在一定压强下,测得反应①的实验数据如表:
根据表中数据分析:…
①温度升高,K值减小(填“增大”“减小”或“不变”).
②提高氢碳比[n(H2)/n(CO2)],对生成乙醇有利(填“有利”或“不利”).
2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g)①298K时,K1=2.95×1011
2CO(g)+4H2(g) CH3CH2OH(g)+H2O(g)②298K时,K2=1.71×1022
(1)条件相同时,反应①与反应②相比,转化程度更大的是②.
(2)在一定压强下,测得反应①的实验数据如表:
| 温度(K) CO2转化率(%) n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
①温度升高,K值减小(填“增大”“减小”或“不变”).
②提高氢碳比[n(H2)/n(CO2)],对生成乙醇有利(填“有利”或“不利”).
9.煤的气化是高效、清洁的利用煤炭的重要途径之一.
(1)焦炭与水蒸气反应是将固体煤变为气体燃料的方法.已知:
①C(s)+O2 (g)=CO2 (g)△H=-393.5kJ•mol-1
②CO(g)+$\frac{1}{2}$O2 (g)=CO2 (g)△H=-283.0kJ•mol-1
③H2(g)+$\frac{1}{2}$O2 (g)=H2O (g)△H=-241.8kJ•mol-1
则碳与水蒸气反应生成一氧化碳和氢气的热化学方程式是C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ/mol,该反应的化学平衡常数K随温度的升高将增大(填“增大”、“减小”或“不变”).
(2)CO可以与H2O(g)进一步发生反应CO(g)+H2O(g)?CO2(g)+H2(g)△H<0.在甲、乙两个恒容密闭容器中,起始时按照表数据进行投料,在800℃时达到平衡状态,K=1.0.
起始时,甲容器中反应向逆反应(填“正反应”或“逆反应”)方向进行;平衡时,乙容器中CO的转化率为50%.
(3)以CO为燃料制作燃料电池,电池的正极通入O2和CO2,负极通入CO,电解质是熔融碳酸钠,写出工作时正极的电极反应式:O2+4e-+2CO2=2CO32-,若使用该电池电解熔融Al2O3制取10.8g Al,则理论上需要氧气的体积为(标准状况下)6.72L.
(4)将(2)中生成的混合气用过量的NaOH溶液吸收,得到的溶液中有一种溶质可以水解,请写出其水解的离子方程式:CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-.
(1)焦炭与水蒸气反应是将固体煤变为气体燃料的方法.已知:
①C(s)+O2 (g)=CO2 (g)△H=-393.5kJ•mol-1
②CO(g)+$\frac{1}{2}$O2 (g)=CO2 (g)△H=-283.0kJ•mol-1
③H2(g)+$\frac{1}{2}$O2 (g)=H2O (g)△H=-241.8kJ•mol-1
则碳与水蒸气反应生成一氧化碳和氢气的热化学方程式是C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ/mol,该反应的化学平衡常数K随温度的升高将增大(填“增大”、“减小”或“不变”).
(2)CO可以与H2O(g)进一步发生反应CO(g)+H2O(g)?CO2(g)+H2(g)△H<0.在甲、乙两个恒容密闭容器中,起始时按照表数据进行投料,在800℃时达到平衡状态,K=1.0.
| H2O | CO | CO2 | H2 | |
| 甲 n/mol | 0.10 | 0.30 | 0.10 | 0.50 |
| 乙 n/mol | 0.20 | 0.20 | 0 | 0 |
(3)以CO为燃料制作燃料电池,电池的正极通入O2和CO2,负极通入CO,电解质是熔融碳酸钠,写出工作时正极的电极反应式:O2+4e-+2CO2=2CO32-,若使用该电池电解熔融Al2O3制取10.8g Al,则理论上需要氧气的体积为(标准状况下)6.72L.
(4)将(2)中生成的混合气用过量的NaOH溶液吸收,得到的溶液中有一种溶质可以水解,请写出其水解的离子方程式:CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-.
8.一定条件下,可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压代替平衡浓度计算,分压=总压×物质的量分数.在恒温恒压条件下,总压不变,用平衡分压计算平衡常数更方便.下列说法不正确的是( )
| A. | 对于C2H4 (g)+H2O(g)?C2H5OH(g),在一定条件下达到平衡状态时,体系的总压强为P,其中C2H4(g)、H2O(g)、C2H5OH(g)均为2 mol,则用分压表示的平衡常数Kp=$\frac{3}{P}$ | |
| B. | 恒温恒压下,在一容积可变的容器中,N2(g)+3H2(g)?2NH3(g)达到平衡状态时,N2、H2、NH3各1mol,若此时再充入3mol N2,则平衡正向移动 | |
| C. | 恒温恒压下,在一容积可变的容器中,反应2A(g)+B(g)?2C(g)达到平衡时,A、B和 C的物质的量分别为4mol、2mol和4mol,若此时A、B和C均减少1 mol,平衡逆向移动 | |
| D. | 对于一定条件下的某一可逆反应,用平衡浓度表示的平衡常数和用平衡分压表示的平衡常数,其数值不同,但意义相同,都只与温度有关 |
7.下列实验中,对应的现象以及实验目的都正确的是( )
| 选项 | 目的 | 实验 | 现象 |
| A | 检验CO2气体中混有SO2 | 将气体通入盛有足量的澄清石灰水中的洗气瓶中 | 石灰水变浑浊 |
| B | 检验黑色固体Fe3O4中含有+3价铁元素 | 将少量黑色固体加入盛有KSCN溶液的烧杯中 | 固体溶解,溶液呈血红色 |
| C | 比较氯和碳的非金属性强弱 | 将碳酸钠溶液中滴入稀盐酸 | 有气泡产生 |
| D | 验证氧化性:Fe3+>Cu2+ | 将一定量铜粉加到盛有一定体积的1.0mol•L-1Fe2(SO4)3溶液的试管中 | 铜粉溶解,溶液变蓝色 |
| A. | A | B. | B | C. | C | D. | D |
5.(1)如图 I表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为5,量筒中液体的体积是3.6mL.
(2)如图 II表示50mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)D.
A.是a mL B.是(50-a)mLC.一定大于a mL D.一定大于(50-a)mL
(3)某研究性学习小组为了探究醋酸的电离情况,进行了如实验.配制并标定醋酸溶液的浓度,取冰醋酸配制250mL 0.2mol•L-1的醋酸溶液,用0.2mol•L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定.回答下列问题:
①配制250mL 0.2mol•L-1醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和250 mL容量瓶.
②为标定某醋酸溶液的准确浓度,用0.200 0mol•L-1的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如表:
则该醋酸溶液的准确浓度为0.2000 mol/L.(保留小数点后四位)
③关于该滴定实验,从下列选项中选出最恰当的一项D(选填字母).
探究浓度对醋酸电离程度的影响
用pH计测定25℃时不同浓度的醋酸的pH,结果如表:
回答下列问题:
④根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是:0.0100 mol•L-1醋酸的pH大于2或醋酸稀释10倍时,pH的变化值小于1.
⑤从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度将增大.(填“增大”“减小”或“不变”)
探究温度对醋酸电离程度的影响
⑥请你设计一个实验完成该探究,请简述你的实验方案:用pH计(或精密pH试纸)测定相同浓度的醋酸在几种不同温度时的pH.
0 160217 160225 160231 160235 160241 160243 160247 160253 160255 160261 160267 160271 160273 160277 160283 160285 160291 160295 160297 160301 160303 160307 160309 160311 160312 160313 160315 160316 160317 160319 160321 160325 160327 160331 160333 160337 160343 160345 160351 160355 160357 160361 160367 160373 160375 160381 160385 160387 160393 160397 160403 160411 203614

(2)如图 II表示50mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)D.
A.是a mL B.是(50-a)mLC.一定大于a mL D.一定大于(50-a)mL
(3)某研究性学习小组为了探究醋酸的电离情况,进行了如实验.配制并标定醋酸溶液的浓度,取冰醋酸配制250mL 0.2mol•L-1的醋酸溶液,用0.2mol•L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定.回答下列问题:
①配制250mL 0.2mol•L-1醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和250 mL容量瓶.
②为标定某醋酸溶液的准确浓度,用0.200 0mol•L-1的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如表:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
③关于该滴定实验,从下列选项中选出最恰当的一项D(选填字母).
| 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 | |
| A | 碱 | 酸 | 石蕊 | (乙) |
| B | 酸 | 碱 | 甲基橙 | (甲) |
| C | 碱 | 酸 | 酚酞 | (甲) |
| D | 酸 | 碱 | 酚酞 | (乙) |
用pH计测定25℃时不同浓度的醋酸的pH,结果如表:
| 醋酸浓度(mol•L-1) | 0.001 0 | 0.010 0 | 0.020 0 | 0.100 0 | 0.200 0 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
④根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是:0.0100 mol•L-1醋酸的pH大于2或醋酸稀释10倍时,pH的变化值小于1.
⑤从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度将增大.(填“增大”“减小”或“不变”)
探究温度对醋酸电离程度的影响
⑥请你设计一个实验完成该探究,请简述你的实验方案:用pH计(或精密pH试纸)测定相同浓度的醋酸在几种不同温度时的pH.