1. 2013年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.
2013年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.
(1)CO2是大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径.目前,由CO2来合成二甲醚已取得了较大的进展,其化学反应是:2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g)△H>0.
①写出该反应的平衡常数表达式K=$\frac{[CH{\;}_{3}OCH{\;}_{3}]•[H{\;}_{2}O]{\;}^{3}}{[CO{\;}_{2}]{\;}^{2}•[H{\;}_{2}]{\;}^{6}}$.
②判断该反应在一定条件下,体积恒定的密闭容器中是否达到化学平衡状态的依据是BD.
A.容器中密度不变
B.单位时间内消耗2molCO2,同时消耗1mol二甲醚
C.v(CO2):v(H2)=1:3
D.容器内压强保持不变
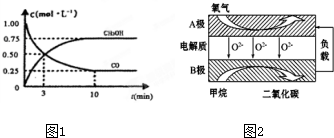
(2)汽车尾气净化的主要原理为:2NO(g)+2CO (g) $\stackrel{催化剂}{?}$2CO2 (g)+N2 (g).在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示.据此判断:
①该反应的△H<0(选填“>”、“<”).
②当固体催化剂的质量一定时,增大其表面积可提高化学反应速率.若催化剂的表面积S1>S2,在图中画出c(CO2)在T2、S2条件下达到平衡过程中的变化曲线.
(3)已知:CO(g)+2H2(g)?CH3OH(g)△H=-a kJ•mol-1.
①经测定不同温度下该反应的平衡常数如下:
若某时刻、250℃测得该反应的反应物与生成物的浓度为c(CO)=0.4mol•L-1、c(H2)=0.4mol•L-1、c(CH3OH)=0.8mol•L-1,则此时v正<v逆(填“>”、“<”或“=”).
②某温度下,在体积固定的2L的密闭容器中将1mol CO和2mol H2混合,测得不同时刻的反应前后压强关系如下:
则前15分钟,用氢气表示的平均化学反应速率为0.02mol•(L•min)-1,达到平衡时CO的转化率为45%.
 2013年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.
2013年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.(1)CO2是大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径.目前,由CO2来合成二甲醚已取得了较大的进展,其化学反应是:2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g)△H>0.
①写出该反应的平衡常数表达式K=$\frac{[CH{\;}_{3}OCH{\;}_{3}]•[H{\;}_{2}O]{\;}^{3}}{[CO{\;}_{2}]{\;}^{2}•[H{\;}_{2}]{\;}^{6}}$.
②判断该反应在一定条件下,体积恒定的密闭容器中是否达到化学平衡状态的依据是BD.
A.容器中密度不变
B.单位时间内消耗2molCO2,同时消耗1mol二甲醚
C.v(CO2):v(H2)=1:3
D.容器内压强保持不变
(2)汽车尾气净化的主要原理为:2NO(g)+2CO (g) $\stackrel{催化剂}{?}$2CO2 (g)+N2 (g).在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示.据此判断:
①该反应的△H<0(选填“>”、“<”).
②当固体催化剂的质量一定时,增大其表面积可提高化学反应速率.若催化剂的表面积S1>S2,在图中画出c(CO2)在T2、S2条件下达到平衡过程中的变化曲线.
(3)已知:CO(g)+2H2(g)?CH3OH(g)△H=-a kJ•mol-1.
①经测定不同温度下该反应的平衡常数如下:
| 温度(℃) | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
②某温度下,在体积固定的2L的密闭容器中将1mol CO和2mol H2混合,测得不同时刻的反应前后压强关系如下:
| 时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强比(P后/P前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
20.碳循环是地球上重要的物质循环,碳循环包含石油及石油制品的研发应用.石油工业上用两步法生产二甲醚,其工艺流程如下:
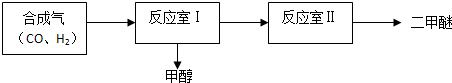
反应室Ⅰ:CO(g)+2H2(g)═CH3OH(g)
反应室Ⅱ:2CH3OH(g)═CH3OCH3(g)+H2O(g)
(1)欲提高反应室Ⅰ中CO的转化率,可以采取的方法有增大氢气浓度、不断分离出甲醇或者加压.
(2)反应室Ⅰ(恒容10L)中有关反应数据如下:
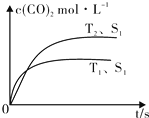
①图1表示反应室Ⅰ中不同温度下序号1(曲线m)和序号3(曲线n) 反应中CO转化率随时间变化的曲线,请在答题纸上的图4中补画出曲线n.
②判断:$\frac{{b}_{3}}{{b}_{1}}$>4(填“>”、“<”或“=”).
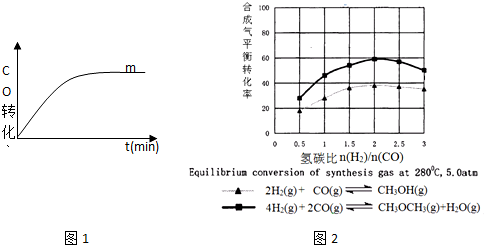
(3)图2表示甲醇或二甲醚体积分数随氢碳比$\frac{n({H}^{2})}{n(CO)}$的变化情况,从图中可以得到的结论是C.
A.提高氢碳比可以加快反应速率
B.提高氢碳比可以提高氢气的转化率
C.按方程式系数比投料时甲醇或二甲醚体积分数最大
D.对于同一反应氢碳比越大,生成物浓度越大
(4)已知某温度下下列热化学方程式:CO(g)+2H2(g)═CH3OH(g)△H1=-100.46kJ•mol-1
2CH3OH(g)═CH3OCH3(g)+H2O(g)△H2=-20.59kJ•mol-1,则2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g)△H3=-221.51kJ•mol-1.

反应室Ⅰ:CO(g)+2H2(g)═CH3OH(g)
反应室Ⅱ:2CH3OH(g)═CH3OCH3(g)+H2O(g)
(1)欲提高反应室Ⅰ中CO的转化率,可以采取的方法有增大氢气浓度、不断分离出甲醇或者加压.
(2)反应室Ⅰ(恒容10L)中有关反应数据如下:
| 序号 | 温度(°C) | 起始浓度(mol•L-1) | 平衡浓度(mol•L-1) | ||||
| CO | H2 | CH3OH | CO | H2 | CH3OH | ||
| ① | T | 1 | 3 | 0 | 0.2 | 1.4 | 0.8 |
| ② | T | 1.5 | 4.6 | 0.1 | b1 | b2 | b3 |
| ③ | T+30 | 1 | 3 | 0 | 0.25 | 1.5 | 0.75 |
②判断:$\frac{{b}_{3}}{{b}_{1}}$>4(填“>”、“<”或“=”).

(3)图2表示甲醇或二甲醚体积分数随氢碳比$\frac{n({H}^{2})}{n(CO)}$的变化情况,从图中可以得到的结论是C.
A.提高氢碳比可以加快反应速率
B.提高氢碳比可以提高氢气的转化率
C.按方程式系数比投料时甲醇或二甲醚体积分数最大
D.对于同一反应氢碳比越大,生成物浓度越大
(4)已知某温度下下列热化学方程式:CO(g)+2H2(g)═CH3OH(g)△H1=-100.46kJ•mol-1
2CH3OH(g)═CH3OCH3(g)+H2O(g)△H2=-20.59kJ•mol-1,则2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g)△H3=-221.51kJ•mol-1.
17.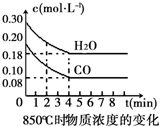 在一体积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g).CO和H2O(g)浓度变化如图
在一体积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g).CO和H2O(g)浓度变化如图
(1)0~4min的平均反应速率v(CO)=0.03mol•L-1•min-1.
(2)该条件下,此反应的平衡常数K=$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)c({H}_{2}O)}$(写表达式).
(3)该反应平衡时CO的转化率为60%.
(4)能判断该反应达到化学平衡状态的依据是BC.
A.容器中压强不变 B.混合气体中c(CO)不变
C.v(H2)正=v(H2O)逆 D.c(CO2)=c(CO)
若降低温度,该反应的K值将增大,该反应的化学反应速率将减小(填“增大”“减小”或“不变”).
(5)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表.
①c1数值大于0.08mol•L-1(填大于、小于或等于).
②反应在4min~5min间,平衡向逆方向移动,可能的原因是D,表中5min~6min之间数值发生变化,可能的原因是A.
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.
 在一体积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g).CO和H2O(g)浓度变化如图
在一体积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g).CO和H2O(g)浓度变化如图(1)0~4min的平均反应速率v(CO)=0.03mol•L-1•min-1.
(2)该条件下,此反应的平衡常数K=$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)c({H}_{2}O)}$(写表达式).
(3)该反应平衡时CO的转化率为60%.
(4)能判断该反应达到化学平衡状态的依据是BC.
A.容器中压强不变 B.混合气体中c(CO)不变
C.v(H2)正=v(H2O)逆 D.c(CO2)=c(CO)
若降低温度,该反应的K值将增大,该反应的化学反应速率将减小(填“增大”“减小”或“不变”).
(5)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表.
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0J062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
②反应在4min~5min间,平衡向逆方向移动,可能的原因是D,表中5min~6min之间数值发生变化,可能的原因是A.
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.
16.如图是煤化工产业链的一部分,试运用所学知识,解决下列问题:
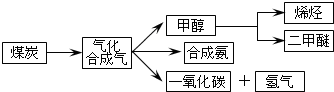
I.已知该产业链中某反应的平衡表达式为:K=$\frac{{c({H_2})•c({CO})}}{{c({H_2}O)}}$,它所对应反应的化学方程式为C(s)+H2O(g)?CO(g)+H2(g);
II.二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用,工业上以CO和H2为原料生产CH3OCH3.工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g)?CH3OH(g)△H1=-90.7kJ•mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-23.5kJ•mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g)△H3=-41.2kJ•mol-1
(1)催化反应室中总反应的热化学方程式为3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)△H=-247kJ•mol-1,830℃时反应③的K=1.0,则在催化反应室中反应③的K>1.0(填“>”、“<”或“=”).
(2)在某温度下,若反应①的起始浓度分别为:c(CO)=1mol/L,c(H2)=2.4mol/L,5min后达到平衡,CO的转化率为50%,若反应物的起始浓度分别为:c(CO)=4mol/L,c(H2)=a mol/L;达到平衡后,c(CH3OH)=2mol/L,a=5.4mol/L.
(3)反应②在t℃时的平衡常数为400,此温度下,在0.5L的密闭容器中加入一定量的甲醇,反应到某时刻测得各组分的物质的量浓度如下:
①此时刻,v正大于 v逆(填“大于”、“小于”或“等于”).
②平衡时二甲醚的物质的量浓度是1.6mol/L.

I.已知该产业链中某反应的平衡表达式为:K=$\frac{{c({H_2})•c({CO})}}{{c({H_2}O)}}$,它所对应反应的化学方程式为C(s)+H2O(g)?CO(g)+H2(g);
II.二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用,工业上以CO和H2为原料生产CH3OCH3.工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g)?CH3OH(g)△H1=-90.7kJ•mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-23.5kJ•mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g)△H3=-41.2kJ•mol-1
(1)催化反应室中总反应的热化学方程式为3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)△H=-247kJ•mol-1,830℃时反应③的K=1.0,则在催化反应室中反应③的K>1.0(填“>”、“<”或“=”).
(2)在某温度下,若反应①的起始浓度分别为:c(CO)=1mol/L,c(H2)=2.4mol/L,5min后达到平衡,CO的转化率为50%,若反应物的起始浓度分别为:c(CO)=4mol/L,c(H2)=a mol/L;达到平衡后,c(CH3OH)=2mol/L,a=5.4mol/L.
(3)反应②在t℃时的平衡常数为400,此温度下,在0.5L的密闭容器中加入一定量的甲醇,反应到某时刻测得各组分的物质的量浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| c/(mol•L-1) | 0.8 | 1.24 | 1.24 |
②平衡时二甲醚的物质的量浓度是1.6mol/L.
15.在2L密闭容器中进行反应:mX(g)+nY(g)?pZ(g)+qQ(g),式中m、n、p、q为化学计量数.在0~3min内,各物质物质的量的变化如表所示:
已知:2min内v(Q)=0.075mol•L-1•min-1,v(Z):v(Y)=1:2.
(1)2min内Z的反应速率v(Z)=0.05mol•L-1•min-1.
(2)试确定以下物质的相关量:起始时n(Y)=2.3mol,n(Q)=3mol.
(3)方程式中m=1,n=4,p=2,q=3.
(4)对于该反应,能增大正反应速率的措施是CD
A.增大容器体积 B.移走部分Q C.通入大量X D.升高温度.
| 物质 | X | Y | Z | Q |
| 时间 | ||||
| 起始/mol | 0.7 | 1 | ||
| 2min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
| 3min末/mol | 0.8 |
(1)2min内Z的反应速率v(Z)=0.05mol•L-1•min-1.
(2)试确定以下物质的相关量:起始时n(Y)=2.3mol,n(Q)=3mol.
(3)方程式中m=1,n=4,p=2,q=3.
(4)对于该反应,能增大正反应速率的措施是CD
A.增大容器体积 B.移走部分Q C.通入大量X D.升高温度.
14.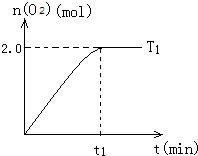 一定温度下,在2L密闭容器中加入纳米级Cu2O并通入10.0mol水蒸气,发生反应:2H2O(g)?2H2(g)+O2(g)△H=+484kJ/mol,T1温度下不同时段产生O2的量,见表:
一定温度下,在2L密闭容器中加入纳米级Cu2O并通入10.0mol水蒸气,发生反应:2H2O(g)?2H2(g)+O2(g)△H=+484kJ/mol,T1温度下不同时段产生O2的量,见表:
(1)前20min的反应速率ⅴ(H2O)=5.0×10-2 mol.L-1.min -1
(2)T1温度下,该反应的平衡常数表达式为:K=$\frac{{c}^{2}({H}_{2})×c({O}_{2})}{{c}^{2}({H}_{2}O)}$
(3)在T2温度时,K=0.4,T1> T2(填“>”“<”“=”)
(4)T1温度下,t1时刻达到平衡时的图象大致为:(见图I)
请在图I中画出降温至T0后,t0min达到平衡时的大致图象,并作必要的简单标注.
(5)H2可作氢氧燃料电池的反应物质,请写出在酸性介质中,氢氧燃料电池的负极反应式:H2-2e-=2H+.
 一定温度下,在2L密闭容器中加入纳米级Cu2O并通入10.0mol水蒸气,发生反应:2H2O(g)?2H2(g)+O2(g)△H=+484kJ/mol,T1温度下不同时段产生O2的量,见表:
一定温度下,在2L密闭容器中加入纳米级Cu2O并通入10.0mol水蒸气,发生反应:2H2O(g)?2H2(g)+O2(g)△H=+484kJ/mol,T1温度下不同时段产生O2的量,见表:| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 1.0 | 1.6 | 2.0 | 2.0 |
(2)T1温度下,该反应的平衡常数表达式为:K=$\frac{{c}^{2}({H}_{2})×c({O}_{2})}{{c}^{2}({H}_{2}O)}$
(3)在T2温度时,K=0.4,T1> T2(填“>”“<”“=”)
(4)T1温度下,t1时刻达到平衡时的图象大致为:(见图I)
请在图I中画出降温至T0后,t0min达到平衡时的大致图象,并作必要的简单标注.
(5)H2可作氢氧燃料电池的反应物质,请写出在酸性介质中,氢氧燃料电池的负极反应式:H2-2e-=2H+.
13.工业合成氨的反应如下:N2(g)+3H2(g)?2NG3(g).
某温度下,在容积恒定为2.0L的密闭容器中充入2.0molN2和2.0molH2,一段时间后反应达平衡状态,实验数据如下表所示:
(1)0~50s内的平均反应速率 v(N2)=1.2×10-3mol/(L•s).
(2)250s时,H2的转化率为30%.
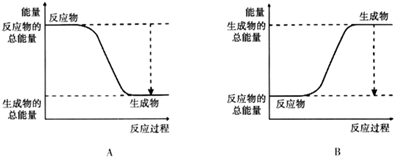
(3)已知N≡N的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1molNH3过程中的热量变化92 kJ.下图能正确表示该反应中能量变化的是A.
(4)为加快反应速率,可以采取的措施b
a.降低温度 b.增大压强 c.恒容时充入He气d.恒压时充入He气 e.及时分离NH3
(5)下列说法错误的是d
a.使用催化剂是为了加快反应速率,提高生产效率
b.上述条件下,N2不可能100%转化为NH3
c.为了提高N2的转化率,应适当提高H2的浓度
d.250~350s生成物浓度保持不变,反应停止.
0 160210 160218 160224 160228 160234 160236 160240 160246 160248 160254 160260 160264 160266 160270 160276 160278 160284 160288 160290 160294 160296 160300 160302 160304 160305 160306 160308 160309 160310 160312 160314 160318 160320 160324 160326 160330 160336 160338 160344 160348 160350 160354 160360 160366 160368 160374 160378 160380 160386 160390 160396 160404 203614
某温度下,在容积恒定为2.0L的密闭容器中充入2.0molN2和2.0molH2,一段时间后反应达平衡状态,实验数据如下表所示:
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(NH3) | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
(2)250s时,H2的转化率为30%.
(3)已知N≡N的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1molNH3过程中的热量变化92 kJ.下图能正确表示该反应中能量变化的是A.

(4)为加快反应速率,可以采取的措施b
a.降低温度 b.增大压强 c.恒容时充入He气d.恒压时充入He气 e.及时分离NH3
(5)下列说法错误的是d
a.使用催化剂是为了加快反应速率,提高生产效率
b.上述条件下,N2不可能100%转化为NH3
c.为了提高N2的转化率,应适当提高H2的浓度
d.250~350s生成物浓度保持不变,反应停止.