13.恒温恒容,可逆反应:2NO2?2NO+O2达到平衡状态的标志是( )
①单位时间内生成n molO2的同时生成2n molNO2
②2v(NO2、正)=v(O2、逆)
③用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态.
①单位时间内生成n molO2的同时生成2n molNO2
②2v(NO2、正)=v(O2、逆)
③用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态.
| A. | ①④⑥ | B. | ②③⑤ | C. | ①③④ | D. | ①②③④⑤⑥ |
12.把足量放锌放入盛有一定体积的稀硫酸的试管中,能使反应速率降低且不影响氢气产生量的因素是( )
| A. | 加入少量CuSO4溶液 | B. | 加入少量K2SO4溶液 | ||
| C. | 加入少量的Na2CO3溶液 | D. | 将稀硫酸换为浓硫酸 |
11.下列措施不能使3Fe(s)+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4(s)+4H2(g)反应速率改变的是( )
①增加铁的用量
②恒压下增加水的用量
③用铁粉代替铁屑
④升温
⑤压强不变,充入N2使容器体积增大.
①增加铁的用量
②恒压下增加水的用量
③用铁粉代替铁屑
④升温
⑤压强不变,充入N2使容器体积增大.
| A. | ① | B. | ②③④ | C. | ①②④ | D. | ①②⑤ |
10.某同学为研究电化学原理,使用KCl盐桥设计如图所示实验装置.下列分析不合理的是( )
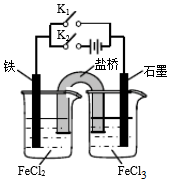

| A. | 闭合K1断开K2,左侧烧杯中的FeCl2溶液浓度逐渐增大 | |
| B. | 闭合K2断开K1,左侧烧杯中的Fe2+向铁电极移动 | |
| C. | 闭合K1断开K2,电流从石墨电极经过K1流向铁电极 | |
| D. | 无论闭合K1断开K2,还是断开K1闭合K2,石墨电极上发生的反应都是Fe3++e-=Fe2+ |
9.下列有关反应限度的叙述正确的是( )
| A. | 当温度一定时,不同的起始条件下可逆反应建立平衡状态时,平衡常数和转化率一定是定值 | |
| B. | 依据焓判据:NH4HCO3受热分解可自发进行 | |
| C. | 大多数化学反应在一定条件下都有一定的限度 | |
| D. | FeCl3与KSCN反应达到平衡时,向其中滴加少量KCl溶液,则溶液颜色变深 |
5.当可逆反应2SO2(g)+O2(g)?2SO3(g)达到平衡后,通入18O2气体,再次达到平衡时18O存在于( )
0 160200 160208 160214 160218 160224 160226 160230 160236 160238 160244 160250 160254 160256 160260 160266 160268 160274 160278 160280 160284 160286 160290 160292 160294 160295 160296 160298 160299 160300 160302 160304 160308 160310 160314 160316 160320 160326 160328 160334 160338 160340 160344 160350 160356 160358 160364 160368 160370 160376 160380 160386 160394 203614
| A. | SO2、O2、SO3中 | B. | SO3中 | C. | SO2、O2中 | D. | SO2、SO3中 |
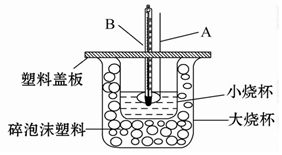
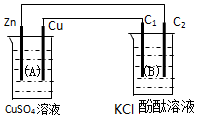 按如图装置进行实验,图中C1、C2均为石墨棒.请回答下列问题.
按如图装置进行实验,图中C1、C2均为石墨棒.请回答下列问题.