3.某化学反应2A (g)?B(g)+D(g) 在4种不同条件下进行,B和D的起始浓度为0,反应物A 的浓度(mol•L-1) 随反应时间 (min) 的变化情况如下表:
根据上述数据,完成下列填空:
(1)实验1达到平衡的时间是40min,实验4达到平衡的时间是30min.
(2)C1大于C2 (填“大于”“小于”“等于”);C3=1.0mol•L-1
(3)实验4比实验1的反应速率快(填“快”或“慢”),原因是实验4的温度比实验1高,温度越高,反应越快
(4)如果2A (g)?B(g)+D(g) 是一个放热反应,那么实验4与实验1相比,实验1 放出的热量多,理由是升高温度平衡向逆方向移动.
实验 序号 | 时间 浓度 温 度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | c1 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | 1.0 | c2 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)实验1达到平衡的时间是40min,实验4达到平衡的时间是30min.
(2)C1大于C2 (填“大于”“小于”“等于”);C3=1.0mol•L-1
(3)实验4比实验1的反应速率快(填“快”或“慢”),原因是实验4的温度比实验1高,温度越高,反应越快
(4)如果2A (g)?B(g)+D(g) 是一个放热反应,那么实验4与实验1相比,实验1 放出的热量多,理由是升高温度平衡向逆方向移动.
1.氨是氮循环中的重要物质,氨的合成是目前普遍使用的人工固氮方法.
(1)已知:H-H键能为436kJ•mol-1,N≡N键能为945kJ•mol-1,N-H键能为391kJ?mol-1.写出合成氨反应的热化学方程式N2(g)+3H2(g)?2NH3(g)△H=-93kJ•mol-1.
(2)恒温下,往一个2L的密闭容器中充入2.6mol H2和1mol N2,反应过程中对NH3的浓度进行检测,得到的数据如表所示:
5min内,消耗N2的平均反应速率为0.008mol•L-1•min-1,此条件下该反应的化学平衡常数K=0.1[或0.1(mol•L-1)-2];反应达到平衡后,若往平衡体系中加入H2、N2和NH3各2mol,化学平衡将向逆反应方向移动(填“正反应”或“逆反应”).
(1)已知:H-H键能为436kJ•mol-1,N≡N键能为945kJ•mol-1,N-H键能为391kJ?mol-1.写出合成氨反应的热化学方程式N2(g)+3H2(g)?2NH3(g)△H=-93kJ•mol-1.
(2)恒温下,往一个2L的密闭容器中充入2.6mol H2和1mol N2,反应过程中对NH3的浓度进行检测,得到的数据如表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol•L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
18.下列物质中有非极性共价键的是( )
| A. | 单质碘 | B. | 硫化氢 | C. | 氯化镁 | D. | 氢氧化钠 |
17.下列元素不属于主族元素的是( )
| A. | 钙 | B. | 铜 | C. | 溴 | D. | 铯 |
16.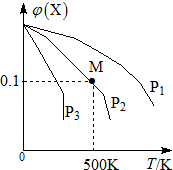 某可逆反应为2X(g)?3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示,下列推断正确的是( )
某可逆反应为2X(g)?3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示,下列推断正确的是( )
 某可逆反应为2X(g)?3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示,下列推断正确的是( )
某可逆反应为2X(g)?3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示,下列推断正确的是( )| A. | 在该条件下M点X平衡转化率为$\frac{9}{11}$ | |
| B. | 压强大小有P3>P2>P1 | |
| C. | 平衡后加入高效催化剂使气体相对分子质量增大 | |
| D. | 升高温度,该反应平衡常数K减小 |
15.PCl3和PCl5都是重要的化工原料.将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中,在一定条件下发生下述反应,并于10min时达到平衡:PCl3(g)+Cl2(g)?PCl5(g)△H<0.有关数据如下:
下列判断不正确的是( )
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度/(mol/L) | 2.0 | 1.0 | 0 |
| 平衡浓度/(mol/L) | c1 | c2 | 0.4 |
| A. | 10 min内,v(Cl2)=0.04 mol/(L•min) | |
| B. | 升高温度,反应的平衡常数减小,则平衡时PCl3的转化率变大 | |
| C. | 当容器中Cl2为1.2 mol时,反应达到平衡 | |
| D. | 平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L |
14.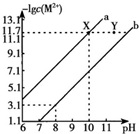 25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[-lgC(M2+)]与溶液PH的变化关系如图所示,已知:该温度下,Ksp[Cu(OH)2]<Ksp[Fe(OH)2].下列说法正确的是( )
25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[-lgC(M2+)]与溶液PH的变化关系如图所示,已知:该温度下,Ksp[Cu(OH)2]<Ksp[Fe(OH)2].下列说法正确的是( )
0 160187 160195 160201 160205 160211 160213 160217 160223 160225 160231 160237 160241 160243 160247 160253 160255 160261 160265 160267 160271 160273 160277 160279 160281 160282 160283 160285 160286 160287 160289 160291 160295 160297 160301 160303 160307 160313 160315 160321 160325 160327 160331 160337 160343 160345 160351 160355 160357 160363 160367 160373 160381 203614
 25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[-lgC(M2+)]与溶液PH的变化关系如图所示,已知:该温度下,Ksp[Cu(OH)2]<Ksp[Fe(OH)2].下列说法正确的是( )
25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[-lgC(M2+)]与溶液PH的变化关系如图所示,已知:该温度下,Ksp[Cu(OH)2]<Ksp[Fe(OH)2].下列说法正确的是( )| A. | b线表示Fe(OH)2饱和溶液中的变化关系,且Ksp[Fe(OH)2]=10-15.1 | |
| B. | 当Fe(OH)2和Cu(OH)2沉淀共存时,溶液中C(Fe2+):C(Cu2+)=1:104.6 | |
| C. | 向X点对应的饱和溶液中加入少量NaOH,可转化为Y点对应的溶液 | |
| D. | 除去CuSO4溶液中含有的少量Fe2+,可加入适量CuO |
 如图所示①②③④分别是几种常见漏斗的上部,A、B、C、D是实际操作应用时,各漏斗的下部插入容器中的示意图.请指出A、B、C、D分别与①②③④相匹配的可能组合:A与③; B与②④(或①②④);C与①; D与④.
如图所示①②③④分别是几种常见漏斗的上部,A、B、C、D是实际操作应用时,各漏斗的下部插入容器中的示意图.请指出A、B、C、D分别与①②③④相匹配的可能组合:A与③; B与②④(或①②④);C与①; D与④.