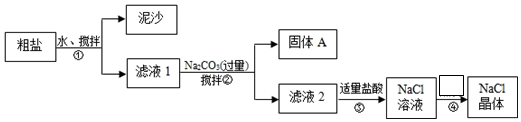
12.下列实验操作正确的是( )
①用50mL量筒量取5.2mL稀硫酸;
②用分液漏斗分离苯和四氯化碳的混合物
③用托盘天平称量17.7g氯化钠晶体
④向小试管中加入100ml稀盐酸.
①用50mL量筒量取5.2mL稀硫酸;
②用分液漏斗分离苯和四氯化碳的混合物
③用托盘天平称量17.7g氯化钠晶体
④向小试管中加入100ml稀盐酸.
| A. | ①② | B. | ②③ | C. | ③ | D. | ②④ |
9.下列有关化学用语正确的是( )
| A. | NH4Cl的电子式: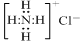 | |
| B. | 2-硝基甲苯的结构简式: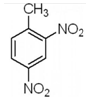 | |
| C. | 硫原子结构示意图: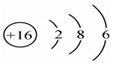 | |
| D. | 质子数为94、中子数为144的钚原子:${\;}_{94}^{144}$Pu |
8.甲醇是重要的化学工业基础原料和清洁液体燃料.工业上可利用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如表所示:
(1)据反应①与②可推导出K1、K2与K3之间的关系,则K3=K1•K2(用K1、K2表示).500℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol•L-1)分别为0.8、0.1、0.3、0.15,则此时v正>v逆(填“>”、“=”或“<”).
(2)对于反应③,在相同温度和容积不变时,能说明该反应已达平衡状态的是BC
A.n(CO2):n(H2):n(CH3OH):n(H2O)=1:3:1:1
B.容器内压强保持不变
C.H2的消耗速率与CH3OH的消耗速率之比为3:1
D.容器内的密度保持不变.
| 化学反应 | 平衡 常数 | 温度/℃ | |
| 500 | 800 | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)?H2O(g)+CO(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O(g) | K3 | ||
(2)对于反应③,在相同温度和容积不变时,能说明该反应已达平衡状态的是BC
A.n(CO2):n(H2):n(CH3OH):n(H2O)=1:3:1:1
B.容器内压强保持不变
C.H2的消耗速率与CH3OH的消耗速率之比为3:1
D.容器内的密度保持不变.
6.如图为用球棍模型表示的某有机反应过程的示意图,该反应的类型是( )
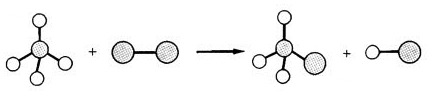

| A. | 取代反应 | B. | 加成反应 | C. | 聚合反应 | D. | 氧化反应 |
5.对于溶液中的反应,不影响反应速率的因素是( )
| A. | 温度 | B. | 压强 | C. | 浓度 | D. | 催化剂 |
4.羟基的化学符号是( )
0 160161 160169 160175 160179 160185 160187 160191 160197 160199 160205 160211 160215 160217 160221 160227 160229 160235 160239 160241 160245 160247 160251 160253 160255 160256 160257 160259 160260 160261 160263 160265 160269 160271 160275 160277 160281 160287 160289 160295 160299 160301 160305 160311 160317 160319 160325 160329 160331 160337 160341 160347 160355 203614
| A. | -NO2 | B. | -OH | C. | -COOH | D. | OH- |