13.反应 X (s)+3Y (g)?2Z (g)+Q(Q>0)处于平衡状态,为了使平衡向生成Z的方向移动,应选择的条件是( )
| A. | 升高温度 | B. | 降低压强 | C. | 及时分离出Z | D. | 使用催化剂 |
12. 丰富的CO2完全可以作为新碳源,解决当前应用最广泛的碳源(石油和天然气)到本世纪中叶将枯竭的危机.
丰富的CO2完全可以作为新碳源,解决当前应用最广泛的碳源(石油和天然气)到本世纪中叶将枯竭的危机.
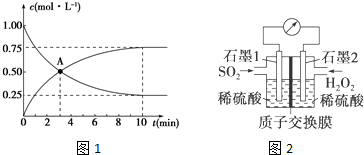
(1)目前工业上有一种方法是用CO2和H2在230℃催化剂条件下转化生成甲醇(CH3OH)蒸汽和水蒸气CO2(g)+3H2(g)?CH3OH(g)+H2O(g).如图表示恒压容器中充入1mol CO2和3mol H2,转化率达50%时放出热量19.6KJ写出该反应的热化学方程式:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-39.2 kJ•mol-1.
(2)另外工业上还可用CO和H2制备甲醇. 反应为CO(g)+2H2(g)═CH3OH(g),某温度下,在容积为2L的恒容密闭容器中进行该反应,其相关数据如图:t min至2t min时速率变化的原因可能是升温或使用了催化剂;
(3)CO2在一定条件下,还可以与H2合成二甲醚:2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g).
将2.5mol H2与b mol CO2置于容积为1L的密闭容器中,发生上述反应,达到平衡状态时,测得实验数据如表:
①降温时,上述平衡向正反应方向移动(填“正反应”或“逆反应”).
②表中y、z的大小关系为B.
A.y=z B.y>z C.y<z D.无法判断
③表中x、y、z、w对应的平衡常数分别为Kx、Ky、Kz、Kw,它们之间的大小关系为Kx>Kz>Ky=Kw.
 丰富的CO2完全可以作为新碳源,解决当前应用最广泛的碳源(石油和天然气)到本世纪中叶将枯竭的危机.
丰富的CO2完全可以作为新碳源,解决当前应用最广泛的碳源(石油和天然气)到本世纪中叶将枯竭的危机.(1)目前工业上有一种方法是用CO2和H2在230℃催化剂条件下转化生成甲醇(CH3OH)蒸汽和水蒸气CO2(g)+3H2(g)?CH3OH(g)+H2O(g).如图表示恒压容器中充入1mol CO2和3mol H2,转化率达50%时放出热量19.6KJ写出该反应的热化学方程式:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-39.2 kJ•mol-1.
(2)另外工业上还可用CO和H2制备甲醇. 反应为CO(g)+2H2(g)═CH3OH(g),某温度下,在容积为2L的恒容密闭容器中进行该反应,其相关数据如图:t min至2t min时速率变化的原因可能是升温或使用了催化剂;
(3)CO2在一定条件下,还可以与H2合成二甲醚:2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g).
将2.5mol H2与b mol CO2置于容积为1L的密闭容器中,发生上述反应,达到平衡状态时,测得实验数据如表:
 | 500 | 600 | 700 | 800 |
| 1.67 | X | 33 | ||
| 1.25 | 60 | 43 | Y | |
| 0.83 | Z | 32w |
②表中y、z的大小关系为B.
A.y=z B.y>z C.y<z D.无法判断
③表中x、y、z、w对应的平衡常数分别为Kx、Ky、Kz、Kw,它们之间的大小关系为Kx>Kz>Ky=Kw.
10.在一定条件下,发生反应:aA(g)+bB(g)?cC(g)△H=“Q“kJ/mol,其化学平衡常数K和温度的关系如表所示:
(1)依据图表判断该反应△H< 0(填“>”或“<”).
(2)500℃,固定容器的密闭容器中,放入混合物,其始浓度为c(A)=0.25mol/L,c(B)=0.60mol/L,c(C)=0.30mol/L,则反应开始时,B的消耗速率比生成速率不能确定 (填“大”、“小”或“不能确定”).
| t℃ | 400 | 500 | 800 | 1000 |
| K | 2.6 | 1.6 | 1.0 | 0.40 |
(2)500℃,固定容器的密闭容器中,放入混合物,其始浓度为c(A)=0.25mol/L,c(B)=0.60mol/L,c(C)=0.30mol/L,则反应开始时,B的消耗速率比生成速率不能确定 (填“大”、“小”或“不能确定”).
8.二甲醚(DME)被誉为“21世纪的清洁燃料”.由合成气制备二甲醚的主要原理如下:
反应Ⅰ:CO(g)+2H2(g)?CH3OH(g)△H1
反应Ⅱ:2CH3OH(g)?CH3OCH3(g)+H2O(g)、△H2
反应Ⅲ:2CO(g)+4H2(g)?CH3OCH3(g)+H2O(g)△H3
相关反应在不同温度时的平衡常数及其大小关系如表所示
回答下列问题:
(1)反应Ⅰ的自发性可能自发(填“一定自发”、“可能自发”或“一定不自发”);反应Ⅱ的平衡常数表达式为$\frac{c({H}_{2}O)•c(C{H}_{3}OC{H}_{3})}{{c}^{2}(C{H}_{3}OH)}$,反应Ⅲ的△H3和△H1、△H2的关系△H3=2×△H1+△H2反应.
(2)在合成过程中,因为有CO(g)+H2O(g)?CO2(g)+H2(g)反应发生,所以能提高CH3OCH3的产率,原因是此反应消耗了H2O(g)有利于反应II、III正向移动;同时此反应生成了H2,有利于反应I、III正向移动.
(3)如图1两条曲线分别表示反应I(按物质的量比:n(CO):n(H2)=1:2)中压强为0.1MPa和5.0MPa下CO转化率随温度的变化关系,计算压强为5.0MPa、温度为200℃时,平衡混合气中甲醇的物质的量分数是43.75%.

(4)反应Ⅲ逆反应速率与时间的关系如图2所示:
①试判断t2时改变的条件是增大生成物C浓度或升高温度.
②若t4扩大容器体积,t5达到平衡,t6时增大反应物浓度,请在上图中画出t4-t6的变化曲线.
反应Ⅰ:CO(g)+2H2(g)?CH3OH(g)△H1
反应Ⅱ:2CH3OH(g)?CH3OCH3(g)+H2O(g)、△H2
反应Ⅲ:2CO(g)+4H2(g)?CH3OCH3(g)+H2O(g)△H3
相关反应在不同温度时的平衡常数及其大小关系如表所示
| 温度/K | 反应I | 反应Ⅱ | 已知: K1>K2>K1′>K2′ |
| 298 | K1 | K2 | |
| 328 | K1′ | K2′ |
(1)反应Ⅰ的自发性可能自发(填“一定自发”、“可能自发”或“一定不自发”);反应Ⅱ的平衡常数表达式为$\frac{c({H}_{2}O)•c(C{H}_{3}OC{H}_{3})}{{c}^{2}(C{H}_{3}OH)}$,反应Ⅲ的△H3和△H1、△H2的关系△H3=2×△H1+△H2反应.
(2)在合成过程中,因为有CO(g)+H2O(g)?CO2(g)+H2(g)反应发生,所以能提高CH3OCH3的产率,原因是此反应消耗了H2O(g)有利于反应II、III正向移动;同时此反应生成了H2,有利于反应I、III正向移动.
(3)如图1两条曲线分别表示反应I(按物质的量比:n(CO):n(H2)=1:2)中压强为0.1MPa和5.0MPa下CO转化率随温度的变化关系,计算压强为5.0MPa、温度为200℃时,平衡混合气中甲醇的物质的量分数是43.75%.

(4)反应Ⅲ逆反应速率与时间的关系如图2所示:
①试判断t2时改变的条件是增大生成物C浓度或升高温度.
②若t4扩大容器体积,t5达到平衡,t6时增大反应物浓度,请在上图中画出t4-t6的变化曲线.
7. 2013年12月17日,中国国土资源部召开新闻发布会,宣布在广东沿海珠江口盆地东部海域首次钻获高纯度可燃冰.可燃冰的主要成分是甲烷,甲烷既是清洁的燃料,也是重要的化工原料.
2013年12月17日,中国国土资源部召开新闻发布会,宣布在广东沿海珠江口盆地东部海域首次钻获高纯度可燃冰.可燃冰的主要成分是甲烷,甲烷既是清洁的燃料,也是重要的化工原料.
(1)甲烷和二氧化碳重整制合成气,对于温室气体的治理具有重大意义.
已知:CH4(g)+CO2(g)?2CO(g)+2H2(g)△H=+247.3kJ•mol-1
CH4(g)?C(s)+2H2(g)△H=+75kJ•mol-1
①反应2CO(g)═C(s)+CO2(g)在一定条件下能自发进行的原因是△H<0.
②合成甲醇的主要反应是:2H2(g)+CO(g)?CH3OH(g)△H=-90.8kJ•mol-1,T℃下此反应的平衡常数为160.某时刻测得各组分的浓度如下:
比较此时正、逆反应速率的大小:v(正)>v(逆)(填“>”、“<”或“=”).生产过程中,合成气要进行循环,其目的是提高原料的利用率.
③在一恒容密闭容器中,要提高反应2H2(g)+CO(g)?CH3OH(g) 中CO的转化率,可以采取的措施是df.
a.升温 b.加入催化剂 c.增加CO的浓度
d.加入H2 e.加入惰性气体 f.分离出甲醇
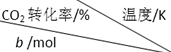
(2)以甲烷为燃料的新型电池,其成本大大低于以氢为燃料的传统燃料电池,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图(如图).
①B极为电池负极,电极反应式为CH4+4O2--8e-=CO2+2H2O.
②若用该燃料电池作电源,用石墨作电极电解100mL 1mol/L的硫酸铜溶液,当两极收集到的气体体积相等时,理论上消耗甲烷的体积为1.12 L(标况下).
 2013年12月17日,中国国土资源部召开新闻发布会,宣布在广东沿海珠江口盆地东部海域首次钻获高纯度可燃冰.可燃冰的主要成分是甲烷,甲烷既是清洁的燃料,也是重要的化工原料.
2013年12月17日,中国国土资源部召开新闻发布会,宣布在广东沿海珠江口盆地东部海域首次钻获高纯度可燃冰.可燃冰的主要成分是甲烷,甲烷既是清洁的燃料,也是重要的化工原料.(1)甲烷和二氧化碳重整制合成气,对于温室气体的治理具有重大意义.
已知:CH4(g)+CO2(g)?2CO(g)+2H2(g)△H=+247.3kJ•mol-1
CH4(g)?C(s)+2H2(g)△H=+75kJ•mol-1
①反应2CO(g)═C(s)+CO2(g)在一定条件下能自发进行的原因是△H<0.
②合成甲醇的主要反应是:2H2(g)+CO(g)?CH3OH(g)△H=-90.8kJ•mol-1,T℃下此反应的平衡常数为160.某时刻测得各组分的浓度如下:
| 物质 | H2 | CO | CH3OH |
| 浓度/(mol•L-1) | 0.20 | 0.10 | 0.40 |
③在一恒容密闭容器中,要提高反应2H2(g)+CO(g)?CH3OH(g) 中CO的转化率,可以采取的措施是df.
a.升温 b.加入催化剂 c.增加CO的浓度
d.加入H2 e.加入惰性气体 f.分离出甲醇
(2)以甲烷为燃料的新型电池,其成本大大低于以氢为燃料的传统燃料电池,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图(如图).
①B极为电池负极,电极反应式为CH4+4O2--8e-=CO2+2H2O.
②若用该燃料电池作电源,用石墨作电极电解100mL 1mol/L的硫酸铜溶液,当两极收集到的气体体积相等时,理论上消耗甲烷的体积为1.12 L(标况下).
6.甲醇是21世纪应用最广泛的清洁燃料之一,通过下列反应可以制备甲醇:
CO ( g )+2H2( g )?CH3OH ( l )△H
(1)已知:
计算上述反应的△H=-128.1 kJ•mol-1.
(2)在容积可变的密闭容器中充入1mol CO ( g )和2molH2( g )生成CH3OH( g ),H2的平衡转
化率随温度(T)、压强(P)的变化如图1所示.
①该反应的△S<0,图中的T1<T2(填“<”、“>”或“=”).
②当达到平衡状态A 时,容器的体积为2L,此时该反应的平衡常数为4,若达到平衡状态B 时,则容器的体积V(B)=0.4L.
(3)在容积固定为2L的密闭容器中充入2molCO( g )和6molH2( g )生成CH3OH( g ),反应时间与物质的量浓度的关系如图2所示,则前10分钟内,氢气的平均反应速率为0.16mol•L-1•min-1;若15分钟时升高体系温度,在20分钟时达到新平衡,此时氢气的转化率为33.3%,请在图2中画出15-25分钟c(CO)的变化曲线.

CO ( g )+2H2( g )?CH3OH ( l )△H
(1)已知:
| 化学式 | H2(g) | CO(g) | CH3OH(l) |
| 标准燃烧热(25℃) △H/kJ•mol-1 | -285.8 | -283.0 | -726.5 |
(2)在容积可变的密闭容器中充入1mol CO ( g )和2molH2( g )生成CH3OH( g ),H2的平衡转
化率随温度(T)、压强(P)的变化如图1所示.
①该反应的△S<0,图中的T1<T2(填“<”、“>”或“=”).
②当达到平衡状态A 时,容器的体积为2L,此时该反应的平衡常数为4,若达到平衡状态B 时,则容器的体积V(B)=0.4L.
(3)在容积固定为2L的密闭容器中充入2molCO( g )和6molH2( g )生成CH3OH( g ),反应时间与物质的量浓度的关系如图2所示,则前10分钟内,氢气的平均反应速率为0.16mol•L-1•min-1;若15分钟时升高体系温度,在20分钟时达到新平衡,此时氢气的转化率为33.3%,请在图2中画出15-25分钟c(CO)的变化曲线.

5.下列化学用语表达正确的是( )
0 160151 160159 160165 160169 160175 160177 160181 160187 160189 160195 160201 160205 160207 160211 160217 160219 160225 160229 160231 160235 160237 160241 160243 160245 160246 160247 160249 160250 160251 160253 160255 160259 160261 160265 160267 160271 160277 160279 160285 160289 160291 160295 160301 160307 160309 160315 160319 160321 160327 160331 160337 160345 203614
| A. | F-的原子结构示意图: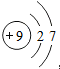 | B. | 乙烯的结构简式:CH2CH2 | ||
| C. | 葡萄糖的分子式:C6H12O6 | D. | 二氧化碳的电子式: |