5.误服重金属盐使人中毒,应及时采用哪种措施救助?( )
| A. | 喝大量冷开水 | B. | 喝大量食盐水 | ||
| C. | 喝大量牛奶 | D. | 注射大量葡萄糖水 |
4.某溶液可能含有Cl-、SO42-、CO32-、HCO3-、NH4+、Fe3+、Ba2+和K+,取该溶液100mL,加入过量NaOH溶液加热,得到0.02mol气体,同时产生1.97g白色沉淀;向上述滤液中加足量BaCl2溶液,也得到1.97g沉淀.由此可知原溶液中( )
| A. | 至少存在5种离子 | |
| B. | Cl-一定存在,且c(Cl-)≥0.2mol/L | |
| C. | SO42-、NH4+、Fe3+一定存在,Al3+、K+、Cl-可能存在 | |
| D. | CO32-一定不存在,SO42-、NH4+、Fe3+、Cl-一定存在 |
3.等物质的量浓度、等体积的氢氧化钠溶液和醋酸溶液完全反应后,溶液中有关离子浓度之间不存在的关系是( )
| A. | c(H+)•c(OH-)=KW | B. | c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | ||
| C. | c(Na+)=c(CH3COO-)+c(OH-) | D. | c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
2. 汽车尾气是造成雾霾天气的原因之一.
汽车尾气是造成雾霾天气的原因之一.
(1)汽车尾气中含有CO、NO2等有毒气体对汽车加装尾气净化装置可使有毒气体相互反应转化为无毒气体. 写出该反应的热化学方程式4CO(g)+2NO2(g)=4CO2(g)+N2(g)△=-1200.0kJ/mol.
N2(g)+2O2(g)═2NO2(g)△H=+68.0kJ•mol-1;
2C(s)+O2(g)═2CO(g)△H=-221.0kJ•mol-1;
C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
(2)汽车尾气中含有CO和H2O(g)在一定条件下可以发生反应
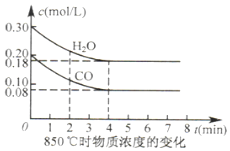
CO(g)+H2O(g)?CO2(g)+H2(g)△H<0.850℃在体积为10L反应器中通入一定量的CO和H2O(g)发生上述反应CO和H2O(g)的浓度变化如图所示则0-4min是平均反应速率v(H2O)=0.03mol•L-1•min-1此时K=1.
850℃在甲、乙、丙三个1L的恒容密闭容器中,起始时按照表进行投料,达到平衡状态.平衡时甲容器中CO的转化率是50%.比较下列容器中CO的转化率甲<乙(填“大于”、“<”或“等于”).
 汽车尾气是造成雾霾天气的原因之一.
汽车尾气是造成雾霾天气的原因之一.(1)汽车尾气中含有CO、NO2等有毒气体对汽车加装尾气净化装置可使有毒气体相互反应转化为无毒气体. 写出该反应的热化学方程式4CO(g)+2NO2(g)=4CO2(g)+N2(g)△=-1200.0kJ/mol.
N2(g)+2O2(g)═2NO2(g)△H=+68.0kJ•mol-1;
2C(s)+O2(g)═2CO(g)△H=-221.0kJ•mol-1;
C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
(2)汽车尾气中含有CO和H2O(g)在一定条件下可以发生反应
CO(g)+H2O(g)?CO2(g)+H2(g)△H<0.850℃在体积为10L反应器中通入一定量的CO和H2O(g)发生上述反应CO和H2O(g)的浓度变化如图所示则0-4min是平均反应速率v(H2O)=0.03mol•L-1•min-1此时K=1.
| 起始物质的量 | 甲 | 乙 | 丙 |
| n(H2O)/mol | 0.10 | 0.20 | 0.20 |
| n(CO)/mol | 0.10 | 0.10 | 0.20 |
20.在温度相同、容积均为2L的3个恒容密闭容器中,按不同方式投入反应物,保持恒温,测得反应达到平衡时的有关数据如下,下列说法正确的是( )
(已知N2(g)+3H2(g)=2NH3(g)△H=-92.4kJ•mol-1)
| 甲 | 乙 | 丙 | |
| 反应物投入量 | 1moN2、3mol H2 | 2mol N2、6mol H2 | 2mol NH3 |
| NH3浓度(mol•L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1kJ | 放出Q2kJ | 吸收Q3kJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A. | 2p1=2p3>p2 | |
| B. | α2+α3<1 | |
| C. | 达到平衡时丙容器中NH3的体积分数最大 | |
| D. | Q1+Q3>92.4 |
19.下列实验操作中有错误的是( )
| A. | 蒸发操作时,应使混合物中的水分大部分蒸干后,停止加热,利用余热蒸干 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 浓硫酸稀释时,应该将水缓缓加入盛浓硫酸的烧杯中,边加边搅拌 | |
| D. | 萃取分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
16.Ⅰ.高炉炼铁是冶炼铁的主要方法,发生的主要反应为
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H
(1)已知:Fe2O3(s)+3C(石墨,s)=2Fe(s)+3CO(g)△H1
C(石墨,s)+CO2(g)=2CO(g)△H2
则△H=△H1-3△H2(用含△H1、△H2代数式表示)
(2)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按表所示加入物质,反应经过一段时间后达到平衡.
①甲容器中CO的平衡转化率为60%.
②下列说法正确的是B(填字母).
A.若容器压强恒定,反应达到平衡状态
B.若容器内气体密度恒定,反应达到平衡状态
C.甲容器中CO的平衡转化率大于乙的
D.增加Fe2O3就能提高CO的转化率
II.利用空气催化氧化法制取联氨,其有关物质的转化如图1所示(R1、R2代表烃基).
①在图1示的转化中,化合价不变的一种元素是氢或H.
②反应中当有1mol NH3转化为N2H4时,保持溶液中酮的物质的量不变,需要消耗O2的物质的量为0.25mol.
③在温度一定和不补加溶液的条件下,缓慢通入NH3、O2混合气体,并充分搅拌.欲使生成的N2H4中不含NH3,可采取的措施有增大混合气体中氧气的含量.
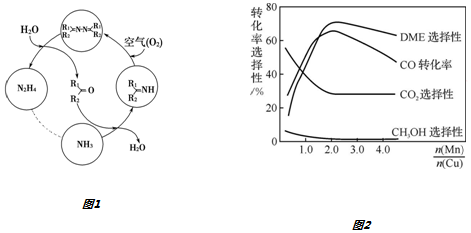
Ⅲ.采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2制备二甲醚(DME).观察如图2回答问题:催化剂中$\frac{n(Mn)}{n(Cu)}$约为2.0时最有利于二甲醚的合成.
0 160135 160143 160149 160153 160159 160161 160165 160171 160173 160179 160185 160189 160191 160195 160201 160203 160209 160213 160215 160219 160221 160225 160227 160229 160230 160231 160233 160234 160235 160237 160239 160243 160245 160249 160251 160255 160261 160263 160269 160273 160275 160279 160285 160291 160293 160299 160303 160305 160311 160315 160321 160329 203614
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H
(1)已知:Fe2O3(s)+3C(石墨,s)=2Fe(s)+3CO(g)△H1
C(石墨,s)+CO2(g)=2CO(g)△H2
则△H=△H1-3△H2(用含△H1、△H2代数式表示)
(2)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按表所示加入物质,反应经过一段时间后达到平衡.
| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 1.5 | 1.0 | 1.0 |
②下列说法正确的是B(填字母).
A.若容器压强恒定,反应达到平衡状态
B.若容器内气体密度恒定,反应达到平衡状态
C.甲容器中CO的平衡转化率大于乙的
D.增加Fe2O3就能提高CO的转化率
II.利用空气催化氧化法制取联氨,其有关物质的转化如图1所示(R1、R2代表烃基).
①在图1示的转化中,化合价不变的一种元素是氢或H.
②反应中当有1mol NH3转化为N2H4时,保持溶液中酮的物质的量不变,需要消耗O2的物质的量为0.25mol.
③在温度一定和不补加溶液的条件下,缓慢通入NH3、O2混合气体,并充分搅拌.欲使生成的N2H4中不含NH3,可采取的措施有增大混合气体中氧气的含量.

Ⅲ.采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2制备二甲醚(DME).观察如图2回答问题:催化剂中$\frac{n(Mn)}{n(Cu)}$约为2.0时最有利于二甲醚的合成.
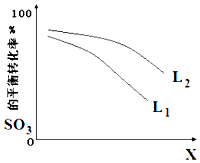 高温裂解法处理工业废硫酸的原理为:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g)△H=+550kJ/mol,它由两步反应组成:
高温裂解法处理工业废硫酸的原理为:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g)△H=+550kJ/mol,它由两步反应组成: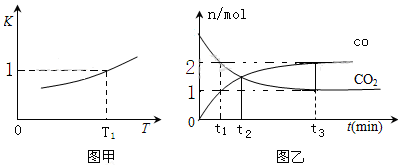
 ,W与R形成的化合物的化学式为Na3N.它们的晶体属于离子晶体.
,W与R形成的化合物的化学式为Na3N.它们的晶体属于离子晶体.