5. 甲醇被称为21世纪的新型燃料,工业上用CH4和H2O为原料通过下列反应①和②,
甲醇被称为21世纪的新型燃料,工业上用CH4和H2O为原料通过下列反应①和②,
来制备甲醇.
①CH4(g)+H2O(g)?CO(g)+3H2(g)△H
②CO(g)+2H2(g)?CH3OH(g)△H△
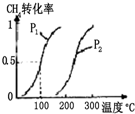
将0.20mol CH4和0.30mol H2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度、压强的关系如图:
(1)温度不变,缩小体积,①的逆反应速率增大(填“增大”、“减小”或“不变”).
(2)反应①的△H>0(填“<”“=”或“>”);
100℃时的平衡常数值K=1.35×10-3.
(3)在压强为0.1Mpa条件下,将a molCO与3a molH2的混合气体在催化剂作用下进行反应②
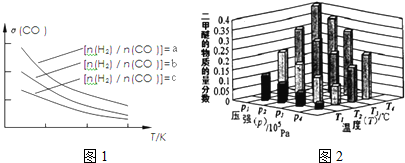
再生成甲醇.为了发寻找合成甲醇的适宜的温度和压强,某同学设计了二组实验,部分实验条件已经填在下面实验设计表中.请在空格中填入剩余的实验条件数据.
300°C时,其他条件不变,将容器的容积压缩到原来的$\frac{1}{2}$,对平衡体系产生的影响是(填
字母)CD
A.c(H2)减少
B.正反应速率加快,逆反应速率减慢
C.CH3OH的物质的量增加D.重新平衡时c(H2)/c(CH2OH)减小
(4)已知在常温常压下:
①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△△H1=-1275.6kJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△△H2=-556.0kJ•mol-1
③H2O(g)═H2O(l)△△H3=-44.0kJ•mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ•mol-1.
(5)据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电.其电池
反应为:2CH3OH+3O2+4OH-?2CO32-+6H2O,放电时负极的电极反应方程为:CH3OH-6e-+8OH-=CO32-+6H2O.
 甲醇被称为21世纪的新型燃料,工业上用CH4和H2O为原料通过下列反应①和②,
甲醇被称为21世纪的新型燃料,工业上用CH4和H2O为原料通过下列反应①和②,来制备甲醇.
①CH4(g)+H2O(g)?CO(g)+3H2(g)△H
②CO(g)+2H2(g)?CH3OH(g)△H△
将0.20mol CH4和0.30mol H2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度、压强的关系如图:
(1)温度不变,缩小体积,①的逆反应速率增大(填“增大”、“减小”或“不变”).
(2)反应①的△H>0(填“<”“=”或“>”);
100℃时的平衡常数值K=1.35×10-3.
(3)在压强为0.1Mpa条件下,将a molCO与3a molH2的混合气体在催化剂作用下进行反应②
再生成甲醇.为了发寻找合成甲醇的适宜的温度和压强,某同学设计了二组实验,部分实验条件已经填在下面实验设计表中.请在空格中填入剩余的实验条件数据.
| 实验编号 | T(°C) | n(CO)/n(H2) | p(MPa) |
| Ⅰ | 150 | 1/3 | 0.1 |
| Ⅱ | 5 | ||
| Ⅲ | 350 | 5 |
字母)CD
A.c(H2)减少
B.正反应速率加快,逆反应速率减慢
C.CH3OH的物质的量增加D.重新平衡时c(H2)/c(CH2OH)减小
(4)已知在常温常压下:
①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△△H1=-1275.6kJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△△H2=-556.0kJ•mol-1
③H2O(g)═H2O(l)△△H3=-44.0kJ•mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ•mol-1.
(5)据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电.其电池
反应为:2CH3OH+3O2+4OH-?2CO32-+6H2O,放电时负极的电极反应方程为:CH3OH-6e-+8OH-=CO32-+6H2O.
4.已知下表数据:
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不科学的是( )
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp/25℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | ≥3.4 |
| A. | 向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀 | |
| B. | 该溶液中[SO42-]:([Cu2+]+[Fe2+]+[Fe3+])>5:4.([SO42-]表示SO42-物质的量浓度 ) | |
| C. | 向该溶液中加入适量氯水,并调节pH到3.4过滤,可获得纯净的CuSO4溶液 | |
| D. | 在pH=4的溶液中Fe3+不能大量存在 |
1.下列方法中,可制得Cl2的正确组合是( )
①MnO2和浓盐酸混合共热 ②KMnO4和浓盐酸混合 ③NaClO和浓盐酸混合
④K2Cr2O7和浓盐酸混合 ⑤KClO3和浓盐酸混合.
①MnO2和浓盐酸混合共热 ②KMnO4和浓盐酸混合 ③NaClO和浓盐酸混合
④K2Cr2O7和浓盐酸混合 ⑤KClO3和浓盐酸混合.
| A. | ①② | B. | ②③④ | C. | ①④ | D. | ①②③④⑤ |
20.用98%,密度为1.84g/cm3的浓硫酸配制1mol/L的稀硫酸100mL,配制过程中需要用到的仪器及使用的先后顺序排列正确的是( )
①100mL量筒 ②10mL量筒 ③50mL烧杯 ④托盘天平 ⑤100mL 容量瓶⑥胶头滴管 ⑦玻璃棒.
①100mL量筒 ②10mL量筒 ③50mL烧杯 ④托盘天平 ⑤100mL 容量瓶⑥胶头滴管 ⑦玻璃棒.
| A. | ②⑥⑤⑦⑥ | B. | ④⑥③⑦⑤⑥ | C. | ②⑥③⑦⑤⑥ | D. | ①⑥③⑤⑥⑦ |
19.下列说法正确的是( )
| A. | 共价化合物中一定不含离子键 | |
| B. | 离子化合物中一定不含共价键 | |
| C. | 金属越活泼金属键越强 | |
| D. | 双原子分子中共价键越强,沸点越高 |
18.某有机物M的结构简式为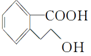 ,下列有关M的说法正确的是( )
,下列有关M的说法正确的是( )
 ,下列有关M的说法正确的是( )
,下列有关M的说法正确的是( )| A. | 该分子中存在一个手性碳原子 | |
| B. | M的分子式为C9H10O3 | |
| C. | 1 mol M能与足量Na反应生成0.5 mol H2 | |
| D. | 1 mol M完全燃烧消耗10 mol O2 |
17.在不引入新杂质的情况下,分离FeCl3、KCl、BaSO4的混合物,应选用的一组试剂是( )
0 160127 160135 160141 160145 160151 160153 160157 160163 160165 160171 160177 160181 160183 160187 160193 160195 160201 160205 160207 160211 160213 160217 160219 160221 160222 160223 160225 160226 160227 160229 160231 160235 160237 160241 160243 160247 160253 160255 160261 160265 160267 160271 160277 160283 160285 160291 160295 160297 160303 160307 160313 160321 203614
| A. | 水、氢氧化钾溶液、稀盐酸 | B. | 水、氢氧化钠溶液、稀盐酸? | ||
| C. | 水、硝酸银溶液、稀硝酸 | D. | 水、氢氧化钾溶液、稀硝酸? |