20.某反应2C(g)?A(g)+2B(g)△H<0,下列判断正确的是( )
| A. | 任何温度下反应均难以自发进行 | B. | 任何温度下反应均可以自发进行 | ||
| C. | 仅常温下反应可以自发进行 | D. | 仅高温下反应可以自发进行 |
19.下列反应不属于四种基本反应类型,但属于氧化还原反应的是( )
| A. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | B. | Cu(OH)2+2HCl═CuCl2+2H2O | ||
| C. | 2Na+2H2O═2NaOH+H2↑ | D. | 2Na2O2+2CO2═2Na2CO3+O2 |
18.一定温度下,在4个容积均为1L的容器中分别进行反应(各容器中A都足量)A(s)+B(g)?C(g)+D(g)△H=+100kJ/mol,某时刻测得部分数据如表:下列说法正确的是( )
| 容器编号 | n(B)/mol | n(C)/mol | n(D)/mol | 反应时间/min | 反应速率 |
| Ⅰ | 0.06 | 0.60 | 0.10 | t1 | v(正)=v(逆) |
| Ⅱ | 0.12 | 1.20 | 0.20 | t2 | |
| Ⅲ | 0.32 | 1.0 | 0 | 0 | |
| Ⅳ | 0.12 | 0.30 | v(正)=v(逆) |
| A. | 容器Ⅳ中c(D)=0.4 mol/L | |
| B. | t2时容器Ⅱ中v(正)>v(逆) | |
| C. | 容器Ⅰ中平均反应速率v(B)=$\frac{0.04}{{t}_{1}}$mol/(L•min) | |
| D. | 容器Ⅲ中反应至平衡时吸热20 kJ |
17.下列关于钠及其氧化物的叙述中正确的是( )
| A. | 钠着火后,可用泡沫灭火器来灭火 | |
| B. | 氧化钠和过氧化钠都属于碱性氧化物 | |
| C. | 过氧化钠与水的反应中,Na2O2作氧化剂,水作还原剂 | |
| D. | 用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应 |
16.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 32 g O2气体含有的氧原子数为NA | |
| B. | 2 L 0.3 mol/L Na2SO4溶液中含有Na+为0.6NA | |
| C. | 54 g铝完全反应后失去的电子数为6NA | |
| D. | 11.2 L氮气所含的分子数为0.5NA |
15.已知在相同条件下,下列几种微粒的还原性强弱顺序为Cl-<Br-<Fe2+<I-<SO2,由此判断下列反应不能发生的是( )
| A. | 2Fe3++SO2+2H2O═SO42-+4H++2Fe2+ | B. | 2Br-+SO42-+4H+═SO2+Br2+2H2O | ||
| C. | 2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | D. | 2Fe3++2I-═2Fe2++I2 |
14.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.5 mol Al与足量盐酸反应转移电子数为1NA | |
| B. | 500mL 1mol/LNa2CO3溶液中,含有Na+离子数目为NA | |
| C. | 常温常压下,11.2LO2(g)中含有O2分子数目为0.5NA | |
| D. | 标准状况下,11.2 L H2O所含的分子数为0.5 NA |
13.最近中国科学院上海高等研究院在合成气直接制烯烃研究获重大突破.已知:
反应①:C(s)+$\frac{1}{2}$O2(g)=CO (g)△H1
反应②:C(s)+H2O(g)=CO(g)+H2(g)△H2
反应③:CO(g)+2H2(g)=CH3OH(g)△H 3=-90.1kJ•mol-1
反应④:2CH3OH(g)=CH3OCH3(g)+H2O(g)△H 4=-134.0kJ•mol-1
反应⑤:3CH3OH(g)=CH3CH=CH2(g)+3H2O(g)△H 5=-31.0kJ•mol-1
下列说法正确的是( )
反应①:C(s)+$\frac{1}{2}$O2(g)=CO (g)△H1
反应②:C(s)+H2O(g)=CO(g)+H2(g)△H2
反应③:CO(g)+2H2(g)=CH3OH(g)△H 3=-90.1kJ•mol-1
反应④:2CH3OH(g)=CH3OCH3(g)+H2O(g)△H 4=-134.0kJ•mol-1
反应⑤:3CH3OH(g)=CH3CH=CH2(g)+3H2O(g)△H 5=-31.0kJ•mol-1
下列说法正确的是( )
| A. | △H1-△H2<0 | |
| B. | 反应②为放热反应 | |
| C. | 3CH3OCH3(g)=2CH3CH=CH2(g)+3H2O(g)△H=-103.0 kJ•mol-1 | |
| D. | 3CO(g)+6H2(g)=CH3CH=CH2(g)+3H2O(g)△H=-301.3kJ•mol-1 |
12.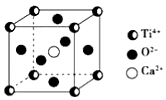 CaTiO3的晶体结构模型如图所示(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶角),下列关于晶体的说法正确的是( )
CaTiO3的晶体结构模型如图所示(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶角),下列关于晶体的说法正确的是( )
0 160109 160117 160123 160127 160133 160135 160139 160145 160147 160153 160159 160163 160165 160169 160175 160177 160183 160187 160189 160193 160195 160199 160201 160203 160204 160205 160207 160208 160209 160211 160213 160217 160219 160223 160225 160229 160235 160237 160243 160247 160249 160253 160259 160265 160267 160273 160277 160279 160285 160289 160295 160303 203614
 CaTiO3的晶体结构模型如图所示(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶角),下列关于晶体的说法正确的是( )
CaTiO3的晶体结构模型如图所示(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶角),下列关于晶体的说法正确的是( )| A. | CaTiO3的摩尔质量为136 | |
| B. | CaTiO3晶体中每个Ti4+与12个Ca2+紧相邻 | |
| C. | CaTiO3晶体中每个Ti4+与12个O2-紧相邻 | |
| D. | CaTiO3晶体中每个Ti4+与12个Ti4+紧相邻 |