17.下列溶液中溶质的物质的量浓度为1mol/L 的是( )
| A. | 称40.0 g 氢氧化钠固体解于1L水中配成1L的氢氧化钠溶液 | |
| B. | 常温常压下将22.4L氯化氢气体溶于水配成1L的盐酸溶液 | |
| C. | 将1L 10mol/L的浓盐酸与水混合配成10L溶液 | |
| D. | 从1000mL 2mol/L NaCl溶液中取出500mL的溶液 |
16.单晶硅是制作电子集成电路的基础材料,科学家预计,到2011年一个电脑芯片上将会集成10亿个晶体管,其功能远比我们想象的要大的多,这对硅的纯度要求很高.用化学方法可制得高纯度硅,其化学方程式为:
①2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑
②Si+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4
③SiCl4+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl
下列有关说法不正确的是( )
①2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑
②Si+2Cl2$\frac{\underline{\;高温\;}}{\;}$SiCl4
③SiCl4+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl
下列有关说法不正确的是( )
| A. | ②是化合反应 | B. | ①②③是氧化还原反应 | ||
| C. | ①③是置换反应 | D. | ①③是复分解反应 |
15.下列各项中括号里的物质是除去杂质所用的药品,其中错误的是( )
| A. | SO2中有少量HCl气体(氢氧化钠溶液) | B. | CO中混有CO2(石灰水、浓硫酸) | ||
| C. | CO2中有少量CO(灼热氧化铜) | D. | Cl2中混有HCl(饱和食盐水、浓硫酸) |
14.能使湿润的淀粉KI试纸变蓝的是( )
①氯水 ②溴水 ③碘水 ④氯化钠 ⑤溴化钾.
①氯水 ②溴水 ③碘水 ④氯化钠 ⑤溴化钾.
| A. | ①② | B. | ①②③ | C. | ①②④ | D. | ①③⑤ |
13.在可逆反应2NO2(g)?N2O4(g)中,下列可说明反应已达到平衡状态的是( )
| A. | NO2和N2O4浓度相等 | B. | NO2和N2O4分子数之比为2:1 | ||
| C. | 体系颜色不再发生变化 | D. | N2O4不再分解 |
11.在相同条件下,下列各组物质中,分子数最多的是( )
| A. | 14g N2 | B. | 4g H2 | ||
| C. | 标准状况下11.2L CO2 | D. | 0.5mol O2 |
10.下列物质发生变化时,所克服的粒子间相互作用属于分子间作用力的是( )
0 160100 160108 160114 160118 160124 160126 160130 160136 160138 160144 160150 160154 160156 160160 160166 160168 160174 160178 160180 160184 160186 160190 160192 160194 160195 160196 160198 160199 160200 160202 160204 160208 160210 160214 160216 160220 160226 160228 160234 160238 160240 160244 160250 160256 160258 160264 160268 160270 160276 160280 160286 160294 203614
| A. | 酒精受热变为气体 | B. | 氯化铵受热变为气体 | ||
| C. | 二氧化硅受热熔化 | D. | 食盐溶解在水中 |
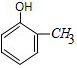 2-甲基苯酚、
2-甲基苯酚、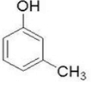 3-甲基苯酚、
3-甲基苯酚、 4-甲基苯酚.
4-甲基苯酚.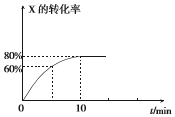 恒定温度为T1℃时,在容积为10L的密闭容器中充人1.0mol X和0.80mol Y,发生反应:
恒定温度为T1℃时,在容积为10L的密闭容器中充人1.0mol X和0.80mol Y,发生反应: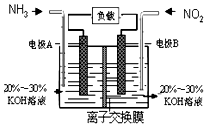 空气质量与我们的健康息息相关,目我国通过检测6项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2、和CO是其中3项中的污染物.
空气质量与我们的健康息息相关,目我国通过检测6项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2、和CO是其中3项中的污染物.