5.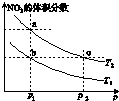 在密闭容器中充入一定量的NO2,发生反应2NO2(g)?N2O4(g)△H=-57kJ•mol-1.在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示.下列说法正确的是( )
在密闭容器中充入一定量的NO2,发生反应2NO2(g)?N2O4(g)△H=-57kJ•mol-1.在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示.下列说法正确的是( )
 在密闭容器中充入一定量的NO2,发生反应2NO2(g)?N2O4(g)△H=-57kJ•mol-1.在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示.下列说法正确的是( )
在密闭容器中充入一定量的NO2,发生反应2NO2(g)?N2O4(g)△H=-57kJ•mol-1.在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示.下列说法正确的是( )| A. | a、c两点的反应速率:a>c | B. | 由a点到b点,可以用加热的方法 | ||
| C. | a、c两点气体的颜色:a深,c浅 | D. | a、b两点NO2的转化率:a<b |
3.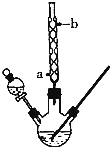 某化学课外小组设计了如图所示的装置制取乙酸乙酯(图中夹持仪器和加热装置已略去).请回答下列问题:
某化学课外小组设计了如图所示的装置制取乙酸乙酯(图中夹持仪器和加热装置已略去).请回答下列问题:
(1)该实验中,将乙醇、乙酸和浓硫酸加入三颈烧瓶中时,最先加入的液体不能是浓硫酸.
(2)水从冷凝管的a(填“a”或“b”)处进入.
(3)已知下列数据:
又知温度高于140℃时发生副反应:2CH3CH2OH→CH3CH2OCH2CH3+H2O.
①该副反应属于b反应(填字母).
a.加成 b.取代 c.酯化
②考虑到反应速率等多种因素,用上述装置制备乙酸乙酯时,反应的最佳温度范围是c(填字母).
a.T<77.5℃b.T>150℃c.115℃<T<130℃
(4)将反应后的混合液缓缓倒入盛有足量饱和碳酸钠溶液的烧杯中,搅拌、静置.饱和碳酸钠溶液的作用是中和乙酸、溶解乙醇,降低乙酸乙酯的溶解度,便于分层欲分离出乙酸乙酯,应使用的分离方法是分液(填操作方法名称,下同),所用到的仪器为分液漏斗,乙酸乙酯从该仪器的上端(上端或下端)流出.进行此步操作后,所得有机层中的主要无机物杂质是水,在不允许使用干燥剂的条件下,除去水可用蒸馏的方法.
(5)若实验所用乙酸质量为6.0g,乙醇质量为5.0g,得到纯净的产品质量为4.4g,则乙酸乙酯的产率是50%.
 某化学课外小组设计了如图所示的装置制取乙酸乙酯(图中夹持仪器和加热装置已略去).请回答下列问题:
某化学课外小组设计了如图所示的装置制取乙酸乙酯(图中夹持仪器和加热装置已略去).请回答下列问题:(1)该实验中,将乙醇、乙酸和浓硫酸加入三颈烧瓶中时,最先加入的液体不能是浓硫酸.
(2)水从冷凝管的a(填“a”或“b”)处进入.
(3)已知下列数据:
| 乙醇 | 乙酸 | 乙酸乙酯 | 98%浓硫酸 | |
| 熔点/℃ | -117.3 | 16.6 | -83.6 | - |
| 沸点/℃ | 78.5 | 117.9 | 77.5 | 338.0 |
①该副反应属于b反应(填字母).
a.加成 b.取代 c.酯化
②考虑到反应速率等多种因素,用上述装置制备乙酸乙酯时,反应的最佳温度范围是c(填字母).
a.T<77.5℃b.T>150℃c.115℃<T<130℃
(4)将反应后的混合液缓缓倒入盛有足量饱和碳酸钠溶液的烧杯中,搅拌、静置.饱和碳酸钠溶液的作用是中和乙酸、溶解乙醇,降低乙酸乙酯的溶解度,便于分层欲分离出乙酸乙酯,应使用的分离方法是分液(填操作方法名称,下同),所用到的仪器为分液漏斗,乙酸乙酯从该仪器的上端(上端或下端)流出.进行此步操作后,所得有机层中的主要无机物杂质是水,在不允许使用干燥剂的条件下,除去水可用蒸馏的方法.
(5)若实验所用乙酸质量为6.0g,乙醇质量为5.0g,得到纯净的产品质量为4.4g,则乙酸乙酯的产率是50%.
1.金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝.高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:WO3(s)+3H2(g)$\stackrel{高温}{?}$W(s)+3H2O(g)
(1)上述反应的化学平衡常数表达式为K=$\frac{{c}^{3}({H}_{2}O)}{{c}^{3}({H}_{2})}$.
(2)某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为60%
(3)上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
第一阶段反应的化学方程式为2WO3+H2$\frac{\underline{\;高温\;}}{\;}$W2O5+H2O;假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为1:1:4.
(4)已知:温度过高时,WO2(s)转变为WO2(g):
WO2(s)+2H2(g)?W(s)+2H2O (g)△H=+66.0kJ?mol-1
WO2(g)+2H2(g)?W(s)+2H2O (g)△H=-137.9kJ?mol-1
则WO2(s)?WO2(g),则WO2(s)?WO2 (g) 的△H=+203.9 kJ•mol-1.
(1)上述反应的化学平衡常数表达式为K=$\frac{{c}^{3}({H}_{2}O)}{{c}^{3}({H}_{2})}$.
(2)某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为60%
(3)上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
| 温度 | 25℃~550℃~600℃~700℃ |
| 主要成分 | WO3 W2O5 WO2 W |
(4)已知:温度过高时,WO2(s)转变为WO2(g):
WO2(s)+2H2(g)?W(s)+2H2O (g)△H=+66.0kJ?mol-1
WO2(g)+2H2(g)?W(s)+2H2O (g)△H=-137.9kJ?mol-1
则WO2(s)?WO2(g),则WO2(s)?WO2 (g) 的△H=+203.9 kJ•mol-1.
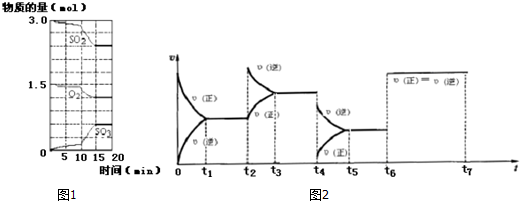
19.煤化工中常需研究不同温度下平衡常数、投料比及热值等问题.
已知:CO(g)+H2O(g)?H2(g)+CO2(g)的平衡常数随温度的变化如表:
试回答下列问题
(1)某温度下,上述反应达到平衡后,保持容器体积不变降低温度,平衡正向移动(填“正向移动”、“逆向移动”或“不移动”).
(2)在恒容绝热容器中,下列描述中能说明上述反应已达到平衡的是C
A、容器内混合气体分子总数不再发生变化
B、容器内混合气体的密度不再变化
C、$\frac{c(C{O}_{2})•c({H}_{2})}{c(CO)•c({H}_{2}O)}$不再变化
D、单位时间内消耗18g H2O同时生成1mol CO2
(3)830℃时,在恒容密闭容器中发生上述反应,按表中的物质的量投入反应混合物,其中向正反应方向进行的有AD(选填字母序号).
(4)830℃时,在2L的密闭容器中加入4mol CO(g)和4mol H2O(g),2min达到平衡时,CO的转化率为50%,用CO表示的平均反应速率为0.5mol/(L•min).
0 160085 160093 160099 160103 160109 160111 160115 160121 160123 160129 160135 160139 160141 160145 160151 160153 160159 160163 160165 160169 160171 160175 160177 160179 160180 160181 160183 160184 160185 160187 160189 160193 160195 160199 160201 160205 160211 160213 160219 160223 160225 160229 160235 160241 160243 160249 160253 160255 160261 160265 160271 160279 203614
已知:CO(g)+H2O(g)?H2(g)+CO2(g)的平衡常数随温度的变化如表:
| 温度℃ | 400 | 500 | 830 | 1 000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
(1)某温度下,上述反应达到平衡后,保持容器体积不变降低温度,平衡正向移动(填“正向移动”、“逆向移动”或“不移动”).
(2)在恒容绝热容器中,下列描述中能说明上述反应已达到平衡的是C
A、容器内混合气体分子总数不再发生变化
B、容器内混合气体的密度不再变化
C、$\frac{c(C{O}_{2})•c({H}_{2})}{c(CO)•c({H}_{2}O)}$不再变化
D、单位时间内消耗18g H2O同时生成1mol CO2
(3)830℃时,在恒容密闭容器中发生上述反应,按表中的物质的量投入反应混合物,其中向正反应方向进行的有AD(选填字母序号).
| A | B | C | D | |
| n(CO2)/mol | 0 | 1 | 3 | 1 |
| n(H2)/mol | 0 | 2 | 2 | 1 |
| n(CO)/mol | 3 | 0.5 | 1 | 2 |
| n(H2O)/mol | 3 | 2 | 5 | 2 |
 碱式碳酸铜是一种化工原料,化学式用mCu(OH)2•nCuCO3表示.实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
碱式碳酸铜是一种化工原料,化学式用mCu(OH)2•nCuCO3表示.实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
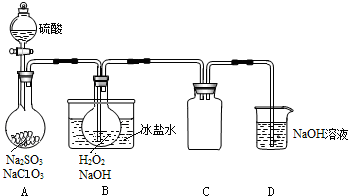
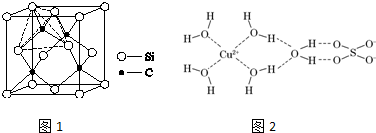
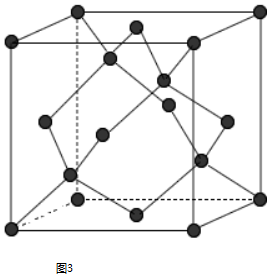
 ;亚铜离子(Cu+)基态时的电子排布式为1s22s22p63s23p63d10或[Ar]3d10.
;亚铜离子(Cu+)基态时的电子排布式为1s22s22p63s23p63d10或[Ar]3d10.