6.某化学小组欲探究铁及其化合物的氧化性和还原性,请回答下列问题:
(1)请帮他们完成以下实验报告:
实验目的:探究铁及其化合物的氧化性和还原性.
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片.
实验记录:
实验结论:Fe只有还原性,Fe3+只有氧化性,Fe2+既有氧化性,又有还原性.
(2)根据以上结论判断,下列物质中既有氧化性,又有还原性的有:AEF.(填序号)
A.Cl2 B.Na C.Na+ D.Cl- E.SO2 F.NO2
(3)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液.那么保存亚铁盐溶液时可以在溶液中加入少量铁粉以防止亚铁盐被氧化.
(4)检验亚铁盐溶液是否被氧化的操作步骤和现象是取少许亚铁盐溶液于试管中,滴加几滴KSCN溶液,如果溶液变红则说明亚铁盐被氧化.
(5)向FeCl2溶液滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为生成白色沉淀,迅速变成灰绿色,最终变成红褐色,此过程中发生的氧化还原反应的化学方程式4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(1)请帮他们完成以下实验报告:
实验目的:探究铁及其化合物的氧化性和还原性.
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片.
实验记录:
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为棕黄色 | Fe2+具有还原性 | |
| ② | 在FeCl2溶液中加入锌片 | (不写) | Zn+Fe2+═Zn2++Fe | |
| ③ | 在FeCl3溶液中加入足量铁粉 | Fe+2Fe3+═3Fe2+ | Fe3+具有氧化性 | |
| ④ | (不写) | Fe3+具有氧化性 |
(2)根据以上结论判断,下列物质中既有氧化性,又有还原性的有:AEF.(填序号)
A.Cl2 B.Na C.Na+ D.Cl- E.SO2 F.NO2
(3)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液.那么保存亚铁盐溶液时可以在溶液中加入少量铁粉以防止亚铁盐被氧化.
(4)检验亚铁盐溶液是否被氧化的操作步骤和现象是取少许亚铁盐溶液于试管中,滴加几滴KSCN溶液,如果溶液变红则说明亚铁盐被氧化.
(5)向FeCl2溶液滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为生成白色沉淀,迅速变成灰绿色,最终变成红褐色,此过程中发生的氧化还原反应的化学方程式4Fe(OH)2+O2+2H2O=4Fe(OH)3.
17.含有极性键且分子中各原子都满足8电子稳定结构的化合物是( )
| A. | CH4 | B. | CH2═CH2 | C. | CO2 | D. | N2 |
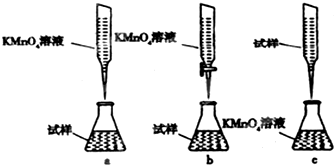
16.下列有关实验操作分析正确的是( )
0 160083 160091 160097 160101 160107 160109 160113 160119 160121 160127 160133 160137 160139 160143 160149 160151 160157 160161 160163 160167 160169 160173 160175 160177 160178 160179 160181 160182 160183 160185 160187 160191 160193 160197 160199 160203 160209 160211 160217 160221 160223 160227 160233 160239 160241 160247 160251 160253 160259 160263 160269 160277 203614
| A. | 从溴水中萃取溴,可用酒精做萃取剂 | |
| B. | 蒸发实验完毕后,发现蒸发皿炸裂,这是因为没有垫石棉网 | |
| C. | 萃取碘水溶液中碘,分离碘四氯化碳溶液时,眼睛注视分液漏斗里液面 | |
| D. | 蒸馏时,为了加快水的流速,水应从上口进入,下口流出 |

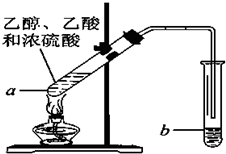 乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平.请回答下列问题.
乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平.请回答下列问题. ,结构简式H2C=CH2.
,结构简式H2C=CH2. ,反应类型是加聚反应.
,反应类型是加聚反应.