4.为了证明甲酸中含有乙醛,应采用的方法是( )
| A. | 加入银氨溶液,并水浴加热 | |
| B. | 加入2~3滴石蕊试液 | |
| C. | 先加入浓NaOH溶液,加热蒸馏,把蒸馏出的物质加银氨溶液并水浴加热 | |
| D. | 直接蒸馏,把蒸馏出的物质加NaOH溶液调至碱性,再加银氨溶液,并水浴加热 |
3.下列说法正确的是( )
| A. | 减小反应物浓度,可减小单位体积内活化分子的百分数,从而使有效碰撞次数减少 | |
| B. | 对于有气体参加的化学反应,若减小压强(即扩大反应容器的体积),可减小活化分子的百分数,从而使反应速率减小 | |
| C. | 改变条件能使化学反应速率增大的主要原因是增大了反应物分子中活化分子的有效碰撞几率 | |
| D. | 能量高的分子一定能发生有效碰撞 |
2.根据如图提供的信息,下列所得结论不正确的是( )
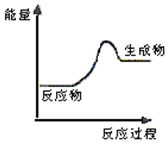

| A. | 该反应可能为吸热反应 | |
| B. | 该反应一定有能量转化成了生成物的化学能 | |
| C. | 反应物比生成物稳定 | |
| D. | 生成物的总能量高于反应物的总能量,反应不需要加热 |
1.配置250mL0.5mol/L的NaCl溶液,有下列仪器:①托盘天平、②量筒、③烧杯、④玻璃棒、⑤漏斗、⑥500mL容量瓶、⑦药匙、⑧250mL容量瓶、⑨胶头滴管、⑩坩埚,需要用到的仪器有( )
| A. | ①③④⑦⑧⑨ | B. | ①④⑦⑧⑨⑩ | C. | ①③④⑥⑨⑩ | D. | ①②④⑤⑧⑨ |
20.设NA为阿伏加德罗常数值.下列有关叙述正确的是( )
| A. | 1molN2与4molH2反应生成的NH3分子数为2NA | |
| B. | 14g乙烯和丙烯混合气体中的氢原子数为2NA | |
| C. | 1 molFe溶于过量硝酸,电子转移数为2NA | |
| D. | 标准状况下,2.24LCCl4含有的共价键数为0.4NA |
19.人们常将在同一原子轨道上运动的、自旋状态相反的2个电子,称为“电子对”;在同一原子轨道上运动的单个电子,称为“未成对电子”.以下有关主族元素原子的“未成对电子”的说法,错误的是( )
| A. | 第四周期元素的基态原子中,Cr元素的未成对电子数最多 | |
| B. | 第三周期元素中3p原子轨道有一个未成对电子的原子有2种 | |
| C. | 核外电子数为偶数的基态原子,其原子轨道中可能含有“未成对电子” | |
| D. | 基态碳原子无未成对电子 |
18.下列说法或表示方法正确的是( )
| A. | 等质量的硫蒸气和硫固体分别在氧气中完全燃烧,后者放出的热量少 | |
| B. | 1molH2在足量氯气中完全燃烧所放出的热量,是H2的燃烧热 | |
| C. | 盐酸与NaOH溶液反应的中和热△H=-57.3kJ•mol-1,则硫酸和Ca(OH)2溶液反应的中和热△H=-2×57.3kJ•mol-1 | |
| D. | 一定条件下,0.1molN2(g)与0.3molH2(g)混合充分反应时放出的热量为8kJ,则有N2(g)+3H2(g)?2NH3(g)△H=-80kJ•mol-1 |
16.下列有关实验的选项正确的是( )
| A. |  配制0.10mol/L NaOH溶液 | |
| B. |  除去CO中的CO2 | |
| C. |  苯萃取碘水中的I2分出水层后的操作 | |
| D. |  除去粗盐溶液中的不溶物 |
15.某兴趣小组甲设计了以下装置和方法测定空气中SO2含量.你认为可行的操作是B
0 160081 160089 160095 160099 160105 160107 160111 160117 160119 160125 160131 160135 160137 160141 160147 160149 160155 160159 160161 160165 160167 160171 160173 160175 160176 160177 160179 160180 160181 160183 160185 160189 160191 160195 160197 160201 160207 160209 160215 160219 160221 160225 160231 160237 160239 160245 160249 160251 160257 160261 160267 160275 203614
| 序号 | A | B | C |
| 装置 | 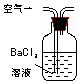 | 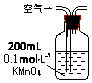 | 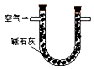 |
| 原理 | 通入V升空气,测定生成沉淀的质量 | 当KMnO4溶液刚好褪色时,测定通入空气的体积V | 通入V升空气,测定U型管增加的质量 |
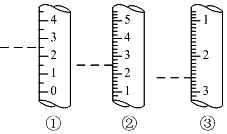 托盘天平、容量瓶、量筒是常见的中学化学计量仪器,熟知这些仪器的使用是定量研究化学的基础.
托盘天平、容量瓶、量筒是常见的中学化学计量仪器,熟知这些仪器的使用是定量研究化学的基础.