14.同温同压下,下列各组热化学方程式中,△H1<△H2的是( )
| A. | C(s)+$\frac{1}{2}$O2(g)=CO(g);△H1 C(s)+O2(g)=CO2(g);△H2 | |
| B. | $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)=HCl(g);△H1 H2(g)+Cl2(g)=2HCl(g);△H2 | |
| C. | S(g)+O2(g)=SO2(g);△H1 S(s)+O2(g)=SO2(g);△H2 | |
| D. | 2H2(g)+O2(g)=2H2O(g);△H1 2H2(g)+O2(g)=2H2O(l);△H2 |
13.下列说法正确的是( )
| A. | 一定温度下,反应MgCl2(l)=Mg(l)+Cl2(g)的△H>0、△S>0 | |
| B. | 水解反应NH4++H2O?NH3•H2O+H+达到平衡后,升高温度平衡逆向移动 | |
| C. | AlCl3溶液蒸干、灼烧至恒重,最终剩余固体是AlCl3 | |
| D. | 对于反应2H2O2=2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率 |
12.下列有关说法正确的是( )
| A. | 已知:HI(g)═$\frac{1}{2}$H2(g)+$\frac{1}{2}$I2(s)△H=-26.5kJ/mol,由此可知1mol HI气体在密闭容器中充分分解后可以放出26.5kJ的热量 | |
| B. | 已知:2H2(g)+O2(g)=2H2O(l)△H=-571.6 kJ/mol,则氢气的燃烧热为△H=-285.8 kJ/mol | |
| C. | 肼(N2H4)是一种用于火箭或燃料电池的原料,已知2H2O(g)+O2(g)=2H2O2(l)△H=+108.3kJ/mol ①N2H4(l)+O2(g)=N2(g)+2H2O(g)△H=-534.0kJ/mol ②则有反应:N2H4(l)+2 H2O2(l)=N2(g)+4H2O(l)△H=-642.3kJ/mol | |
| D. | 含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l)△H=-57.4 kJ/mol |
11.在某一容积为2L的密闭容器内,加入0.2mol的CO和 0.2mol的 H2O(g),在催化剂存在的条件下恒温下发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g);△H=a kJ/mol(a>0).反应达到平衡后,测得c(CO):c(CO2)=3:2.下列说法正确的是( )
| A. | 当体系压强不变时反应一定达到平衡 | |
| B. | 反应放出的热量为 0.2a kJ | |
| C. | 若升高温度,v(正)加快,v(逆)减慢,平衡正向移动 | |
| D. | 在相同条件下再加入0.2mol的CO和0.2mol的 H2O(g),重新达平衡时,c(CO):c(CO2)=3:2 |
10.常温下Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.0×10-16,将等体积的AgCl和AgI的饱和溶液的清液混合,再向其中加入一定量的AgNO3固体,下列说法正确的是( )
| A. | 两溶液混合,AgCl和AgI都沉淀 | |
| B. | 若AgNO3足量,AgCl和AgI都可沉淀,但以AgCl为主 | |
| C. | 向AgI的饱和溶液中加AgNO3,c(Ag+)增大,Ksp(AgI)也增大 | |
| D. | 若取0.1435克AgCl固体配成100mL溶液,c(Cl-)为0.01mol/L |
9.已知:2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1
2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1 452kJ•mol-1
H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1下列说法正确的是( )
2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1 452kJ•mol-1
H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1下列说法正确的是( )
| A. | H2(g)的燃烧热为571.6 kJ•mol-1 | |
| B. | $\frac{1}{2}$H2SO4(aq)+$\frac{1}{2}$Ba(OH)2(aq)═$\frac{1}{2}$BaSO4(s)+H2O(l)△H=-57.3 kJ•mol-1 | |
| C. | 同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 | |
| D. | 3H2(g)+CO2(g)═CH3OH(l)+H2O(l)△H=-131.4 kJ•mol-1 |
8.已知:a.C2H2(g)+H2(g)=C2H4(g)△H<0 b.2CH4(g)=C2H4(g)+2H2(g)△H>0
判断以下3个热化学方程式:①C(s)+2H2(g)=CH4(g)△H1
②C(s)+$\frac{1}{2}$H2(g)=$\frac{1}{2}$C2H2(g)△H2③C(s)+H2(g)=$\frac{1}{2}$C2H4(g)△H3
△H1、△H2、△H3由大到小的顺序是( )
判断以下3个热化学方程式:①C(s)+2H2(g)=CH4(g)△H1
②C(s)+$\frac{1}{2}$H2(g)=$\frac{1}{2}$C2H2(g)△H2③C(s)+H2(g)=$\frac{1}{2}$C2H4(g)△H3
△H1、△H2、△H3由大到小的顺序是( )
| A. | △H2>△H3>△H1 | B. | △H3>△H2>△H1 | C. | △H3>△H1>△H2 | D. | △H1>△H2>△H3 |
7.在一个盛有催化剂容积可变的密闭容器中,保持一定的温度和压强,进行以下反应:N2+3H2?2NH3.已知加入1molN2和4molH2时,达到平衡后生成amolNH3.有恒温恒压下欲保持平衡时各组分的体积分数不变.填表(恒温恒压)
| 已知 编号 | 起始状态物质的量/mol | 平衡时NH3的 物质的量/mol | ||
| N2 | H2 | NH3 | ||
| 1 | 4 | 0 | a | |
| ① | 1.5 | 9 | 0 | >1.5a |
| ② | 0 | 0.5 | 1 | 0.5a |
| ③ | m | g(g≥4m) | 0 | am或者$\frac{ag}{4}$ |
5. 常温常压下,甲、乙两容器带有相同质量的活塞且容积相等,甲容器中盛有二氧化氮气体,乙容器中盛有空气,现分别进行下列两实验:(已知:N2O4(g)?2NO2(g)△H>0)
常温常压下,甲、乙两容器带有相同质量的活塞且容积相等,甲容器中盛有二氧化氮气体,乙容器中盛有空气,现分别进行下列两实验:(已知:N2O4(g)?2NO2(g)△H>0)
(a)将两容器置于沸水中加热
(b)在活塞上都加2kg的砝码
在以上两情况下,甲和乙容器的体积大小的比较,正确的是( )
0 160068 160076 160082 160086 160092 160094 160098 160104 160106 160112 160118 160122 160124 160128 160134 160136 160142 160146 160148 160152 160154 160158 160160 160162 160163 160164 160166 160167 160168 160170 160172 160176 160178 160182 160184 160188 160194 160196 160202 160206 160208 160212 160218 160224 160226 160232 160236 160238 160244 160248 160254 160262 203614
 常温常压下,甲、乙两容器带有相同质量的活塞且容积相等,甲容器中盛有二氧化氮气体,乙容器中盛有空气,现分别进行下列两实验:(已知:N2O4(g)?2NO2(g)△H>0)
常温常压下,甲、乙两容器带有相同质量的活塞且容积相等,甲容器中盛有二氧化氮气体,乙容器中盛有空气,现分别进行下列两实验:(已知:N2O4(g)?2NO2(g)△H>0)(a)将两容器置于沸水中加热
(b)在活塞上都加2kg的砝码
在以上两情况下,甲和乙容器的体积大小的比较,正确的是( )
| A. | (a)甲>乙,(b)甲>乙 | B. | (a)甲>乙,(b)甲=乙 | C. | (a)甲<乙,(b)甲>乙 | D. | (a)甲>乙,(b)甲<乙 |
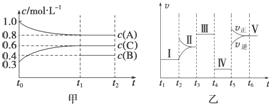 向某密闭容器中加入 4mol A、1.2mol C 和一定量的 B 三种气体,一定条件 下发生反应,各物质的浓度随时间变化如甲图所示[已知 t0~t1 阶段保持恒温、恒容,且 c(B)未画出].乙图为 t2 时刻后改变反应条件,反应速率随时间的变化情况,已知 在 t2、t3、t4、t5 时刻各改变一种不同的条件,其中 t3 时刻为使用催化剂.
向某密闭容器中加入 4mol A、1.2mol C 和一定量的 B 三种气体,一定条件 下发生反应,各物质的浓度随时间变化如甲图所示[已知 t0~t1 阶段保持恒温、恒容,且 c(B)未画出].乙图为 t2 时刻后改变反应条件,反应速率随时间的变化情况,已知 在 t2、t3、t4、t5 时刻各改变一种不同的条件,其中 t3 时刻为使用催化剂.