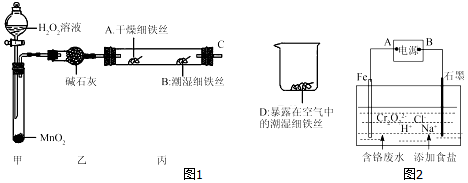
16.下列叙述正确的是( )
| A. | 硫离子的结构示意图为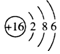 | |
| B. | 核外电子排布相同的微粒化学性质也相同 | |
| C. | 氢弹中用到的2H、3H互为同位素 | |
| D. | 同种元素的原子均有相同的质子数和中子数 |
15.化学与社会、生产、生活密切相关.下列说法不正确的是( )
| A. | 高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路” | |
| B. | 我国油品从国IV汽油升级到国V汽油,有助于减少酸雨、雾霾,提高空气质量 | |
| C. | 臭氧是氧化性极强的淡蓝色气体,可用作自来水的消毒剂 | |
| D. | 科学家发现一种新细菌的DNA链中有砷(As)元素,该As元素最有可能取代普通DNA链中的P元素 |
7.氨对地球上的生物相当重要,它是许多食物和肥料的重要成分.氨也是制造硝酸、化肥、炸药 的重要原料.氨在国民经济中占有重要地位.回答下列问题:
(1)合成氨工业中,合成塔中每产生2mol NH3,放出92.2kJ热量.
①工业合成氨的热化学方程式是N2(g)+3H2(g)=2NH3(g)△H=-92.2kJ/mol.
②若起始时向容器内放入1mol N2和3mol H2,达平衡后N2的转化率为20%,则反应放出的热量为Q1 kJ,则Q1的数值为18.44;若在同体积的容器中充人2mol N2和6molH2,达平衡后放出的热量为Q2 kJ,则Q2>(填“>”、“<”或“=”)2Q1.
③已知:

1mol N-H键断裂吸收的能量约等于391kJ.
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行合成氨反应:N2 (g)+3H2(g)?2NH3 (g),其平衡常数K与温度T的关系如表:
①平衡常数表达式K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$,K1>(填“>”、“<”或“一”)K2.
②一定温度下,下列各项能作为判断该反应达到化学平衡状态的依据是bc(填字母).
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.浓度商Q=平衡常数K
c.容器内压强保持不变
d.混合气体的密度保持不变
③在400℃时,当测得N2、H2和NH3的物质的量分别为2mol、1mol、2mol时,则此时该反应处于(填“处于”或“不处于”)平衡状态.
0 160040 160048 160054 160058 160064 160066 160070 160076 160078 160084 160090 160094 160096 160100 160106 160108 160114 160118 160120 160124 160126 160130 160132 160134 160135 160136 160138 160139 160140 160142 160144 160148 160150 160154 160156 160160 160166 160168 160174 160178 160180 160184 160190 160196 160198 160204 160208 160210 160216 160220 160226 160234 203614
(1)合成氨工业中,合成塔中每产生2mol NH3,放出92.2kJ热量.
①工业合成氨的热化学方程式是N2(g)+3H2(g)=2NH3(g)△H=-92.2kJ/mol.
②若起始时向容器内放入1mol N2和3mol H2,达平衡后N2的转化率为20%,则反应放出的热量为Q1 kJ,则Q1的数值为18.44;若在同体积的容器中充人2mol N2和6molH2,达平衡后放出的热量为Q2 kJ,则Q2>(填“>”、“<”或“=”)2Q1.
③已知:

1mol N-H键断裂吸收的能量约等于391kJ.
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行合成氨反应:N2 (g)+3H2(g)?2NH3 (g),其平衡常数K与温度T的关系如表:
| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
②一定温度下,下列各项能作为判断该反应达到化学平衡状态的依据是bc(填字母).
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.浓度商Q=平衡常数K
c.容器内压强保持不变
d.混合气体的密度保持不变
③在400℃时,当测得N2、H2和NH3的物质的量分别为2mol、1mol、2mol时,则此时该反应处于(填“处于”或“不处于”)平衡状态.
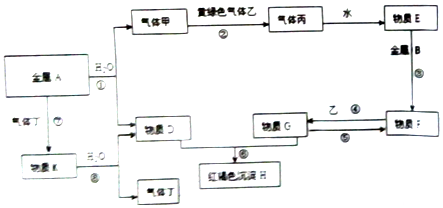
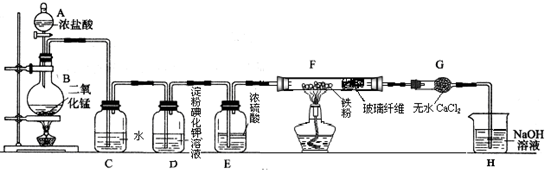
 实验室需要0.1mol•L-1NaOH溶液500mL,根据溶液的配制情况,回答下列问题:
实验室需要0.1mol•L-1NaOH溶液500mL,根据溶液的配制情况,回答下列问题: