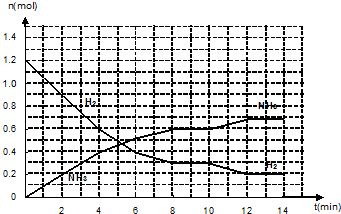
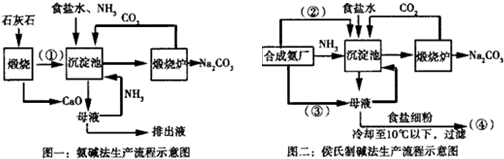
5.一定温度下,在2L的密闭容器中发生如下反应:A(s)+2B(g)?xC(g)△H<0,B、C的物质的量随时间变化的关系如图一,达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如图二.
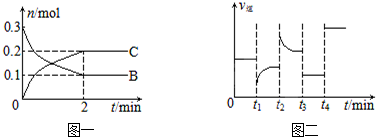
下列有关说法正确的是( )

下列有关说法正确的是( )
| A. | t2时改变的条件可能是增大c(C),平衡时B的物质的量分数增大 | |
| B. | t1时改变的条件是降温,平衡逆向移动 | |
| C. | t3时可能是减小压强,平衡不移动;t4时可能是使用催化剂,c(B)不变 | |
| D. | x=2,反应开始2 min内,v(B)=0.1 mol/(L•min) |
4.已知:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1
现有温度、容积相同的4个密闭容器,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如表:
则下列说法中正确的是ACD.
A.2c2<c3 2y>z B. p1=p2 x=y
C.(a1+a3)<1 D.若x=24.5kJ,则w=14.7kJ.
现有温度、容积相同的4个密闭容器,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如表:
| 容器 | 1 | 2 | 3 | 4 |
| 反应物投入量 (始态) | 1mol CO2 3mol H2 | 1mol CH3OH 1mol H2O | 2mol CH3OH 2mol H2O | 0.8mol CO2 2.4mol H2 0.2mol CH3OH 0.2mol H2O |
| CH3OH的平衡浓度/mol•L-1 | c1 | c2 | c3 | c4 |
| 反应的能量变化 | 放出 x kJ | 吸收y kJ | 吸收z kJ | 放出 w kJ |
| 体系压强/Pa | p1 | p2 | p3 | p4 |
| 反应物转化率 | a1 | a2 | a3 | a4 |
A.2c2<c3 2y>z B. p1=p2 x=y
C.(a1+a3)<1 D.若x=24.5kJ,则w=14.7kJ.
20.(1)用O2将HC1转化为Cl2,可提高效益,减少污染,传统上该转化通过如图所示的催化剂循环实现,

其中,反应①为:2HCl(g)+CuO(s)?H2O(g)+CuCl2(s)△H1,反应②生成1mol Cl2 (g)的反应热为△H2,则总反应的热化学方程式为2HCl(g)+$\frac{1}{2}$O2(g)$\frac{\underline{\;\;△\;\;}}{\;}$H2O(g)+Cl2(g)△H=△H1+△H2.(反应热用△H1和△H2表示).
(2)一定条件下测得上述反应过程中c(Cl2)的数据如下:
计算2.0~6.0min内以HCl的物质的量浓度变化表示的反应速率1.8×10-3mol/(L•min).
(3)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生.
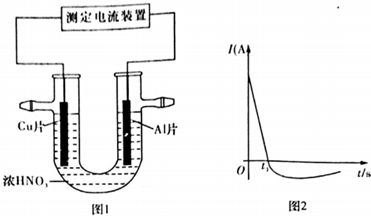
0~tl时,原电池的负极是Al片,此时,正极的电极反应式是2H++NO3-+e-=NO2↑+H2O,溶液中的H+向正极移动,tl时,原电池中电子流动方向发生改变,其原因是铝钝化后,铜成为负极.

其中,反应①为:2HCl(g)+CuO(s)?H2O(g)+CuCl2(s)△H1,反应②生成1mol Cl2 (g)的反应热为△H2,则总反应的热化学方程式为2HCl(g)+$\frac{1}{2}$O2(g)$\frac{\underline{\;\;△\;\;}}{\;}$H2O(g)+Cl2(g)△H=△H1+△H2.(反应热用△H1和△H2表示).
(2)一定条件下测得上述反应过程中c(Cl2)的数据如下:
| t(min) | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
| N(Cl2)/10-3(mol/L) | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
(3)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生.

0~tl时,原电池的负极是Al片,此时,正极的电极反应式是2H++NO3-+e-=NO2↑+H2O,溶液中的H+向正极移动,tl时,原电池中电子流动方向发生改变,其原因是铝钝化后,铜成为负极.
19.用化学反应原理研究NH3的性质具有重要意义.请回答下列问题:
(1)已知:①4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H=-1266.8kJ•mol-1
②N2(g)+O2(g)=2NO(g)△H=+180.5kJ•mol-1
写出氨高温催化氧化的热化学方程式4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=-905.8kJ•mol-1.
(2)氨气、空气可以构成燃料电池,则原电解质溶液显碱性(填“酸性”、“中性”或“碱性”),
负极的电极反应式为2NH3+6OH--6e-═N2+6H2O.
(3)在0.5L的密闭容器中,一定量的N2和H2发生反应:N2(g)+3H2(g)?2NH3(g)△H=akJ/mol,其化学平衡常数K与温度的关系如下:
①由上表数据可知a<0 (填“>”、“<”或“=”).
②理论上,为了增大平衡时H2的转化率,可采取的措施是ad(填字母序号).
a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物中的NH3
③400oC时,测得某时刻氨气、氮气、氢气的物质的量分别为3mol、2mol、1mol,此时刻该反应的v正(N2)<v逆(N2)(填“>”、“<”或“=”).
(4)25oC时,将amol•L-1的氨水与0.1mol•L-1的盐酸等体积混合
①当溶液中离子浓度关系满足c(NH4+)>c(Cl-)时,反应的情况可能为a(填字母序号).
a.盐酸不足,氨水剩余 b.氨水与盐酸恰好完全反应 c.盐酸过量
②当溶液中c(NH4+)=c(Cl-)时,用含a的代数式表示NH3•H2O的电离常数Kb=$\frac{1{0}^{-8}}{a-0.1}$.
(1)已知:①4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H=-1266.8kJ•mol-1
②N2(g)+O2(g)=2NO(g)△H=+180.5kJ•mol-1
写出氨高温催化氧化的热化学方程式4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=-905.8kJ•mol-1.
(2)氨气、空气可以构成燃料电池,则原电解质溶液显碱性(填“酸性”、“中性”或“碱性”),
负极的电极反应式为2NH3+6OH--6e-═N2+6H2O.
(3)在0.5L的密闭容器中,一定量的N2和H2发生反应:N2(g)+3H2(g)?2NH3(g)△H=akJ/mol,其化学平衡常数K与温度的关系如下:
| 温度/oC | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
②理论上,为了增大平衡时H2的转化率,可采取的措施是ad(填字母序号).
a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物中的NH3
③400oC时,测得某时刻氨气、氮气、氢气的物质的量分别为3mol、2mol、1mol,此时刻该反应的v正(N2)<v逆(N2)(填“>”、“<”或“=”).
(4)25oC时,将amol•L-1的氨水与0.1mol•L-1的盐酸等体积混合
①当溶液中离子浓度关系满足c(NH4+)>c(Cl-)时,反应的情况可能为a(填字母序号).
a.盐酸不足,氨水剩余 b.氨水与盐酸恰好完全反应 c.盐酸过量
②当溶液中c(NH4+)=c(Cl-)时,用含a的代数式表示NH3•H2O的电离常数Kb=$\frac{1{0}^{-8}}{a-0.1}$.
18.工业上可利用煤的气化产物(CO和H2)合成二甲醚(CH3OCH3)同时生成二氧化碳,其三步反应如下:
①2H2(g)+CO(g)?CH3OH (g)△H=-90.8kJ•mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ•mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.3kJ•mol-1
(1)总合成反应的热化学方程式为3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-246.4kJ•mol.
(2)一定条件下的密闭容器中,上述总反应达到平衡时,要提高CO的转化率,可以采取的措施是CE(填字母代号).
A.高温高压 B.加入催化剂 C.减少CO2的浓度 D.增加CO的浓度 E.分离出二甲醚
(3)已知反应②2CH3OH(g)?CH3OCH3(g)+H2O(g)在某温度下的平衡常数K=400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如表格:
此时,v(正)> v(逆) 填“>”、“<”或“=”);达到平衡后,CH3OCH3的物质的量浓度是0.80mol/L.
0 160031 160039 160045 160049 160055 160057 160061 160067 160069 160075 160081 160085 160087 160091 160097 160099 160105 160109 160111 160115 160117 160121 160123 160125 160126 160127 160129 160130 160131 160133 160135 160139 160141 160145 160147 160151 160157 160159 160165 160169 160171 160175 160181 160187 160189 160195 160199 160201 160207 160211 160217 160225 203614
①2H2(g)+CO(g)?CH3OH (g)△H=-90.8kJ•mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ•mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.3kJ•mol-1
(1)总合成反应的热化学方程式为3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-246.4kJ•mol.
(2)一定条件下的密闭容器中,上述总反应达到平衡时,要提高CO的转化率,可以采取的措施是CE(填字母代号).
A.高温高压 B.加入催化剂 C.减少CO2的浓度 D.增加CO的浓度 E.分离出二甲醚
(3)已知反应②2CH3OH(g)?CH3OCH3(g)+H2O(g)在某温度下的平衡常数K=400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如表格:
| 物质 | CH3OH | CH3OCH3 | H2O |
| c/mol•L-1 | 0.44 | 0.60 | 0.60 |