16.在溶液中有浓度均为0.01mol•L-1的Fe3+、Cr3+、Zn2+、Mg2+等离子,已知:25℃时,Ksp[Fe(OH)3]=4.0×10-38;Ksp[Cr(OH)3]=7.0×10-31,Ksp[Zn(OH)2]=1.0×10-17;Ksp[Mg(OH)2]=1.8×10-11.当其氢氧化物刚开始沉淀时,下列哪一种离子所需的pH最小( )
| A. | Fe3+ | B. | Cr3+ | C. | Zn2+ | D. | Mg2+ |
15.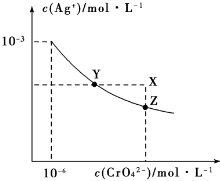 t℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
t℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
 t℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
t℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )| A. | 加热蒸发饱和Ag2CrO4溶液再恢复到t℃,可使溶液由Y点变到Z点 | |
| B. | 在X点没有Ag2CrO4沉淀生成,则此时温度低于t℃ | |
| C. | 向饱和Ag2CrO4溶液中加入少量AgNO3固体,可使溶液由Z点到Y点 | |
| D. | 在t℃时,Ag2CrO4的Ksp为1×10-9 |
9.对于已达到平衡的可逆反应:A(g)?2B(?)+C(g)△H>0,假设A、C状态保持不变,下列说法正确的是( )
| A. | 当混合气体的质量不变,说明反应已达平衡状态 | |
| B. | 缩小容器体积,重新达到平衡时,气体混合物中C%可能增大 | |
| C. | 在恒压容器中升高温度,气体混合物中C%可能先增大后减小 | |
| D. | 在恒容容器中升高温度,达到新平衡时,气体的密度增大 |
7.工业上用化学法除锅炉的水垢时,先向锅炉中注入饱和Na2CO3溶液侵泡,将水垢中的CaSO4转化为CaCO3,再用盐酸除去[Ksp(CaCO3)=1×10-10,Ksp(Ca SO4)=1×10-6].下列说法正确的是( )
0 160030 160038 160044 160048 160054 160056 160060 160066 160068 160074 160080 160084 160086 160090 160096 160098 160104 160108 160110 160114 160116 160120 160122 160124 160125 160126 160128 160129 160130 160132 160134 160138 160140 160144 160146 160150 160156 160158 160164 160168 160170 160174 160180 160186 160188 160194 160198 160200 160206 160210 160216 160224 203614
| A. | 温度升高,Na2CO3溶液中各种离子的浓度均增大 | |
| B. | 沉淀转化的离子方程式为CO32-(aq)+CaSO4(s)?CaCO3(s)+SO42-(aq) | |
| C. | 该条件下CaCO3的溶解度约为1×10-3g | |
| D. | CaCO3和CaSO4共存的体系中,一定有$\frac{c(S{O}_{4}^{2-})}{c(C{O}_{3}^{2-})}$=9×104 |
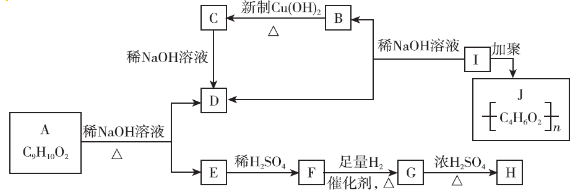
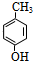 .
.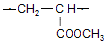 .
.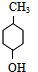 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$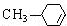 +H2O.
+H2O. .
.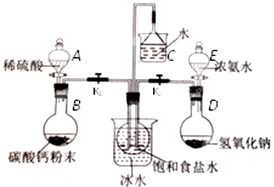
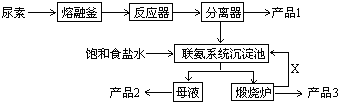
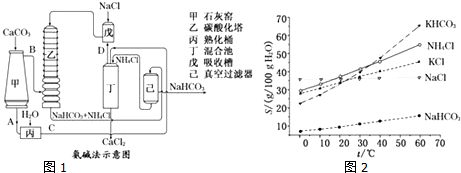
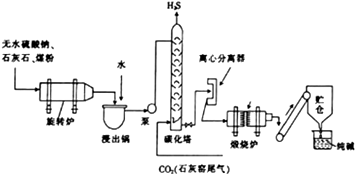 历史上路布兰法生产纯碱的工艺流程如图所示.
历史上路布兰法生产纯碱的工艺流程如图所示.