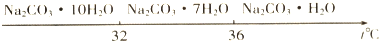6. 氨气是重要的化工原料.
氨气是重要的化工原料.
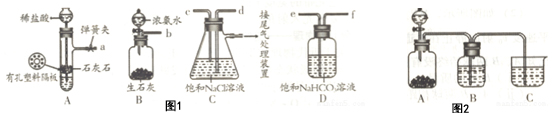
(1)实验室可用浓氨水和abd(选填编号)快速制取氨气.
a.烧碱 b.生石灰 c.氯化铵d.碱石灰
(2)“侯氏制碱”的核心反应为:
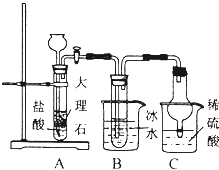
NH3+CO2+NaCl+H2O═NH4Cl+NaHCO3.依据此原理,欲制得碳酸氢钠晶体,某同学设计了如图实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和.
①C装置的作用为防倒吸、吸收过量氨气防污染.
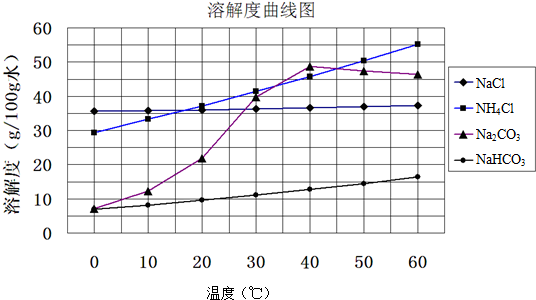
②如表列出的是相关物质在不同温度下的溶解度数据(g/100g水):
参照表中数据,请分析B装置中使用冰水的目的是低温便于析出碳酸氢钠.
③该同学在检查完此套装置的气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在AB装置之间(填写字母)连接一个盛有饱和碳酸氢钠溶液的洗气装置,其作用除去二氧化碳气体中的氯化氢气体.
④若该同学进行实验时,所用饱和食盐水中含NaCl的质量为11.7g,实验后得到干燥的NaHCO3晶体的质量为10.92g,则NaHCO3的产率为65%.
(3)往CuSO4溶液中滴加氨水,先有沉淀析出,后沉淀溶解溶液呈深蓝色,有[Cu(NH3)4]2+生成.往溶液中滴加稀硫酸,溶液变为淡蓝色.颜色变浅的原因除溶液变稀外,还可能存在平衡I:[Cu(NH3)4]2+ (深蓝色)+4H+?Cu2+(蓝色)+4NH4+
请设计一个简单实验证明平衡I是否存在往深蓝色溶液中通入少量HCl气体若溶液颜色变浅,证明有平衡Ⅰ的存在,否则不存在(或通入少量氨气或加少量NaOH固体,若溶液颜色变深证明平衡Ⅰ的存在,否则不存在).
 氨气是重要的化工原料.
氨气是重要的化工原料.(1)实验室可用浓氨水和abd(选填编号)快速制取氨气.
a.烧碱 b.生石灰 c.氯化铵d.碱石灰
(2)“侯氏制碱”的核心反应为:
NH3+CO2+NaCl+H2O═NH4Cl+NaHCO3.依据此原理,欲制得碳酸氢钠晶体,某同学设计了如图实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和.
①C装置的作用为防倒吸、吸收过量氨气防污染.
②如表列出的是相关物质在不同温度下的溶解度数据(g/100g水):
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
③该同学在检查完此套装置的气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在AB装置之间(填写字母)连接一个盛有饱和碳酸氢钠溶液的洗气装置,其作用除去二氧化碳气体中的氯化氢气体.
④若该同学进行实验时,所用饱和食盐水中含NaCl的质量为11.7g,实验后得到干燥的NaHCO3晶体的质量为10.92g,则NaHCO3的产率为65%.
(3)往CuSO4溶液中滴加氨水,先有沉淀析出,后沉淀溶解溶液呈深蓝色,有[Cu(NH3)4]2+生成.往溶液中滴加稀硫酸,溶液变为淡蓝色.颜色变浅的原因除溶液变稀外,还可能存在平衡I:[Cu(NH3)4]2+ (深蓝色)+4H+?Cu2+(蓝色)+4NH4+
请设计一个简单实验证明平衡I是否存在往深蓝色溶液中通入少量HCl气体若溶液颜色变浅,证明有平衡Ⅰ的存在,否则不存在(或通入少量氨气或加少量NaOH固体,若溶液颜色变深证明平衡Ⅰ的存在,否则不存在).
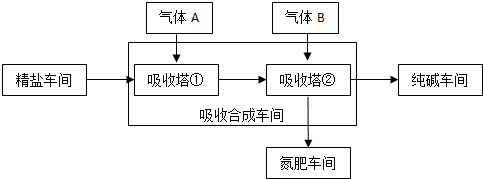
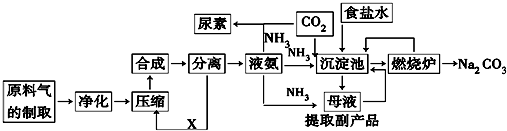
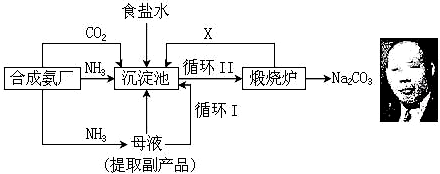
5.(1)应用氨厂生产的氨气,侯德榜设计了侯氏制碱法,其生产流程如下:
①工业合成氨时,通常采用以铁为主的催化剂,在温度为℃和压强为400~500、10~30MPa的条件下合成.
②沉淀池中发生反应的化学方程式NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓.
③上述流程中可循环利用的物质为NH3、CO2(填化学式),副产品为NH4Cl(填化学式).
④与氨碱法生产纯碱比较,侯氏制碱法有什么优点?综合利用原料(氯化钠的利用率提高到了96%)、降低成本、减少环境污染.
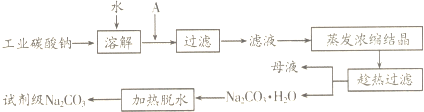
(2)实验室制备纯碱(Na2CO3)的主要步骤为:将饱和NaCl溶液倒入烧杯加热,控制30-35℃,搅拌下分批加入研细的NH4HCO3固体,加料完毕,保温30分钟,静置、过滤得NaHCO3晶体.用少量蒸馏水洗涤除去杂质、抽干,转入蒸发皿中灼烧得Na2CO3固体.
四种盐在不同温度下的溶解度(g/100g水)表
⑤反应温度需要控制在30-35℃,原因是温度高于35℃时碳酸氢铵受热分解剧烈,温度低于30℃又减慢了化学反应的速率;
为控制此温度范围,通常采取的加热方法为水浴加热.
⑥保温30分钟,静置后只析出NaHCO3晶体的原因相同温度下,碳酸氢钠的溶解度小.

①工业合成氨时,通常采用以铁为主的催化剂,在温度为℃和压强为400~500、10~30MPa的条件下合成.
②沉淀池中发生反应的化学方程式NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓.
③上述流程中可循环利用的物质为NH3、CO2(填化学式),副产品为NH4Cl(填化学式).
④与氨碱法生产纯碱比较,侯氏制碱法有什么优点?综合利用原料(氯化钠的利用率提高到了96%)、降低成本、减少环境污染.
(2)实验室制备纯碱(Na2CO3)的主要步骤为:将饱和NaCl溶液倒入烧杯加热,控制30-35℃,搅拌下分批加入研细的NH4HCO3固体,加料完毕,保温30分钟,静置、过滤得NaHCO3晶体.用少量蒸馏水洗涤除去杂质、抽干,转入蒸发皿中灼烧得Na2CO3固体.
四种盐在不同温度下的溶解度(g/100g水)表
温度 盐 溶解度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | - | - | - | - |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
为控制此温度范围,通常采取的加热方法为水浴加热.
⑥保温30分钟,静置后只析出NaHCO3晶体的原因相同温度下,碳酸氢钠的溶解度小.
3.有人常用废旧报纸包装食品,这是极不卫生的.原因是报纸上除含有多种病菌外,还会含有易使人中毒的多氯联苯和( )
| A. | 铅 | B. | 机油 | C. | 三氯化锑 | D. | 硫 |
2.1体积某气态烃和2体积氯化氢发生加成反应后,最多还能和6体积氯气发生取代反应.由此可以断定原气态烃是(气体体积均在相同条件下测定)( )
| A. | C2H2 | B. | C3H4 | C. | C3H8 | D. | C4H6 |
1.蔗糖3.42g与淀粉3.24g混合并完全水解,若生成mg葡萄糖和ng果糖,则m:n为( )
0 160027 160035 160041 160045 160051 160053 160057 160063 160065 160071 160077 160081 160083 160087 160093 160095 160101 160105 160107 160111 160113 160117 160119 160121 160122 160123 160125 160126 160127 160129 160131 160135 160137 160141 160143 160147 160153 160155 160161 160165 160167 160171 160177 160183 160185 160191 160195 160197 160203 160207 160213 160221 203614
| A. | 1:3 | B. | 1:5 | C. | 5:1 | D. | 3:1 |