19.将Na、Fe、Al各0.03mol分别放入100mL 0.1mol•L-1的盐酸中,同温同压下产生气体的体积比为( )
| A. | 1:2:3 | B. | 6:3:2 | C. | 3:1:1 | D. | 1:1:1 |
18.下列离子方程式书写正确的是( )
| A. | 氢氧化钠溶液和稀盐酸反应:H++OH-═H2O | |
| B. | 大理石与盐酸反应制取二氧化碳:CO32-+2H+═H2O+CO2↑ | |
| C. | 铁粉投入盐酸溶液中:2Fe+6H+═Fe3++3H2↑ | |
| D. | 用小苏打治疗胃酸过多:CO32-+2H+═CO2↑+H2O |
17.有关金属腐蚀的论述,正确的是( )
①金属的腐蚀一定伴有电流产生
②纯银器表面在空气中因化学腐蚀渐渐变暗
③可将地下输油钢管与外加直流电源的负极相连以保护它不受腐蚀
④发生化学能转变为电能的腐蚀时较活泼的金属总是作正极而被腐蚀
⑤发生电化学腐蚀时都有能量的转变,且被腐蚀的金属总是失电子
⑥当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
⑦海轮外壳连接锌块以保护外壳不受腐蚀.
①金属的腐蚀一定伴有电流产生
②纯银器表面在空气中因化学腐蚀渐渐变暗
③可将地下输油钢管与外加直流电源的负极相连以保护它不受腐蚀
④发生化学能转变为电能的腐蚀时较活泼的金属总是作正极而被腐蚀
⑤发生电化学腐蚀时都有能量的转变,且被腐蚀的金属总是失电子
⑥当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
⑦海轮外壳连接锌块以保护外壳不受腐蚀.
| A. | ②③⑤⑦ | B. | ①②③⑥⑦ | C. | ①②④⑦ | D. | ②③⑤⑥⑦ |
16.实现下列变化,一定要加入其它物质作氧化剂的是( )
| A. | CaCO3→CO2 | B. | Cl2→ClO- | C. | Zn→ZnCl2 | D. | CuO→CuSO4 |
15.氧化还原反应与四种基本反应类型的关系如图所示,下列化学反应中属于区域3的是( )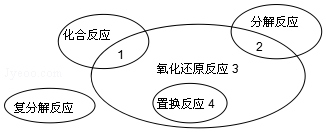

| A. | 2K2O2+2CO2═2K2CO3+O2 | B. | Cl2+2KBr═Br2+2KCl | ||
| C. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | D. | 2NaHCO3═Na2CO3+H2O+CO2↑ |
12.下列推断正确的是( )
| A. | 1 mol Na2O2与水反应,转移电子1 mol | |
| B. | Na2O、Na2O2组成元素相同,与CO2反应的产物也相同 | |
| C. | 钠能与氧气和水反应,钠暴露在空气中最终的产物是NaOH | |
| D. | 将Na2O2加入酚酞试液中,得到红色溶液 |
11.下列依据热化学方程式得出的结论正确的是( )
| A. | 若2CH3OH(1)+3O2(g)═2CO2(g)+2H2O(g)△H=-1478KJ/mol,则CH3OH(1)的燃烧热为739KJ/mol | |
| B. | 若P4(白磷,s)═4P(红磷,s)△H<0,则红磷比白磷稳定 | |
| C. | 已知H+(aq)+OH-(aq)═H2O(1)△H=-57.3KJ/mol,则20.0g NaOH固体与稀盐酸完全中和,放出28.65KJ的热量 | |
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H1; 2C(s)+O2(g)=2CO(g)△H2;△H1>△H2 |
10.在一定条件下,PbO2 与Cr3+反应,产物是Cr2O72-和Pb2+,则与5molCr3+反应所需PbO2的物质的量为( )
0 160026 160034 160040 160044 160050 160052 160056 160062 160064 160070 160076 160080 160082 160086 160092 160094 160100 160104 160106 160110 160112 160116 160118 160120 160121 160122 160124 160125 160126 160128 160130 160134 160136 160140 160142 160146 160152 160154 160160 160164 160166 160170 160176 160182 160184 160190 160194 160196 160202 160206 160212 160220 203614
| A. | 7.5mol | B. | 1.5mol | C. | 3mol | D. | 3.25mol |