18.向AgCl饱和溶液中加水,下列叙述正确的是( )
| A. | AgCl的溶解度增大 | B. | AgCl的溶解度、溶度积KSP均不变 | ||
| C. | AgCl的溶度积KSP增大 | D. | AgCl的溶解度、溶度积KSP均增大 |
17.为处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏.化学家研究在催化条件下,通过下列反应,使CCl4转化为重要的化工原料氯仿(CHCl3).CCl4+H2?CHCl3+HCl△H<0 已知CCl4的沸点为77℃,CHCl3的沸点为61.2℃.
(1)在密闭器中,该反应达到平衡后,测得如表数据.
①实验1中,10h后达到平衡,H2的平均反应速率为0.05mol•L-1•h-1.在此实验的平衡体系中,再加入0.5molCCl4和0.5molHCl,平衡将不移动(“向左”、“向右”、“不”或“无法确定”).
②实验2中,X的值B(填序号).
A.等于50% B.大于50% C.小于50% D.无法确定
③实验3中的Y值为1.2.
(2)为从平衡体系CCl4+H2?CHCl3+HCl中分离得到CHCl3,请你结合题给信息设计合理的方案,用简要的文字表示:先把平衡体系中的混合物降温到61.2℃以下得到CCl4和CHCl3液态混合物,再分馏得到CHCl3.
(1)在密闭器中,该反应达到平衡后,测得如表数据.
| 实验序号 | 温度(℃) | 初始CCl4浓度(mol•L-1) | 初始H2浓度(mol•L-1) | CCl4的平衡转化率 |
| 1 | 110 | 1 | 1 | 50% |
| 2 | 100 | 1 | 1 | X |
| 3 | 110 | 0.8 | Y | 60% |
②实验2中,X的值B(填序号).
A.等于50% B.大于50% C.小于50% D.无法确定
③实验3中的Y值为1.2.
(2)为从平衡体系CCl4+H2?CHCl3+HCl中分离得到CHCl3,请你结合题给信息设计合理的方案,用简要的文字表示:先把平衡体系中的混合物降温到61.2℃以下得到CCl4和CHCl3液态混合物,再分馏得到CHCl3.
15.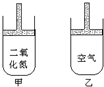 常温常压下在可移动活塞的甲、乙容器(如图)里分别充有等体积的二氧化氮(已建立了平衡:2NO2?N2O4;△H<0.)和空气,现分别进行下列两个实验:
常温常压下在可移动活塞的甲、乙容器(如图)里分别充有等体积的二氧化氮(已建立了平衡:2NO2?N2O4;△H<0.)和空气,现分别进行下列两个实验:
①将两容器置于沸水中加热;②在活塞上都加2千克的砝码.
在以上两情况下,甲和乙容器中气体体积大小的比较,正确的是( )
 常温常压下在可移动活塞的甲、乙容器(如图)里分别充有等体积的二氧化氮(已建立了平衡:2NO2?N2O4;△H<0.)和空气,现分别进行下列两个实验:
常温常压下在可移动活塞的甲、乙容器(如图)里分别充有等体积的二氧化氮(已建立了平衡:2NO2?N2O4;△H<0.)和空气,现分别进行下列两个实验:①将两容器置于沸水中加热;②在活塞上都加2千克的砝码.
在以上两情况下,甲和乙容器中气体体积大小的比较,正确的是( )
| A. | ①甲>乙②甲>乙 | B. | ①甲>乙②甲<乙 | C. | ①甲<乙②甲>乙 | D. | ①甲>乙②甲=乙 |
13.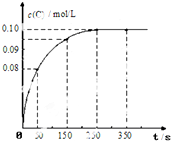 在一定温度下,向2L恒容密闭容器中充入1mol A,发生A(g)?B(g)+C(g)反应.反应过程中c(C) 随时间变化的曲线如图所示,下列说法不正确的是( )
在一定温度下,向2L恒容密闭容器中充入1mol A,发生A(g)?B(g)+C(g)反应.反应过程中c(C) 随时间变化的曲线如图所示,下列说法不正确的是( )
 在一定温度下,向2L恒容密闭容器中充入1mol A,发生A(g)?B(g)+C(g)反应.反应过程中c(C) 随时间变化的曲线如图所示,下列说法不正确的是( )
在一定温度下,向2L恒容密闭容器中充入1mol A,发生A(g)?B(g)+C(g)反应.反应过程中c(C) 随时间变化的曲线如图所示,下列说法不正确的是( )| A. | 反应在0~50s的平均速率v(C)=1.6×10-3mol/(L•s) | |
| B. | 该温度下,反应的平衡常数K=0.025 | |
| C. | 保持其他条件不变,升高温度,平衡时c(B)=0.11mol/L,则该反应的△H<0 | |
| D. | 反应达平衡后,再向容器中充入 1 mol A,该温度下再达到平衡时0.1mol/L<c(C)<0.2mol/L |
12.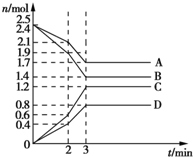 在某容积为2L的密闭容器中,A、B、C、D四种气体物质发生可逆反应,其物质的量n(mol)随时间t(min)的变化如图所示.下列说法正确的是( )
在某容积为2L的密闭容器中,A、B、C、D四种气体物质发生可逆反应,其物质的量n(mol)随时间t(min)的变化如图所示.下列说法正确的是( )
 在某容积为2L的密闭容器中,A、B、C、D四种气体物质发生可逆反应,其物质的量n(mol)随时间t(min)的变化如图所示.下列说法正确的是( )
在某容积为2L的密闭容器中,A、B、C、D四种气体物质发生可逆反应,其物质的量n(mol)随时间t(min)的变化如图所示.下列说法正确的是( )| A. | 前2min内,v(A)=0.2 mol/(L•min) | |
| B. | 在2min时,图象发生改变的原因只可能是增大压强 | |
| C. | 其他条件不变,3min时体系的压强不再发生变化 | |
| D. | 增加气体D的浓度,A的反应速率随之减小 |
11.用NH3催化还原NxOy可以消除氮氧化物的污染.
已知:反应I:4NH3(g)+6NO(g)?5N2(g)+6H2O(l)△H1
反应II:2NO(g)+O2(g)?2NO2(g)△H2 (且|△H1|=2|△H2|)
①现用NH3与NO2以2:3混合可得空气中的两主要气体和液态水,写出此反应的热化学方程式4NH3(g)+6NO2(g)?5N2(g)+3O2(g)+6H2O(l)△H=△H1-3△H2(用△H1.△H2的代数式表示反应热) 推测该反应是吸热反应(填“吸热”或“放热”)
②下列说法不正确的是C
A.反应I:单位时间内H-O键与N-H键断裂的数目相等时,说明反应已经达到平衡
B.反应I:若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
C.反应II:增大压强能使反应速率加快,是因为增加了活化分子百分数
D.恒温恒容条件下,反应II达到平衡时体系中n(NO):n(O2):n(NO2)=2:1:2.在其它条件不变时,再充入NO2气体达到平衡,NO2体积分数变大.
0 160014 160022 160028 160032 160038 160040 160044 160050 160052 160058 160064 160068 160070 160074 160080 160082 160088 160092 160094 160098 160100 160104 160106 160108 160109 160110 160112 160113 160114 160116 160118 160122 160124 160128 160130 160134 160140 160142 160148 160152 160154 160158 160164 160170 160172 160178 160182 160184 160190 160194 160200 160208 203614
已知:反应I:4NH3(g)+6NO(g)?5N2(g)+6H2O(l)△H1
反应II:2NO(g)+O2(g)?2NO2(g)△H2 (且|△H1|=2|△H2|)
| 温度/K | 反应I | 反应II | 已知: K2>K1>K2′>K1′ |
| 298 | K1 | K2 | |
| 398 | K1′ | K2′ |
②下列说法不正确的是C
A.反应I:单位时间内H-O键与N-H键断裂的数目相等时,说明反应已经达到平衡
B.反应I:若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
C.反应II:增大压强能使反应速率加快,是因为增加了活化分子百分数
D.恒温恒容条件下,反应II达到平衡时体系中n(NO):n(O2):n(NO2)=2:1:2.在其它条件不变时,再充入NO2气体达到平衡,NO2体积分数变大.
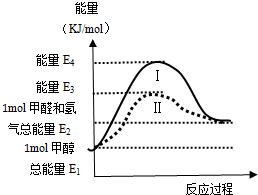 甲醇是重要的化工原料,气态甲醇催化脱氢制备甲醛转化的能量关系如图所示.
甲醇是重要的化工原料,气态甲醇催化脱氢制备甲醛转化的能量关系如图所示.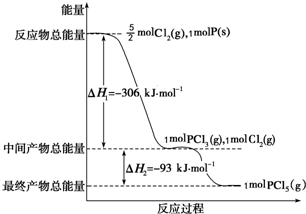 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).