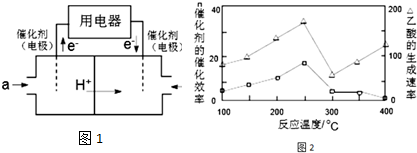
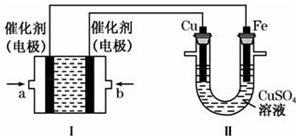
9.下列有关热化学方程式的叙述正确的是( )
| A. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,若将含0.6mol H2SO4的稀硫酸与含1mol NaOH的稀溶液混合,放出的热量等于57.3 kJ | |
| B. | 已知正丁烷(g)→异丁烷(g)△H<0,则正丁烷比异丁烷稳定 | |
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1,则H2的燃烧热为571.6 kJ•mol-1 | |
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)═2CO(g)△H2,则△H1>△H2 |
6.T K时,向2L恒容密闭容器中充入1molCOCl2,发生反应COCl2(g)?Cl2(g)+CO(g),经过一段时间后达到平衡,反应过程中测定的部分数据见下表:
下列说法正确的是( )
| t/% | 0 | 2 | 4 | 6 | 8 |
| n(Cl2)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A. | 反应在前2s的平均速率v(CO)=0.080mol/L/s | |
| B. | 保持其他条件不变,升高温度,平衡时c(Cl2)=0.11mol/L | |
| C. | T K时起始向容器中充入0.9molCOCl2/0.10molCO,反应达到平衡前v(正)>v(逆) | |
| D. | T K时起始向容器中充入1.0molCl2和0.9molCO.达到平衡时,Cl2的转化率小于80% |
3.已知2-丁烯有顺、反两种异构体,在某条件下两种气体处于平衡,下列说法正确的是( )
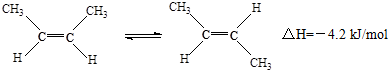

| A. | 顺-2-丁烯比反-2-丁烯稳定 | |
| B. | 顺-2-丁烯的燃烧热比反-2-丁烯大 | |
| C. | 加压和降温有利于平衡向生成顺-2-丁烯反应方向移动 | |
| D. | 它们与氢气加成反应后的产物具有不同的沸点 |
2.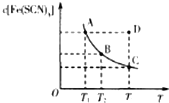 已知:FeCl3(aq)+3KSCN(aq)?3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是( )
已知:FeCl3(aq)+3KSCN(aq)?3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是( )
 已知:FeCl3(aq)+3KSCN(aq)?3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是( )
已知:FeCl3(aq)+3KSCN(aq)?3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是( )| A. | A点与B点相比,A点的血红色沉淀更多 | |
| B. | 加入KCl固体可以使溶液由D点变到C点 | |
| C. | 反应处于D点时,一定有V(正)<V(逆) | |
| D. | 若T1、T2温度下的平衡常数分别为K1、K2,K1<K2 |
1.下列说法正确的是( )
0 160013 160021 160027 160031 160037 160039 160043 160049 160051 160057 160063 160067 160069 160073 160079 160081 160087 160091 160093 160097 160099 160103 160105 160107 160108 160109 160111 160112 160113 160115 160117 160121 160123 160127 160129 160133 160139 160141 160147 160151 160153 160157 160163 160169 160171 160177 160181 160183 160189 160193 160199 160207 203614
| A. | 热化学方程式中,化学式前面的化学计量数既可表示微粒数,又可表示物质的量 | |
| B. | 热化学方程式中,如果没有注明温度和压强则表示在标准状况下测得的数据 | |
| C. | 书写热化学方程式时,不仅要写明反应热的符号和数值,还要注明各物质的聚集状态 | |
| D. | 1mol碳燃烧所放出的热量为燃烧热,1mol强酸和1mol强碱完全反应所放出的热称为中和热 |
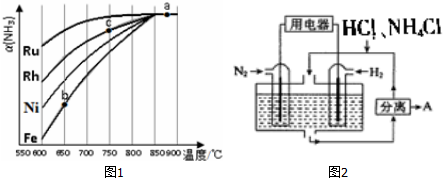
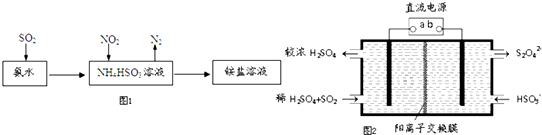 SO2和NOx都是大气污染物.
SO2和NOx都是大气污染物.