7.氨气是化学工业上应用非常广泛的物质.侯氏制碱法的第一步反应是向饱和氨化盐水中通入二氧化碳.现在45℃时,取117g食盐配制成饱和溶液,向其中通入适量氨气后,再向其中通入二氧化碳,使反应进行完全.试计算并回答下列问题(计算结果取三位有效数字)(有关物质的溶解度数据如表,单位:g/100g水).
(1)117g食盐理论上可以制取纯碱106g;45℃反应完毕后,有晶体析出;溶液中剩余水280g,析出晶体的质量129g;过滤除去析出的晶体后再降温至10℃,又有晶体析出,则所析出晶体的质量共30.8克.
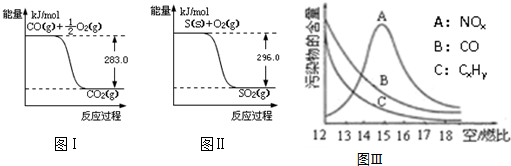
工业制硝酸也是氨气重要用途之一,反应如下:
4NH3+5O2→4NO+6H2O 2NO+O2→2NO2 3NO2+H2O→2HNO3+NO
设空气中氧气的体积分数为0.20,氮气的体积分数为0.80.
(2)a mol NO完全转化为HNO3理论上需要氧气0.75amol;为使NH3恰好完全氧化为NO,氨-空气混合气体中氨的体积分数(用小数表示)为0.14.
(3)20.0mol NH3用空气氧化,产生混合物的组成为:NO 18.0mol、O2 12.0mol、N2 150.0mol和一定量硝酸,以及其他成分(高温下NO与O2不化合).计算氨转化为HNO3的转化率.
(写出简要计算过程)
| 1 | NaCl | NaHCO3 | NH4Cl |
| 10℃ | 35.8 | 8.15 | 33.0 |
| 45℃ | 37.0 | 14.0 | 50.0 |
工业制硝酸也是氨气重要用途之一,反应如下:
4NH3+5O2→4NO+6H2O 2NO+O2→2NO2 3NO2+H2O→2HNO3+NO
设空气中氧气的体积分数为0.20,氮气的体积分数为0.80.
(2)a mol NO完全转化为HNO3理论上需要氧气0.75amol;为使NH3恰好完全氧化为NO,氨-空气混合气体中氨的体积分数(用小数表示)为0.14.
(3)20.0mol NH3用空气氧化,产生混合物的组成为:NO 18.0mol、O2 12.0mol、N2 150.0mol和一定量硝酸,以及其他成分(高温下NO与O2不化合).计算氨转化为HNO3的转化率.
(写出简要计算过程)
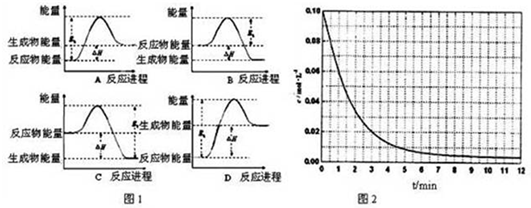
2.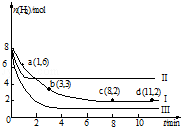 一定温度下,向容积为2L的恒容密闭容器中充入6mol CO2和8mol H2,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,测得n(H2)随时间变化如曲线Ⅰ所示.下列说法正确的是( )
一定温度下,向容积为2L的恒容密闭容器中充入6mol CO2和8mol H2,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,测得n(H2)随时间变化如曲线Ⅰ所示.下列说法正确的是( )
 一定温度下,向容积为2L的恒容密闭容器中充入6mol CO2和8mol H2,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,测得n(H2)随时间变化如曲线Ⅰ所示.下列说法正确的是( )
一定温度下,向容积为2L的恒容密闭容器中充入6mol CO2和8mol H2,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,测得n(H2)随时间变化如曲线Ⅰ所示.下列说法正确的是( )| A. | 该反应在0~8 min内CO2的平均反应速率是 0.375 mol•L-1•min-1 | |
| B. | 若起始时向上述容器中充入3 mol CO2和4 mol H2,则平衡时H2的体积分数大于20% | |
| C. | 若起始时向上述容器中充入4 mol CO2、2 mol H2、2 mol CH3OH和1mol H2O(g),则此时反应向正反应方向进行 | |
| D. | 改变条件得到曲线Ⅱ、Ⅲ,则曲线Ⅱ、Ⅲ改变的条件分别是升高温度、充入氦气 |
20.“Cl化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义
(1)一定温度下,在两个容积均为2L的密闭容器中,分别发生反应:CO2 (g)+3H2(g)?CH3OH g)+H2O(g)△H=-49.0kJ/mol.相关数据如下:
请回答:①c1=c2(填“>”、“<”或“=”);a=19.6.
②若甲中反应10s时达到平衡,则用CO2来表示甲中反应从开始到平衡过程中的平均反应速率是0.03mol/(L•S)
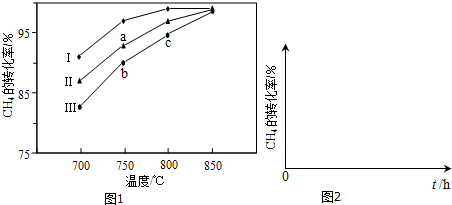
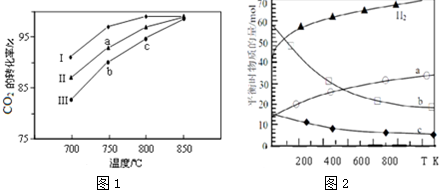
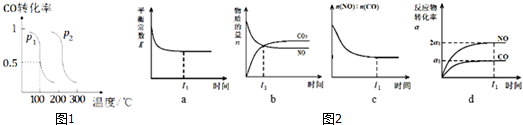
(2)压强为p1时,向体积为1L的密闭容器中充入b mol CO 和2b mol H2,发生反应CO (g)+2H2(g)?CH3OH(g).平衡时CO的转化率与温度、压强的关系如图1所示.请回答:①该反应属于放(填“吸”或“放”)热反应;p1 <p2(填“>”、“<”或“=”)
②100℃时,该反应的平衡常数K=$\frac{1}{{b}^{2}}$(用含b的代数式表示).
(3)一定条件下,治理汽车尾气的反应是2NO(g)+2CO(g)?2CO2(g)+N2(g)△H<0.在恒温恒容的密闭容器中通入n(NO):n(CO)=1:2的混合气体,发生上述反应.下列图象正确且能说明反应在进行到t1时刻一定达到平衡状态的是cd(选填字母).
0 160011 160019 160025 160029 160035 160037 160041 160047 160049 160055 160061 160065 160067 160071 160077 160079 160085 160089 160091 160095 160097 160101 160103 160105 160106 160107 160109 160110 160111 160113 160115 160119 160121 160125 160127 160131 160137 160139 160145 160149 160151 160155 160161 160167 160169 160175 160179 160181 160187 160191 160197 160205 203614
(1)一定温度下,在两个容积均为2L的密闭容器中,分别发生反应:CO2 (g)+3H2(g)?CH3OH g)+H2O(g)△H=-49.0kJ/mol.相关数据如下:
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH(g)和1mol H2O(g) |
| 平衡时c(CH3OH) | c1 | c2 |
| 平衡时能量变化 | 放出29.4kJ | 吸收 a kJ |
②若甲中反应10s时达到平衡,则用CO2来表示甲中反应从开始到平衡过程中的平均反应速率是0.03mol/(L•S)
(2)压强为p1时,向体积为1L的密闭容器中充入b mol CO 和2b mol H2,发生反应CO (g)+2H2(g)?CH3OH(g).平衡时CO的转化率与温度、压强的关系如图1所示.请回答:①该反应属于放(填“吸”或“放”)热反应;p1 <p2(填“>”、“<”或“=”)
②100℃时,该反应的平衡常数K=$\frac{1}{{b}^{2}}$(用含b的代数式表示).
(3)一定条件下,治理汽车尾气的反应是2NO(g)+2CO(g)?2CO2(g)+N2(g)△H<0.在恒温恒容的密闭容器中通入n(NO):n(CO)=1:2的混合气体,发生上述反应.下列图象正确且能说明反应在进行到t1时刻一定达到平衡状态的是cd(选填字母).