10.下列变化必须加还原剂才能发生的是( )
| A. | Na2CO3→NaHCO3 | B. | MnO4-→Mn2+ | C. | Cu→CuO | D. | H2O2→H2O |
9.同温同压下,2体积某气体分解成1体积X2气体与3体积Y2气体,则该化合物的化学式为( )
| A. | XY | B. | X3Y | C. | XY3 | D. | X2Y3 |
8.在不同条件下,分别测得反应2SO2(g)+O2(g)?2SO3(g)的化学反应速率,则其中表示该反应最快的是( )
| A. | v(O2)=0.2mol/(L•s) | B. | v(SO3)=8mol/(L•min) | C. | v(SO2)=6mol/(L•min) | D. | v(O2)=6mol/(L•min) |
7.对于反应4A(s)+2B(g)?3C(g),下列说法正确的是( )
| A. | 体积不变充入惰性气体,反应速率增大 | |
| B. | 其他条件不变,降低温度,平衡转化率一定变化 | |
| C. | 其他条件不变时,增大压强,平衡左移,平衡常数K减小 | |
| D. | 若增加或减少A物质的量,反应速率一定会发生明显的变化 |
6.现有三组溶液,①碘水中提取单质碘 ②碘和四氯化碳的混合物 ③汽油和氯化钠溶液,分离以上混合物的正确方法依次是( )
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
5.下列化学用语应用正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | 乙醇的分子式:CH3CH2OH | ||
| C. | 甲烷的结构式:CH4 | D. | 甲苯的键线式: |
4.某气体可能含有CO、CO2、H2、HCl和水蒸气中的一种或几种,依次通过硝酸银溶液(有浑浊现象)、氢氧化钠溶液(有浑浊现象)、浓硫酸、灼热的氧化铜(变红)和无水CuSO4(变蓝),判断该气体中一定有( )
| A. | HCl、CO2、CO | B. | CO、H2、H2O | C. | HCl、CO2、H2 | D. | HCl、CO2、H2 |
3.下列反应中,在高温下不能自发进行的是( )
| A. | 2CO(g)═2C(s)+O2(g) | B. | NH4Cl(s)=NH3(g)+HCl(g) | ||
| C. | (NH4)2CO3(s)═NH4HCO3(s)+NH3(g) | D. | MgCO3(s)═MgO(s)+CO2(g) |
2.2SO2(g)+O2(g)$?_{△}^{V_{2}O_{5}}$2SO3(g)是制备硫酸的重要反应.下列叙述正确的是( )
| A. | 该反应是放热反应,降低温度将缩短反应达到平衡的时间 | |
| B. | 增大反应体系的压强,反应速率一定增大 | |
| C. | 进入接触室的SO2和空气必须进行净化,且该反应不需要在高压下进行 | |
| D. | 催化剂V2O5能增大该反应的正反应速率而不改变逆反应速率 |
1.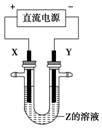 利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
0 160008 160016 160022 160026 160032 160034 160038 160044 160046 160052 160058 160062 160064 160068 160074 160076 160082 160086 160088 160092 160094 160098 160100 160102 160103 160104 160106 160107 160108 160110 160112 160116 160118 160122 160124 160128 160134 160136 160142 160146 160148 160152 160158 160164 160166 160172 160176 160178 160184 160188 160194 160202 203614
 利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )| A. | 氯碱工业中,X、Y均为石墨,X附近能得到氢氧化钠 | |
| B. | 铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4 | |
| C. | 电镀工业中,X是待镀金属,Y是镀层金属 | |
| D. | 若Z是稀硫酸,X为铜,Y为铁,则铁不溶解,该方法为外加电流的阴极保护法 |