10.向容积固定为2L的密闭容器中充入9.6mol NO和4.8mol O2,发生如下反应:

①2NO(g)+O2 (g)?2NO2(g)△H<0 ②2NO2(g)?N2O4(g)△H<0
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T℃,10min时改变某反应条件,一段时间后再次平衡.下列说法正确的是( )

①2NO(g)+O2 (g)?2NO2(g)△H<0 ②2NO2(g)?N2O4(g)△H<0
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T℃,10min时改变某反应条件,一段时间后再次平衡.下列说法正确的是( )
| A. | 前5min反应的平均速率v(NO)=0.24mol•(L•min)-1 | |
| B. | T℃时反应①的化学平衡常数K=0.36 | |
| C. | 10min时改变反应条件可能是降低温度 | |
| D. | 若起始时向该容器中充入1.6mol NO2和4.0mol N2O4,T℃达到平衡时,NO2的物质的量浓度与图中5~10min的不同 |
9.化工生产中常用FeS作沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+FeS(s)?CuS(s)+Fe2+(aq),下列有关叙述中正确的是( )
| A. | FeS的Ksp小于CuS的Ksp | |
| B. | 该反应平衡常数K=$\frac{{K}_{sp}(FeS)}{{K}_{sp}(CuS)}$ | |
| C. | 溶液中加入少量Na2S固体后,溶液中c(Cu2+)、c(Fe2+)保持不变 | |
| D. | 达到平衡时c(Fe2+)=c(Cu2+) |
8.在2L密闭容器内,充入0.2mol NO气体和0.1molO2,T℃时下列反应:
2NO(g)+O2(g)═2NO2(g)体系中n(NO)随时间的变化如表:
(1)写出该反应的平衡常数表达式:K=$\frac{{c}^{2}(N{O}_{2})}{{c}^{2}(NO)c({O}_{2})}$.该温度下反应的平衡常数K=$\frac{900}{8}$.
已知:K300℃>K350℃,则该反应是放热反应.
(2)达到平衡时v(NO)为2×10-2 mol/(L•s).
(3)能说明该反应已达到平衡状态的是be.
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.NO、O2、NO2的浓度之比为2:1:2 d.容器内气体的密度保持不变
e.容器内气体的颜色不再变化
(4)达到平衡时若移走部分NO2,则下列说法正确的是bc.
a.平衡将向正向移动,正反应速率增大,逆反应速率减小
b.重新到达平衡时,NO的平衡转化率将增大,平衡常数不变
c.重新到达平衡时,容器内混合气体的密度较原来减小,压强也减小.
2NO(g)+O2(g)═2NO2(g)体系中n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.20 | 0.10 | 0.09 | 0.08 | 0.08 | 0.08 |
已知:K300℃>K350℃,则该反应是放热反应.
(2)达到平衡时v(NO)为2×10-2 mol/(L•s).
(3)能说明该反应已达到平衡状态的是be.
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.NO、O2、NO2的浓度之比为2:1:2 d.容器内气体的密度保持不变
e.容器内气体的颜色不再变化
(4)达到平衡时若移走部分NO2,则下列说法正确的是bc.
a.平衡将向正向移动,正反应速率增大,逆反应速率减小
b.重新到达平衡时,NO的平衡转化率将增大,平衡常数不变
c.重新到达平衡时,容器内混合气体的密度较原来减小,压强也减小.
7.下列有关AgCl沉淀的溶解平衡的说法中,正确的是( )
| A. | AgCl沉淀生成和溶解不断进行,但速率相等 | |
| B. | AgCl难溶于水,溶液中没有Ag+和Cl- | |
| C. | 其他条件不变时,加水可使Ksp(AgCl)增大 | |
| D. | 向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度不变 |
6.已知20°C时AgBr的溶解度为8.4×10-6AgCI的溶解度为1.5×10-4将AgCl与AgBr的饱和溶液等体积混合,再加入足量浓硝酸银,发生的反应为( )
| A. | 只有AgBr沉淀生成 | B. | AgCl沉淀多于AgBr沉淀 | ||
| C. | AgCl沉淀少于AgBr沉淀 | D. | AgCl和AgBr沉淀等量生成 |
5.已知:Ksp(AgCl)=1.8×10-10;Ksp(Ag2S)=6.3×10-50.向盛0.1mol/L AgNO3溶液的试管中滴加0.1mol/L Na2S溶液至沉淀完全,再滴加足量NaCl溶液,产生的现象或生成的物质是( )
| A. | 黑色沉淀完全转化为白色沉淀 | B. | 既有氯化银也有硫化银 | ||
| C. | 只产生黑色硫化银沉淀 | D. | 只有氯化银白色沉淀 |
4.煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
(1)已知:C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-111kJ•mol-1 2H2(g)+O2(g)═2H2O(g)△H=-484kJ•mol-1.请写出水蒸气通过红热的碳产生水煤气的热化学方程式C(s)+H2O(g)?CO(g)+H2(g)△H=+131kJ•mol-1.一定温度下,在一个容积固定的密闭容器中发生上述反应,下列能判断该反应达到化学平衡状态的是abce(填字母编号).
a.容器中的压强不变 b.1mol H-H键断裂的同时断裂2mol H-O键
c.v正(CO)=v逆(H2O) d.c(CO)=c(H2) e.容器中混合气体的密度不再改变
(2)将不同物质的量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如表中所示的三组数据:
①实验1中以v(CO2)表示的反应速率为0.16mol•(L•min)-1.
②该反应的逆反应为吸(填“吸”或“放”)热反应.
③若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),则a、b应满足的关系是b=2a,且a>1(用含a、b的代数式表示).
(3)目前工业上有一种方法是用CO2来生产甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图1表示该反应过程中能量的变化.
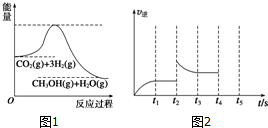
①在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,下列措施中能使CH3OH的体积分数增大的是cde(填字母编号).
a.升高温度 b.充入He(g) c.将H2O(g)从体系中分离出来 d.再充入1mol CO2和3mol H2
e.将该密闭容器改为恒压密闭容器
②容器中反应的逆反应速率随时间变化的关系如图2.t2时改变了某一种条件,改变的条件可能是升高温度.(任写一点)
(1)已知:C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-111kJ•mol-1 2H2(g)+O2(g)═2H2O(g)△H=-484kJ•mol-1.请写出水蒸气通过红热的碳产生水煤气的热化学方程式C(s)+H2O(g)?CO(g)+H2(g)△H=+131kJ•mol-1.一定温度下,在一个容积固定的密闭容器中发生上述反应,下列能判断该反应达到化学平衡状态的是abce(填字母编号).
a.容器中的压强不变 b.1mol H-H键断裂的同时断裂2mol H-O键
c.v正(CO)=v逆(H2O) d.c(CO)=c(H2) e.容器中混合气体的密度不再改变
(2)将不同物质的量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如表中所示的三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/mi n | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
②该反应的逆反应为吸(填“吸”或“放”)热反应.
③若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),则a、b应满足的关系是b=2a,且a>1(用含a、b的代数式表示).
(3)目前工业上有一种方法是用CO2来生产甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图1表示该反应过程中能量的变化.

①在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,下列措施中能使CH3OH的体积分数增大的是cde(填字母编号).
a.升高温度 b.充入He(g) c.将H2O(g)从体系中分离出来 d.再充入1mol CO2和3mol H2
e.将该密闭容器改为恒压密闭容器
②容器中反应的逆反应速率随时间变化的关系如图2.t2时改变了某一种条件,改变的条件可能是升高温度.(任写一点)
3.下列有关沉淀溶解平衡的说法正确的是( )
| A. | Ksp(AB2)<Ksp(CD),则物质AB2的溶解度一定小于物质CD的溶解度 | |
| B. | 在氯化银的沉淀溶解平衡体系中,加入蒸馏水,氯化银的Ksp增大 | |
| C. | 在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘化银 | |
| D. | 在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,溶解平衡不移动 |
2.实验:①0.1mol•L-1AgNO3溶液和0.1mol•L-1NaCl溶液等体积混合得到浊液,过滤.
②分别取少量①的浊液,分别滴加等浓度等体积的饱和Na2S溶液、饱和Na2SO4溶液,前者出现浑浊,后者溶液仍澄清③取少量①的沉淀,滴加几滴氨水,沉淀逐渐溶解
下列分析不正确的是( )
0 159994 160002 160008 160012 160018 160020 160024 160030 160032 160038 160044 160048 160050 160054 160060 160062 160068 160072 160074 160078 160080 160084 160086 160088 160089 160090 160092 160093 160094 160096 160098 160102 160104 160108 160110 160114 160120 160122 160128 160132 160134 160138 160144 160150 160152 160158 160162 160164 160170 160174 160180 160188 203614
②分别取少量①的浊液,分别滴加等浓度等体积的饱和Na2S溶液、饱和Na2SO4溶液,前者出现浑浊,后者溶液仍澄清③取少量①的沉淀,滴加几滴氨水,沉淀逐渐溶解
下列分析不正确的是( )
| A. | 实验②证明了①的滤液中含有Ag+,由此推断的滤液中也含有Cl- | |
| B. | 由实验③推测:若在①的沉淀中滴加NaOH溶液,沉淀也能溶解 | |
| C. | 实验的溶液中含有[Ag(NH3)2]+微粒 | |
| D. | 实验证明了该温度下Ag2S比Ag2SO4更难溶解 |