16.ICl3遇水会产生大量的腐蚀性白色浓雾,有强烈的催泪性.若两种生成物之一是HCl,则另一种是( )
| A. | HIO3 | B. | HIO2 | C. | HIO | D. | ICl |
11. 在恒温条件下起始时容积均为5L的甲、乙两密闭容器中(甲为恒容容器、乙为恒压容器),均进行反应:N2(g)+3H2(g)?2NH3(g)△H2=-92.4kJ/mol,有关数据及特定平衡状态见表.
在恒温条件下起始时容积均为5L的甲、乙两密闭容器中(甲为恒容容器、乙为恒压容器),均进行反应:N2(g)+3H2(g)?2NH3(g)△H2=-92.4kJ/mol,有关数据及特定平衡状态见表.
(1)若平衡后同种物质的体积分数相同,起始时乙容器通入的N2的物质的量为1.6mol,
起始时乙中的压强是甲容器的0.8倍,乙的平衡常数为107(mol/L)-2
(2)恒容密闭容器中可以发生氨气的分解反应,达平衡后,仅改变下表中反应条件x,下列各项中y随x的增大而增大的是bc(选填序号).
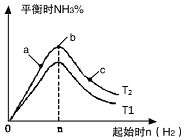
(3)研究在其他条件不变时,改变起始物氢气的物质的量对反应的影响,实验结果如图所示(图中T表示温度,n表示物质的量):
①像中T2和T1的关系是:T2低于T1(填“高于”“低于”“等于”“无法确定”).
②a、b、c三点中,N2转化率最高的是c(填字母).
③若容器容积为1L,T2℃在起始体系中加入1mol N2,3molH2,经过5min反应达到平衡时H2的转化率为60%,则NH3的反应速率为0.24mol.L-1.min-1.保持容器体积不变,若起始时向容器内放入2mol N2和6mol H2,达平衡后放出的热量为Q,则Q>110.88kJ(填“>”、“<”或“=”).
0 159947 159955 159961 159965 159971 159973 159977 159983 159985 159991 159997 160001 160003 160007 160013 160015 160021 160025 160027 160031 160033 160037 160039 160041 160042 160043 160045 160046 160047 160049 160051 160055 160057 160061 160063 160067 160073 160075 160081 160085 160087 160091 160097 160103 160105 160111 160115 160117 160123 160127 160133 160141 203614
 在恒温条件下起始时容积均为5L的甲、乙两密闭容器中(甲为恒容容器、乙为恒压容器),均进行反应:N2(g)+3H2(g)?2NH3(g)△H2=-92.4kJ/mol,有关数据及特定平衡状态见表.
在恒温条件下起始时容积均为5L的甲、乙两密闭容器中(甲为恒容容器、乙为恒压容器),均进行反应:N2(g)+3H2(g)?2NH3(g)△H2=-92.4kJ/mol,有关数据及特定平衡状态见表.| 容器 | 起始投入 | 达平衡时 | |||
| 甲 | 2molN2 | 3molH2 | 0molNH3 | 1.5molNH3 | |
| 乙 | amolN2 | bmolH2 | 0molNH3] | 1.2molNH3 | |
起始时乙中的压强是甲容器的0.8倍,乙的平衡常数为107(mol/L)-2
(2)恒容密闭容器中可以发生氨气的分解反应,达平衡后,仅改变下表中反应条件x,下列各项中y随x的增大而增大的是bc(选填序号).
| 选项 | a | b | c | d |
| x | 温度 | 温度 | 加入H2的物质的量 | 加入氨气的物质的量 |
| y | 混合气体的平均相对分子质量 | 平衡常数K | 混合气体的密度 | 达平衡时氨气的转化率 |
①像中T2和T1的关系是:T2低于T1(填“高于”“低于”“等于”“无法确定”).
②a、b、c三点中,N2转化率最高的是c(填字母).
③若容器容积为1L,T2℃在起始体系中加入1mol N2,3molH2,经过5min反应达到平衡时H2的转化率为60%,则NH3的反应速率为0.24mol.L-1.min-1.保持容器体积不变,若起始时向容器内放入2mol N2和6mol H2,达平衡后放出的热量为Q,则Q>110.88kJ(填“>”、“<”或“=”).
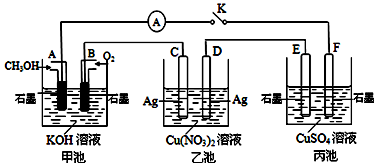
 如图是用自来水制备蒸馏水的实验装置图.
如图是用自来水制备蒸馏水的实验装置图.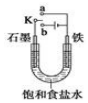 某课外活动小组同学用如图装置进行实验,试回答下列问题
某课外活动小组同学用如图装置进行实验,试回答下列问题
 氨气是一种重要的化工产品,是生产铵盐、尿素等的原料.工业合成氨的反应如下:N2(g)+3H2(g)$?_{高温高压}^{催化剂}$ 2NH3(g)△H=-92.4kJ•mol-1
氨气是一种重要的化工产品,是生产铵盐、尿素等的原料.工业合成氨的反应如下:N2(g)+3H2(g)$?_{高温高压}^{催化剂}$ 2NH3(g)△H=-92.4kJ•mol-1 $→_{键断裂}^{498J/mol}$
$→_{键断裂}^{498J/mol}$ +
+ $→_{键断裂}^{946kJ/mol}$
$→_{键断裂}^{946kJ/mol}$ +
+