6.CO和H2在一定条件下可以合成甲醇:CO(g)+2H2(g)?CH3OH中能说明上述反应在一定条件下一定达到最大限度的是( )
| A. | 反应物全部转化为甲醇 | |
| B. | 正反应和逆反应的化学反应速率均为零 | |
| C. | 反应体系中甲醇的百分含量不再变化 | |
| D. | CO和H2以1:1的物质的量之比反应生成甲醉 |
5. 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂.请填写下列空白:
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶内颜色变化.直到因加入一滴盐酸后,溶液由黄色变为橙色,并半分钟内不褪色为止.
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是D
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则起始读数为0.10mL,终点读数为25.10mL.
(4)某学生根据3次实验分别记录有关数据如表:
依据上表数据列式计算该NaOH溶液的物质的量浓度为0.1040 mol/L.(保留四位有效数字)
 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂.请填写下列空白:(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶内颜色变化.直到因加入一滴盐酸后,溶液由黄色变为橙色,并半分钟内不褪色为止.
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是D
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则起始读数为0.10mL,终点读数为25.10mL.
(4)某学生根据3次实验分别记录有关数据如表:
| 滴定次数 | 待测NaOH溶液的体积/mL | 0.100 0mol/L盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.10 | 26.11 | 26.01 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.32 | 26.31 | 25.99 |
4.已知工业上真空炼铷的反应方程式为:2RbCl+Mg $\stackrel{熔融}{?}$MgCl2+2Rb(g),对于此反应,能够进行正确解释的是( )
| A. | 铷比镁金属性强 | |
| B. | 氯化镁比氯化铷难溶 | |
| C. | 高温下,镁离子得电子能力比铷离子弱 | |
| D. | 铷的沸点比镁低,当把铷蒸气抽走时,平衡向右反应方向移动 |
3.已知:2SO2(g)+O2(g)?2SO3(g)△H=-196kJ/mol.某温度下,向一体积为2L的密闭容器中充入0.2molSO2和0.1molO2,5min后达到平衡,共放出热量11.76kJ,下列说法正确的是( )
| A. | 5min内用O2表示的反应速率为0.12mol/(L•min) | |
| B. | 加入催化剂,可使该反应的化学反应速率加快,△H变小 | |
| C. | SO2的平衡浓度为0.12mol/L | |
| D. | 达到平衡时,若增大容器的体积,则该反应的化学反应速率减慢 |
2.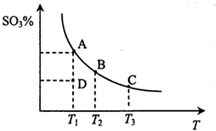 工业生产硫酸中二氧化硫的催化氧化原理为2SO2(g)+O2(g)═2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示.下列说法错误的是( )
工业生产硫酸中二氧化硫的催化氧化原理为2SO2(g)+O2(g)═2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示.下列说法错误的是( )
 工业生产硫酸中二氧化硫的催化氧化原理为2SO2(g)+O2(g)═2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示.下列说法错误的是( )
工业生产硫酸中二氧化硫的催化氧化原理为2SO2(g)+O2(g)═2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示.下列说法错误的是( )| A. | 在A、B、C三点时,v(正)=v(逆),在D点时v(正)>v(逆) | |
| B. | A、B、C三点的平衡常数一定不相同 | |
| C. | 升高温度可以加快化学反应速率,有利于平衡向正反应方向移动 | |
| D. | 在一定温度下,保持容器体积不变,向平衡体系中通入稀有气体,压强增大,平衡不移动 |
1.在等温等容条件下,有下列气体反应:2A(g)+2B(g)?C(g)+3D(g).现分别从两条途径建立平衡:Ⅰ:A、B的起始浓度均为2mol/L.Ⅱ:C、D的起始浓度分别为2mol/L和6mol/L.下列叙述正确的是( )
| A. | Ⅰ和Ⅱ两途径最终达到平衡时,系统内混合气体的平均相对分子质量不同 | |
| B. | Ⅰ和Ⅱ两途径最终达到平衡时,系统内混合气体的百分组成不同 | |
| C. | 达到平衡时Ⅰ途径的VA等于Ⅱ途径的VA | |
| D. | 达到平衡后,第Ⅰ途径混合气密度为第Ⅱ途径混合气密度的$\frac{1}{2}$ |
20. 氮是地球上含量较丰富的一种元素,氮及其化合物在工农业生产、日常生活中有着重要作用.
氮是地球上含量较丰富的一种元素,氮及其化合物在工农业生产、日常生活中有着重要作用.
(1)图是1mol NO2(g)和1mol CO(g)反应生成CO2(g)和NO(g)过程中能量变化示意图,请写出NO2和CO反应的热化学方程式NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ•mol-1.
(2)在一定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g)△H<0
其化学平衡常数K与温度t的关系如表:
完成下列问题:
①比较K1、K2的大小:K1>K2(填“>”、“=”或“<”).
②判断该反应达到化学平衡状态的依据是AC(填序号).
A.2vH2(正)=3vNH3(逆)
B.3vNH3(正)=2vH2(正)
C.容器内压强保持不变
D.混合气体的密度保持不变.
 氮是地球上含量较丰富的一种元素,氮及其化合物在工农业生产、日常生活中有着重要作用.
氮是地球上含量较丰富的一种元素,氮及其化合物在工农业生产、日常生活中有着重要作用.(1)图是1mol NO2(g)和1mol CO(g)反应生成CO2(g)和NO(g)过程中能量变化示意图,请写出NO2和CO反应的热化学方程式NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ•mol-1.
(2)在一定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g)△H<0
其化学平衡常数K与温度t的关系如表:
| t/℃ | 25 | 125 | 225 | … |
| K/(mol•L-1)-2 | 4.1×106 | K1 | K2 | … |
①比较K1、K2的大小:K1>K2(填“>”、“=”或“<”).
②判断该反应达到化学平衡状态的依据是AC(填序号).
A.2vH2(正)=3vNH3(逆)
B.3vNH3(正)=2vH2(正)
C.容器内压强保持不变
D.混合气体的密度保持不变.
19.可逆反应X(g)+Y(g)?2N(g)(正反应为放热反应)从反应开始到t1 s达到平衡,在t2 s末由于条件改变,平衡被破坏,在t3 s末又建立新的平衡.图中表示上述变化过程中X和N的浓度(c)与反应时间的关系.在t2 s~t3 s之间的曲线变化是由下列哪种条件改变引起的( )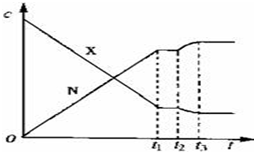

| A. | 降低温度 | B. | 增大N的浓度 | C. | 减小X的浓度 | D. | 增大压强 |
17. 反应mA(s)+nB(g)?pC(g)△H=-QkJ/mol在一定温度下B的体积分数(B%)与压强变化的关系如图所示,下列叙述中正确的是( )
反应mA(s)+nB(g)?pC(g)△H=-QkJ/mol在一定温度下B的体积分数(B%)与压强变化的关系如图所示,下列叙述中正确的是( )
①m+n<p;
②x点表示该反应的正反应速率大于逆反应速率;
③n>p;
④x点时比y点时的反应速率慢.
0 159942 159950 159956 159960 159966 159968 159972 159978 159980 159986 159992 159996 159998 160002 160008 160010 160016 160020 160022 160026 160028 160032 160034 160036 160037 160038 160040 160041 160042 160044 160046 160050 160052 160056 160058 160062 160068 160070 160076 160080 160082 160086 160092 160098 160100 160106 160110 160112 160118 160122 160128 160136 203614
 反应mA(s)+nB(g)?pC(g)△H=-QkJ/mol在一定温度下B的体积分数(B%)与压强变化的关系如图所示,下列叙述中正确的是( )
反应mA(s)+nB(g)?pC(g)△H=-QkJ/mol在一定温度下B的体积分数(B%)与压强变化的关系如图所示,下列叙述中正确的是( )①m+n<p;
②x点表示该反应的正反应速率大于逆反应速率;
③n>p;
④x点时比y点时的反应速率慢.
| A. | 只有① | B. | 只有②④ | C. | 只有①②④ | D. | 只有①和③ |