10.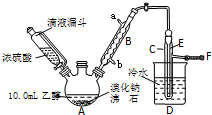 实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):
实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):
H2SO4(浓)+NaBr$\frac{\underline{\;\;△\;\;}}{\;}$NaHSO4+HBr↑
CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O.有关数据见下表:
(1)A中放入沸石的作用是防止液体瀑沸,B中进水口为b(填“a”或“b”)口.
(2)实验中用滴液漏斗代替分液漏斗的优点为平衡压强,使浓磷酸顺利流下
(3)氢溴酸与浓硫酸混合加热发生氧化还原的化学方程式为2HBr+H2SO4(浓)=Br2+SO2↑+2H2O
(4)加热A的目的是加快反应速率,蒸馏出溴乙烷,F接橡皮管导入稀NaOH溶液,其目的是吸收SO2、溴乙烷和溴蒸汽,防止防止空气污染.
(5)图中C中的导管E的末端须在水面以下,其原因是冷却并减少溴乙烷的挥发.
(6)将C中的馏出液转入锥形瓶中,边振荡边逐滴滴入浓H2SO41~2mL以除去水、乙醇等杂质,然后经过操作M,使经硫酸处理后的溴乙烷转入蒸馏瓶,加热蒸馏,收集到38~40℃的馏分约9.3g.
①操作M的名称为分液;为了控制38~40℃,加热使用水浴加热法
②从乙醇的角度考虑,本实验所得溴乙烷的产率是49.7%
(乙醇的相对分子质量为46,溴乙烷的相对分子质量为109)
 实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):
实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):H2SO4(浓)+NaBr$\frac{\underline{\;\;△\;\;}}{\;}$NaHSO4+HBr↑
CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O.有关数据见下表:
| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 深红色液体 |
| 密度/(g•cm-3) | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
(2)实验中用滴液漏斗代替分液漏斗的优点为平衡压强,使浓磷酸顺利流下
(3)氢溴酸与浓硫酸混合加热发生氧化还原的化学方程式为2HBr+H2SO4(浓)=Br2+SO2↑+2H2O
(4)加热A的目的是加快反应速率,蒸馏出溴乙烷,F接橡皮管导入稀NaOH溶液,其目的是吸收SO2、溴乙烷和溴蒸汽,防止防止空气污染.
(5)图中C中的导管E的末端须在水面以下,其原因是冷却并减少溴乙烷的挥发.
(6)将C中的馏出液转入锥形瓶中,边振荡边逐滴滴入浓H2SO41~2mL以除去水、乙醇等杂质,然后经过操作M,使经硫酸处理后的溴乙烷转入蒸馏瓶,加热蒸馏,收集到38~40℃的馏分约9.3g.
①操作M的名称为分液;为了控制38~40℃,加热使用水浴加热法
②从乙醇的角度考虑,本实验所得溴乙烷的产率是49.7%
(乙醇的相对分子质量为46,溴乙烷的相对分子质量为109)
9. 某同学用0.1082mol/L的NaOH溶液滴定未知浓度的盐酸.
某同学用0.1082mol/L的NaOH溶液滴定未知浓度的盐酸.
以下是实验数据记录表:
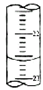
(1)请根据图(滴定管局部)读出第2次实验的末读数,填充上表中的两个空格.
(2)计算待测盐酸溶液浓度.
 某同学用0.1082mol/L的NaOH溶液滴定未知浓度的盐酸.
某同学用0.1082mol/L的NaOH溶液滴定未知浓度的盐酸.以下是实验数据记录表:
| 实验序号 | 待测盐酸溶液体积(mL) | 滴定管读数 | 消耗标准NaOH溶液的体积(mL) | |
| 初读数 | 末读数 | |||
| 1 | 20.00 | 0.00 | 19.90 | 19.90 |
| 2 | 20.00 | 0.05 | ||
(2)计算待测盐酸溶液浓度.
8.用已知浓度的NaOH溶液滴定未知浓度盐酸时,下列操作对实验结果没有影响的是( )
| A. | 锥形瓶用蒸馏水洗涤后,直接盛盐酸溶液 | |
| B. | 中和滴定将要达到滴定终点时,眼睛注视滴定管中液面的位置变化 | |
| C. | 滴定管装碱液前未用标准碱液润洗 | |
| D. | 滴定时,锥形瓶摇动太剧烈,有少量溶液溅出 |
5.食醋总酸量的测定
某实验小组拟用酸碱中和滴定法测定食醋的总酸量(CH3COOH,g/100mL).
(一)、实验用品:市售食用白醋样品500mL(商标注明:总酸量:3.5g-5g/100mL)(下称“原醋”),0.1000mol/LNaOH标准溶液,蒸馏水,0.1%甲基橙溶液、0.1%酚酞溶液;仪器自选.
(二)、实验原理:化学方程式CH3COOH+NaOH=CH3COONa+H2O
(三)、实验步骤:
(1)配制待测食醋溶液
准确量取10.00mL原醋,配制成100.00mL待测食醋溶液(下称“待测液”).完成该步骤,需要的一种定量仪器是100ml容量瓶(填仪器名称)
(2)量取一定体积的待测液
用酸式滴定管取20.00mL待测液于锥形瓶中.加1-2滴0.1%酚酞溶液做指示剂
(3)盛装标准NaOH溶液,记录为NaOH标准溶液体积的初读数.
(4)滴定操作:滴定时一手控制滴定管,一手摇动锥形瓶,眼睛观察锥形瓶内溶液颜色变化直到滴定终点.判断滴定终点的现象是由无色变为浅红色,半分钟内不褪色.
记录NaOH的终读数.重复滴定4次.
(四)、实验记录及数据处理(请完成相关填空)
(5)四次实验中明显有误差的一次是4(填编号).
(6)消耗NaOH溶液的平均值是15.00mL.
(7)待测液的浓度是0.075mol/L.
某实验小组拟用酸碱中和滴定法测定食醋的总酸量(CH3COOH,g/100mL).
(一)、实验用品:市售食用白醋样品500mL(商标注明:总酸量:3.5g-5g/100mL)(下称“原醋”),0.1000mol/LNaOH标准溶液,蒸馏水,0.1%甲基橙溶液、0.1%酚酞溶液;仪器自选.
(二)、实验原理:化学方程式CH3COOH+NaOH=CH3COONa+H2O
(三)、实验步骤:
(1)配制待测食醋溶液
准确量取10.00mL原醋,配制成100.00mL待测食醋溶液(下称“待测液”).完成该步骤,需要的一种定量仪器是100ml容量瓶(填仪器名称)
(2)量取一定体积的待测液
用酸式滴定管取20.00mL待测液于锥形瓶中.加1-2滴0.1%酚酞溶液做指示剂
(3)盛装标准NaOH溶液,记录为NaOH标准溶液体积的初读数.
(4)滴定操作:滴定时一手控制滴定管,一手摇动锥形瓶,眼睛观察锥形瓶内溶液颜色变化直到滴定终点.判断滴定终点的现象是由无色变为浅红色,半分钟内不褪色.
记录NaOH的终读数.重复滴定4次.
(四)、实验记录及数据处理(请完成相关填空)
| 滴定次数 实验数据 | 1 | 2 | 3 | 4 |
| V(待测液)/mL | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)/mL(初读数) | 0.00 | 0.200 | 0.10 | 0.00 |
| V(NaOH)/mL(终读数) | 14.95 | 15.20 | 15.15 | 16.95 |
| V(NaOH)/mL(消耗) | 14.95 | 15.00 | 15.05 | 16.95 |
(6)消耗NaOH溶液的平均值是15.00mL.
(7)待测液的浓度是0.075mol/L.
4. 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:①碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中;②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:①碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中;②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂恰好变色,且半分钟不变化,测得所耗盐酸的体积为V1mL;
④重复以上过程,但滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.
(1)锥形瓶中的溶液从红色变为无色时,停止滴定.
(2)滴定时边滴边摇动锥形瓶,眼睛应注视锥形瓶内容液颜色变化;
(3)该小组在步骤①中的错误是锥形瓶不能用待测液润洗,由此造成的测定结果偏高(填偏高、偏低或无影响);
(4)步骤②缺少的操作是用标准液润洗滴定管;
(5)如图,是某次滴定时的滴定管中的液面,其读数为22.60mL;
(6)根据下列数据:
请计算待测烧碱溶液的浓度为0.08 mol/L.
0 159919 159927 159933 159937 159943 159945 159949 159955 159957 159963 159969 159973 159975 159979 159985 159987 159993 159997 159999 160003 160005 160009 160011 160013 160014 160015 160017 160018 160019 160021 160023 160027 160029 160033 160035 160039 160045 160047 160053 160057 160059 160063 160069 160075 160077 160083 160087 160089 160095 160099 160105 160113 203614
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:①碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中;②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:①碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中;②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂恰好变色,且半分钟不变化,测得所耗盐酸的体积为V1mL;
④重复以上过程,但滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.
(1)锥形瓶中的溶液从红色变为无色时,停止滴定.
(2)滴定时边滴边摇动锥形瓶,眼睛应注视锥形瓶内容液颜色变化;
(3)该小组在步骤①中的错误是锥形瓶不能用待测液润洗,由此造成的测定结果偏高(填偏高、偏低或无影响);
(4)步骤②缺少的操作是用标准液润洗滴定管;
(5)如图,是某次滴定时的滴定管中的液面,其读数为22.60mL;
(6)根据下列数据:
| 滴定次数 | 待测液体(mL) | 标准盐酸体积(mL) | |
| 滴定前读(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 4.00 | 24.10 |
 某学生为测定未知浓度的硫酸溶液,进行如下实验:用1.00mL待测硫酸溶液配制100mL稀H2SO4溶液;以0.14mol•L-1的NaOH溶液滴定上述稀H2SO4 25.00mL,滴定终止时消耗NaOH溶液15.00mL.
某学生为测定未知浓度的硫酸溶液,进行如下实验:用1.00mL待测硫酸溶液配制100mL稀H2SO4溶液;以0.14mol•L-1的NaOH溶液滴定上述稀H2SO4 25.00mL,滴定终止时消耗NaOH溶液15.00mL.