10.环己酮是重要的化工原料,也是重要的工业溶剂.实验室制备环己酮的原理、有关数据及装置示意图如图:
反应原理:如图1所示
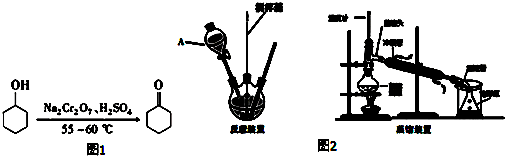
反应放热,温度过高或者重铬酸钠过量会进一步氧化.
主要物料及产物的物理参数:
实验装置:
如图2所示
实验步骤:
Ⅰ.投料:在100mL三颈烧瓶中加入20mL水,慢慢加入5mL浓硫酸摇动,振荡下缓慢加入5mL(4.8g,0.048mol)环己醇,并将混合液温度降至30℃以下.将5g(0.019mol)重铬酸钠溶于水得橙红色溶液备用.
Ⅱ.反应:将约$\frac{1}{5}$的重铬酸钠溶液加入三颈烧瓶中,充分搅拌使之混合均匀.冷水浴冷却,控制反应温度在55~60℃.待橙红色消失后,再将剩余的重铬酸钠溶液分四次加入到三颈烧瓶中.当温度自动下降时,加入4mL甲醇使反应液完全变成墨绿色(三价铬);
Ⅲ.蒸馏:在反应瓶中加入30mL水,并改为蒸馏装置,收集90~99℃之间的馏分(环己酮与水的共沸物)至无油珠为止;
Ⅳ.萃取、干燥:将馏出液用食盐饱和后转入分液漏斗中,分出有机层.水层用8mL乙醚提取一次,将乙醚提取液和有机层合并,用无水硫酸镁干燥; 5.蒸馏,收集环己酮产品2.6g. 请回答下列问题:
(1)装置A的名称是分液漏斗.
(2)完成并配平反应方程式:
3 +1 Na2Cr2O7+4H2SO4→3
+1 Na2Cr2O7+4H2SO4→3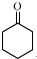 +1 Na2SO4+1 Cr2(SO4)3+7 H2O
+1 Na2SO4+1 Cr2(SO4)3+7 H2O
(3)反应过程中加入甲醇后有无色气体生成.加入甲醇的作用是将过量的重铬酸钠还原,防止环己酮继续被氧化,请用离子方程式表示反应原理CH3OH+Cr2O72-+8H+→CO2↑+2Cr3++6H2O.
(4)步骤4向馏出液加入食盐的目的是利用盐析原理,减少环己酮在水中的溶解度,有利于分层,将乙醚提取液和有机层合并的原因是减少环己酮在水中溶解造成的损失.
(5)计算所得产品的产率55.3%.(保留三位有效数字)
反应原理:如图1所示

反应放热,温度过高或者重铬酸钠过量会进一步氧化.
主要物料及产物的物理参数:
| 名称 | 性状 | 密度 | 溶点℃ | 沸点℃ | 溶解度 | |
| 水 | 乙醚 | |||||
| 环已醇 | 无色,有刺激性气味 | 0.9624 | 25.93 | 161.5 | 5.67g/100mL | ∞ |
| 环已酮 | 无色,有刺激性气味 | 0.9478 | - | 155.7 | 2.4g/100mL | ∞ |
如图2所示
实验步骤:
Ⅰ.投料:在100mL三颈烧瓶中加入20mL水,慢慢加入5mL浓硫酸摇动,振荡下缓慢加入5mL(4.8g,0.048mol)环己醇,并将混合液温度降至30℃以下.将5g(0.019mol)重铬酸钠溶于水得橙红色溶液备用.
Ⅱ.反应:将约$\frac{1}{5}$的重铬酸钠溶液加入三颈烧瓶中,充分搅拌使之混合均匀.冷水浴冷却,控制反应温度在55~60℃.待橙红色消失后,再将剩余的重铬酸钠溶液分四次加入到三颈烧瓶中.当温度自动下降时,加入4mL甲醇使反应液完全变成墨绿色(三价铬);
Ⅲ.蒸馏:在反应瓶中加入30mL水,并改为蒸馏装置,收集90~99℃之间的馏分(环己酮与水的共沸物)至无油珠为止;
Ⅳ.萃取、干燥:将馏出液用食盐饱和后转入分液漏斗中,分出有机层.水层用8mL乙醚提取一次,将乙醚提取液和有机层合并,用无水硫酸镁干燥; 5.蒸馏,收集环己酮产品2.6g. 请回答下列问题:
(1)装置A的名称是分液漏斗.
(2)完成并配平反应方程式:
3
 +1 Na2Cr2O7+4H2SO4→3
+1 Na2Cr2O7+4H2SO4→3 +1 Na2SO4+1 Cr2(SO4)3+7 H2O
+1 Na2SO4+1 Cr2(SO4)3+7 H2O(3)反应过程中加入甲醇后有无色气体生成.加入甲醇的作用是将过量的重铬酸钠还原,防止环己酮继续被氧化,请用离子方程式表示反应原理CH3OH+Cr2O72-+8H+→CO2↑+2Cr3++6H2O.
(4)步骤4向馏出液加入食盐的目的是利用盐析原理,减少环己酮在水中的溶解度,有利于分层,将乙醚提取液和有机层合并的原因是减少环己酮在水中溶解造成的损失.
(5)计算所得产品的产率55.3%.(保留三位有效数字)
9.苯甲酸广泛应用于制药和化工行业.某同学尝试用甲苯的氧化反应制备苯甲酸.反应原理:
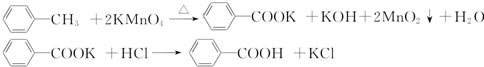
实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如图流程分离出苯甲酸和回收未反应的甲苯.
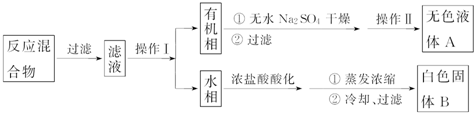
已知:苯甲酸分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;纯净固体有机物一般都有固定熔点.
(1)操作Ⅰ为分液,操作Ⅱ为蒸馏.
(2)无色液体A是甲苯,定性检验A的试剂是酸性KMnO4溶液,现象是溶液褪色.
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔.该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如表方案进行提纯和检验,实验结果表明推测正确.请在完成表中内容.
(4)纯度测定:称取1.220g产品溶解在甲醇中,配成100mL甲醇溶液,移取25.00mL溶液,滴定,消耗KOH的物质的量为2.40×10-3 mol,产品中苯甲酸的质量分数为96%(保留二位有效数字).(注:苯甲酸的相对分子质量为122)

实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如图流程分离出苯甲酸和回收未反应的甲苯.

已知:苯甲酸分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;纯净固体有机物一般都有固定熔点.
(1)操作Ⅰ为分液,操作Ⅱ为蒸馏.
(2)无色液体A是甲苯,定性检验A的试剂是酸性KMnO4溶液,现象是溶液褪色.
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔.该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如表方案进行提纯和检验,实验结果表明推测正确.请在完成表中内容.
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将白色固体B加入水中,加热溶解,冷却结晶,过滤 | 得到白色晶体和无色滤液 | |
| ② | 取少量滤液于试管中,滴入稀HNO3酸化的AgNO3溶液 | 生成白色沉淀 | 滤液含Cl- |
| ③ | 干燥白色晶体,取适量加热,测定熔点 | 白色晶体在122.4℃熔化为液体 | 白色晶体是苯甲酸 |
7.某化学小组为探究草酸的性质并制备草酸钠及其用途,查阅到如表信息:
探究草酸部分性质并制备草酸钠的生产流程如表:
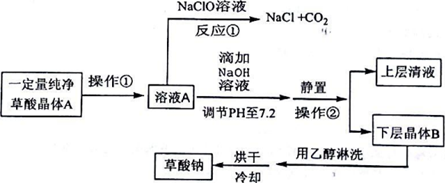
请回答下列问题:
(1)写出反应①的化学方程式H2C2O4+NaC1O=NaC1+2CO2↑+H2O.表明草酸具有还原性.
(2)向溶液A中加入NaOH溶液,开始滴加速度要尽量快些.其目的是利用中和反应放热,升温促进反应(或增大反应速率).该反应达到终点时的化学方程式为H2C2O4+2NaOH=Na2C2O4↓+2H2O.
(3)操作②的名称是过滤.用乙醇淋洗晶体B的目的是除去晶体表面水分减少损失
(4)用0.01000mol/L的高锰酸钾溶液滴定25.00mL某浓度的草酸钠溶液时.需要加入适量的稀硫酸,所发生反应为:5C2O42-+2MnO4-+16H+═2Mn2++10CO2↑+8H2O,若硫酸加入太多,结果会草酸根会生成草酸氢根和草酸,使溶液中草酸根离子浓度降低,减慢反应速率:操作中需用酸式演定管(填“酸式”或“碱式”),当达到反应终点时的现象是溶液呈现浅紫色且30s内不褪色;测得此时消耗上述高锰酸钾溶液20.00mL,则该草酸钠溶液浓度为0.0200mol/L.
| H2C2O4 | 无色晶体 | K1=5.9×10-2,K2=6.4×10-5,能溶于水和乙醇 |
| Na2C2O4 | 白色晶体 | 微溶于水,pH=7.2,不溶于乙醇 |

请回答下列问题:
(1)写出反应①的化学方程式H2C2O4+NaC1O=NaC1+2CO2↑+H2O.表明草酸具有还原性.
(2)向溶液A中加入NaOH溶液,开始滴加速度要尽量快些.其目的是利用中和反应放热,升温促进反应(或增大反应速率).该反应达到终点时的化学方程式为H2C2O4+2NaOH=Na2C2O4↓+2H2O.
(3)操作②的名称是过滤.用乙醇淋洗晶体B的目的是除去晶体表面水分减少损失
(4)用0.01000mol/L的高锰酸钾溶液滴定25.00mL某浓度的草酸钠溶液时.需要加入适量的稀硫酸,所发生反应为:5C2O42-+2MnO4-+16H+═2Mn2++10CO2↑+8H2O,若硫酸加入太多,结果会草酸根会生成草酸氢根和草酸,使溶液中草酸根离子浓度降低,减慢反应速率:操作中需用酸式演定管(填“酸式”或“碱式”),当达到反应终点时的现象是溶液呈现浅紫色且30s内不褪色;测得此时消耗上述高锰酸钾溶液20.00mL,则该草酸钠溶液浓度为0.0200mol/L.
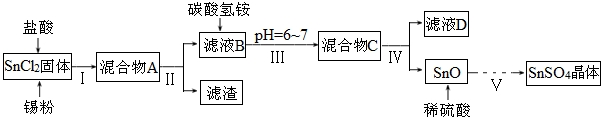
6.硝酸铜是常用的一种无机化学试剂
(1)工业上以粗铜为原料采取如图1所示流程制备硝酸铜晶体:

①在步骤a中,还需要通入氧气和水,其目的是将NOx转化为硝酸,提高原料的利用率,减少污染物的排放
②在保温去铁的过程中,为使Fe3+沉淀完全,可以向溶液中加入CuO调节溶液的pH,根据下表数据,溶液的pH应保持在3.2--4.7范围
③在滤液蒸发浓缩步骤中,适当加入稀硝酸的作用是抑制加热过程中Cu2+的水解
(2)某研究学习小组将一定质量的硝酸铜晶体【Cu(NO3)2.6H2O】放在坩埚中加热,在不同温度阶段进行质量分析,绘制出剩余固体质量分数与温度关系如图2所示.据图回答下列问题:
①当温度27℃<T<120℃时,反应的化学方程式为Cu(NO3)2•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$Cu(NO3)2•3H2O+3H2O
②剩余固体质量为38.4g时,固体成分为【Cu(NO3)2•2Cu(OH)2】当温度120℃<T<800℃时,反应的化学方程式为3Cu(NO3)2•3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Cu(NO3)2•2Cu(OH)2+4NO2↑+O2↑+7H2O (此温度下,HNO3也分解)
③当剩余固体质量为21.6g时,固体的化学式为Cu2O
(3)制备无水硝酸铜的方法之一是用Cu与液态N2O4反应,反应过程
中有无色气体放出,遇到空气变红棕色.反应的化学方程式是Cu+2N2O4=Cu(NO3)2+2NO↑.
(1)工业上以粗铜为原料采取如图1所示流程制备硝酸铜晶体:

①在步骤a中,还需要通入氧气和水,其目的是将NOx转化为硝酸,提高原料的利用率,减少污染物的排放
②在保温去铁的过程中,为使Fe3+沉淀完全,可以向溶液中加入CuO调节溶液的pH,根据下表数据,溶液的pH应保持在3.2--4.7范围
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
(2)某研究学习小组将一定质量的硝酸铜晶体【Cu(NO3)2.6H2O】放在坩埚中加热,在不同温度阶段进行质量分析,绘制出剩余固体质量分数与温度关系如图2所示.据图回答下列问题:
①当温度27℃<T<120℃时,反应的化学方程式为Cu(NO3)2•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$Cu(NO3)2•3H2O+3H2O
②剩余固体质量为38.4g时,固体成分为【Cu(NO3)2•2Cu(OH)2】当温度120℃<T<800℃时,反应的化学方程式为3Cu(NO3)2•3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Cu(NO3)2•2Cu(OH)2+4NO2↑+O2↑+7H2O (此温度下,HNO3也分解)
③当剩余固体质量为21.6g时,固体的化学式为Cu2O
(3)制备无水硝酸铜的方法之一是用Cu与液态N2O4反应,反应过程
中有无色气体放出,遇到空气变红棕色.反应的化学方程式是Cu+2N2O4=Cu(NO3)2+2NO↑.
5.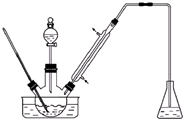 实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见图,相关物质的物理性质见附表).
实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见图,相关物质的物理性质见附表).
其实验步骤为:
步骤1:将三颈瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛(5.3g)充分混合后,升温至60℃,缓慢滴加经浓硫酸干燥过的液溴,保温反应一段时间,冷却.
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液.有机相用10%NaHCO3溶液洗涤.
步骤3:经洗涤的有机相加入适量无水硫酸钙固体,放置一段时间后过滤.
步骤4:为了防止间溴苯甲醛因温度过高被氧化,把步骤3处理得到的间溴苯甲醛加入少量锌粉,同时采用某种技术,收集相应馏分,其中收集到间溴苯甲醛为3.7g.
(1)实验装置中采用的加热方式为水浴加热,冷凝管的作用为导气、冷凝回流,锥形瓶中的试剂应为NaOH.
(2)步骤1所加入的无水AlCl3的作用为催化剂.
(3)步骤2中用10%NaHCO3溶液洗涤有机相,是为了除去溶于有机相的Br2、HCl(填化学式).
(4)步骤3中加入的无水硫酸钙固体的目的是除去有机相的水.
(5)步骤4中,某种技术为减压蒸馏.
(6)本实验所得到的间溴苯甲醛产率是40.0%.
 实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见图,相关物质的物理性质见附表).
实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见图,相关物质的物理性质见附表).| 相对分 子质量 | 密度 /(g•cm-3) | 沸点/℃ | |
| 溴 | 160 | 3.119 | 58.8 |
| 苯甲醛 | 106 | 1.04 | 179 |
| 1,2-二氯乙烷 | 99 | 1.2351 | 83.5 |
| 间溴苯甲醛 | 185 | 1.587 | 229 |
步骤1:将三颈瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛(5.3g)充分混合后,升温至60℃,缓慢滴加经浓硫酸干燥过的液溴,保温反应一段时间,冷却.
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液.有机相用10%NaHCO3溶液洗涤.
步骤3:经洗涤的有机相加入适量无水硫酸钙固体,放置一段时间后过滤.
步骤4:为了防止间溴苯甲醛因温度过高被氧化,把步骤3处理得到的间溴苯甲醛加入少量锌粉,同时采用某种技术,收集相应馏分,其中收集到间溴苯甲醛为3.7g.
(1)实验装置中采用的加热方式为水浴加热,冷凝管的作用为导气、冷凝回流,锥形瓶中的试剂应为NaOH.
(2)步骤1所加入的无水AlCl3的作用为催化剂.
(3)步骤2中用10%NaHCO3溶液洗涤有机相,是为了除去溶于有机相的Br2、HCl(填化学式).
(4)步骤3中加入的无水硫酸钙固体的目的是除去有机相的水.
(5)步骤4中,某种技术为减压蒸馏.
(6)本实验所得到的间溴苯甲醛产率是40.0%.
4.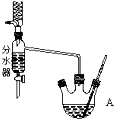 实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如表:
实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如表:
操作如下:
①在50mL三颈烧瓶中投入几粒沸石,将18.5mL正丁醇和13.4mL冰醋酸(过量),3~4滴浓硫酸按一定顺序均匀混合,安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管.
②将分水器分出的酯层和反应液一起倒入分液漏斗中依次用水洗,10% Na2CO3洗,再水洗,最后转移至锥形瓶并干燥.
③将干燥后的乙酸正丁酯加入烧瓶中,常压蒸馏,收集馏分,得15.1g乙酸正丁酯.
请回答有关问题:
(1)写出任意一种正丁醇同类的同分异构体的结构简式CH3CH2CH(OH)CH3.
(2)仪器A中发生反应的化学方程式为CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O.
(3)步骤①向三颈烧瓶中依次加入的药品是:正丁醇,浓硫酸,冰醋酸.
(4)步骤②中,用 10%Na2CO3溶液洗涤有机层,该步操作的目的是除去酯中混有的乙酸和正丁醇.
(5)步骤③在进行蒸馏操作时,若从118℃开始收集馏分,产率偏高,(填“高”或“低”)原因是会收集到少量未反应的冰醋酸和正丁醇.
(6)该实验生成的乙酸正丁酯的产率是65%.
 实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如表:
实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如表:| 化合物 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解度g/l00g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
①在50mL三颈烧瓶中投入几粒沸石,将18.5mL正丁醇和13.4mL冰醋酸(过量),3~4滴浓硫酸按一定顺序均匀混合,安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管.
②将分水器分出的酯层和反应液一起倒入分液漏斗中依次用水洗,10% Na2CO3洗,再水洗,最后转移至锥形瓶并干燥.
③将干燥后的乙酸正丁酯加入烧瓶中,常压蒸馏,收集馏分,得15.1g乙酸正丁酯.
请回答有关问题:
(1)写出任意一种正丁醇同类的同分异构体的结构简式CH3CH2CH(OH)CH3.
(2)仪器A中发生反应的化学方程式为CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O.
(3)步骤①向三颈烧瓶中依次加入的药品是:正丁醇,浓硫酸,冰醋酸.
(4)步骤②中,用 10%Na2CO3溶液洗涤有机层,该步操作的目的是除去酯中混有的乙酸和正丁醇.
(5)步骤③在进行蒸馏操作时,若从118℃开始收集馏分,产率偏高,(填“高”或“低”)原因是会收集到少量未反应的冰醋酸和正丁醇.
(6)该实验生成的乙酸正丁酯的产率是65%.
3.丙烯酸甲酯是一种重要的工业原料,某实验小组制取丙烯酸甲酯的装置如图所示.
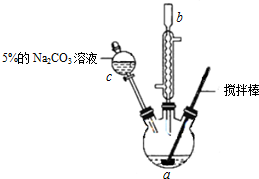
Ⅰ.实验步骤如下:
①向三颈瓶中依次加入:10.0mL丙烯酸(CH2=CHCOOH)、适量的浓硫酸、10.0mL无水甲醇、
2粒沸石,按图示装置连接好冷凝管,用搅拌棒搅拌,水浴加热.
②充分反应后,冷却,向混合液中加入5% Na2CO3溶液洗至中性.
③分液,取上层油状液体,再用无水Na2SO4干燥后蒸馏,收集70℃~90℃馏分.
可能用到的信息:
请回答下列问题:
(1)仪器c的名称是分液漏斗.
(2)混合液用5% Na2CO3溶液洗涤的作用是除去丙烯酸、浓硫酸等酸性物质.
(3)该实验中应采用的安全防护措施有通风橱中实验.(1条即可)
Ⅱ.为测定上述反应中丙烯酸甲酯的产率,设计如下实验:
①将油状物质提纯后平均分成5份,取出1份置于锥形瓶中,加入2.5mol/L的KOH溶液10.0mL,加热使之完全水解.
②用酚酞做指示剂,向冷却后的溶液中滴加0.5mol/L的HCl溶液,中和过量的KOH,滴到终点时共消耗盐酸20.00mL.
(4)请写出(Ⅱ)操作①中发生的化学反应方程式CH2=CHCOOCH3+KOH$\stackrel{△}{→}$CH2=CHCOOK+CH3OH.
(5)计算本次酯化反应丙烯酸甲酯的产率.

Ⅰ.实验步骤如下:
①向三颈瓶中依次加入:10.0mL丙烯酸(CH2=CHCOOH)、适量的浓硫酸、10.0mL无水甲醇、
2粒沸石,按图示装置连接好冷凝管,用搅拌棒搅拌,水浴加热.
②充分反应后,冷却,向混合液中加入5% Na2CO3溶液洗至中性.
③分液,取上层油状液体,再用无水Na2SO4干燥后蒸馏,收集70℃~90℃馏分.
可能用到的信息:
| 密度 | 沸点 | 溶解性 | ||
| 丙烯酸 | 1.05g/cm3 | 141℃ | 与水互溶,易溶于有机溶剂 | 有毒 |
| 甲醇 | 0.79g/cm3 | 64.7℃ | 与水互溶,易溶于有机溶剂 | 易挥发,有毒 |
| 丙烯酸甲酯 | 0.95g/cm3 | 80.5℃ | 难溶于水,易溶于有机溶剂 | 易挥发 |
(1)仪器c的名称是分液漏斗.
(2)混合液用5% Na2CO3溶液洗涤的作用是除去丙烯酸、浓硫酸等酸性物质.
(3)该实验中应采用的安全防护措施有通风橱中实验.(1条即可)
Ⅱ.为测定上述反应中丙烯酸甲酯的产率,设计如下实验:
①将油状物质提纯后平均分成5份,取出1份置于锥形瓶中,加入2.5mol/L的KOH溶液10.0mL,加热使之完全水解.
②用酚酞做指示剂,向冷却后的溶液中滴加0.5mol/L的HCl溶液,中和过量的KOH,滴到终点时共消耗盐酸20.00mL.
(4)请写出(Ⅱ)操作①中发生的化学反应方程式CH2=CHCOOCH3+KOH$\stackrel{△}{→}$CH2=CHCOOK+CH3OH.
(5)计算本次酯化反应丙烯酸甲酯的产率.
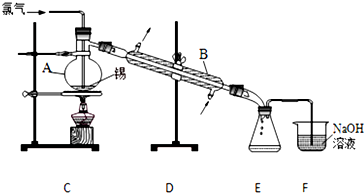
2.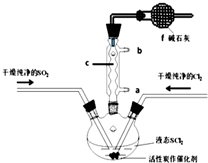 SOCl2是一种液态化合物,沸点为77℃,在农药、制药行业中用途广泛.SOCl2遇水剧烈反应,液面上产生白雾,并带有刺激性气味的气体产生.实验室合成原理:SO2+Cl2+SCl2=2SOCl2,部分装置如图所示,回答以下问题:
SOCl2是一种液态化合物,沸点为77℃,在农药、制药行业中用途广泛.SOCl2遇水剧烈反应,液面上产生白雾,并带有刺激性气味的气体产生.实验室合成原理:SO2+Cl2+SCl2=2SOCl2,部分装置如图所示,回答以下问题:
(1)装置f的作用是吸收逸出有毒的Cl2、SO2,防止空气中的水蒸气进入反应装置,防止SOCl2水解.
(2)实验室制Cl2的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(3)SOCl2与水反应的化学方程式为SOCl2+H2O=SO2↑+2HCl↑.蒸干AlCl3溶液不能得到无水AlCl3,但使SOCl2与AlCl3•6H2O混合加热,可得到无水AlCl3,试解释原因:AlCl3溶液易水解,AlCl3•6H2O与SOCl2混合加热,SOCl2与AlCl3•6H2O中的结晶水作用,生成无水AlCl3及SO2和HCl气体,SOCl2吸水,产物SO2和HCl抑制AlCl3水解;
(4)下列四种制备SO2的方案中最佳选择是丁
(5)试验结束后,将三颈烧瓶中液体混合物分离开的实验操作是蒸馏(填操作名称,已知SCl2的沸点为50℃).若反应中消耗的Cl2的体积为896ml(已转化为标准状况,SO2足量),最后得到纯净的SOCl2 4.76g,则SOCl2的产率为50%
(6)分离产物后,向获得的SOCl2中加入足量NaOH溶液,振荡、静止得到无色溶液w,检验溶液w中存在的Cl-的方法是取少量无色溶液放入试管中,加入Ba(NO3)2溶液至不再生沉淀为止,静置,取出上层清液,加入AgNO3溶液,有白色沉淀生成,可知无色溶液中含有Cl-.
0 159917 159925 159931 159935 159941 159943 159947 159953 159955 159961 159967 159971 159973 159977 159983 159985 159991 159995 159997 160001 160003 160007 160009 160011 160012 160013 160015 160016 160017 160019 160021 160025 160027 160031 160033 160037 160043 160045 160051 160055 160057 160061 160067 160073 160075 160081 160085 160087 160093 160097 160103 160111 203614
 SOCl2是一种液态化合物,沸点为77℃,在农药、制药行业中用途广泛.SOCl2遇水剧烈反应,液面上产生白雾,并带有刺激性气味的气体产生.实验室合成原理:SO2+Cl2+SCl2=2SOCl2,部分装置如图所示,回答以下问题:
SOCl2是一种液态化合物,沸点为77℃,在农药、制药行业中用途广泛.SOCl2遇水剧烈反应,液面上产生白雾,并带有刺激性气味的气体产生.实验室合成原理:SO2+Cl2+SCl2=2SOCl2,部分装置如图所示,回答以下问题:(1)装置f的作用是吸收逸出有毒的Cl2、SO2,防止空气中的水蒸气进入反应装置,防止SOCl2水解.
(2)实验室制Cl2的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(3)SOCl2与水反应的化学方程式为SOCl2+H2O=SO2↑+2HCl↑.蒸干AlCl3溶液不能得到无水AlCl3,但使SOCl2与AlCl3•6H2O混合加热,可得到无水AlCl3,试解释原因:AlCl3溶液易水解,AlCl3•6H2O与SOCl2混合加热,SOCl2与AlCl3•6H2O中的结晶水作用,生成无水AlCl3及SO2和HCl气体,SOCl2吸水,产物SO2和HCl抑制AlCl3水解;
(4)下列四种制备SO2的方案中最佳选择是丁
| 方案 | 甲 | 乙 | 丙 | 丁 |
| 发生装置 | 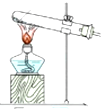 |  | 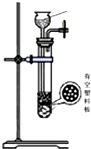 | 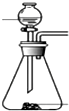 |
| 所选试剂 | NaHSO3固体 | 18.4mol/LH2SO4+Cu | 4mol/LHNO3+Na2SO | 70%H2SO4+K2SO3 |
(6)分离产物后,向获得的SOCl2中加入足量NaOH溶液,振荡、静止得到无色溶液w,检验溶液w中存在的Cl-的方法是取少量无色溶液放入试管中,加入Ba(NO3)2溶液至不再生沉淀为止,静置,取出上层清液,加入AgNO3溶液,有白色沉淀生成,可知无色溶液中含有Cl-.

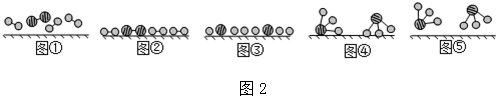
 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和③的含义分别是N2、H2被吸附在催化剂表面、在催化剂表面,N2、H2中化学键断裂.
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和③的含义分别是N2、H2被吸附在催化剂表面、在催化剂表面,N2、H2中化学键断裂.