17.通过以下反应均可获取H2.下列有关说法正确的是( )
①太阳光催化分解水制氢:2H2O(l)═2H2(g)+O2(g)△H1=+571.6kJ•mol-1
②焦炭与水反应制氢:C(s)+H2O(g)═CO(g)+H2(g)△H2=+131.3kJ•mol-1
③甲烷与水反应制氢:CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=+206.1kJ•mol-1.
①太阳光催化分解水制氢:2H2O(l)═2H2(g)+O2(g)△H1=+571.6kJ•mol-1
②焦炭与水反应制氢:C(s)+H2O(g)═CO(g)+H2(g)△H2=+131.3kJ•mol-1
③甲烷与水反应制氢:CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=+206.1kJ•mol-1.
| A. | 反应①中电能转化为化学能 | |
| B. | 反应②为放热反应 | |
| C. | 反应③使用催化剂,△H3减小 | |
| D. | 反应CH4(g)=C(s)+2H2(g)的△H=+74.8 kJ•mol-1 |
15.跟氨分子所含的质子总数和电子总数都相同的粒子是( )
| A. | Na+ | B. | Mg2+ | C. | HCl | D. | HF |
14.下列物质能用于制造光导纤维的是( )
| A. | 钢 | B. | 陶瓷 | C. | 玻璃 | D. | 二氧化硅 |
13.图是炭和水蒸汽发生反应生成CO、H2的途径和三个状态的能量,该反应为吸热反应.下列说法不正确的是( )


| A. | 步骤1为吸热反应,步骤2为放热反应 | |
| B. | E2>E3>E1 | |
| C. | 1mol C发生该反应时吸收的能量为E3-E1 | |
| D. | E2-E1<E2-E3 |
12.下列说法正确的是( )
| A. | 任何条件下,反应2CO2(g)═2CO(g)+O2(g)均不能自发进行 | |
| B. | 依据反应I2+2S2O32-═2I-+S4O62-,若要测定平衡体系I2+I-?I3-中平衡时的 c(I2),可用已知物质的量浓度的Na2S2O3溶液进行滴定实验 | |
| C. | 向含有苯酚的苯溶液中滴入少量浓溴水未见白色沉淀,是因为生成的三溴苯酚又溶于苯中 | |
| D. | 检验某物质是否含有Fe2O3的操作步骤是:样品粉碎→加水溶解→过滤,向滤液中滴加KSCN溶液 |
11.已知:H2O(g)═H2O(l)△H=Q1 kJ•mol-1
C2H5OH(g)═C2H5OH(l)△H=Q2 kJ•mol-1
C2H5OH(g)+3O2(g)═2CO2(g)+3H2O(g)△H=Q3 kJ•mol-1
若使46g酒精液体完全燃烧,最后恢复到室温,则放出的热量为( )
C2H5OH(g)═C2H5OH(l)△H=Q2 kJ•mol-1
C2H5OH(g)+3O2(g)═2CO2(g)+3H2O(g)△H=Q3 kJ•mol-1
若使46g酒精液体完全燃烧,最后恢复到室温,则放出的热量为( )
| A. | (Q1+Q2+Q3) kJ | B. | 0.5(Q+Q2+Q3) kJ | ||
| C. | (0.5Q1-1.5Q2+0.5Q3) kJ | D. | -(3Q1-Q2+Q3) kJ |
10.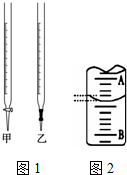 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①取一支图1所示仪器,用蒸馏水洗净,即加入待测的NaOH溶液,
使尖嘴部分充满溶液,并调整液面处于“0“刻度以下的位置,记下读数;
②取锥形瓶用蒸馏水洗净,精确量取一定量的0.1000mol•L-1标准盐酸;
③加入3滴酚酞试液,摇匀;
④进行滴定实验,并记录数据.
⑤重复以上步骤2次.
回答下列问题:
(1)步骤①中应将NaOH溶液注入图中的碱式滴定管(填仪器名称)中.
(2)在步骤①中存在的明显错误是滴定管没有用待测NaOH溶液润洗,由此会使测定结果偏低(选填“偏高”、“偏低”或“无影响”).
(3)图2是某次实验中液面位置示意图,若A与B刻度间相差1mL,A处的刻度为19,滴定管中液面读数应为19.40mL.
(4)操作④中左手轻轻挤压玻璃球,右手振荡锥形瓶,眼睛注视锥形瓶内溶液颜色的变化,能确定实验终点的现象是加入最后一滴液体,溶液由无色变成浅红色,且半分钟内不褪色.
(5)根据下列数据:
计算待测烧碱溶液的浓度为0.1053 mol/L(保留至小数点后四位).
0 159901 159909 159915 159919 159925 159927 159931 159937 159939 159945 159951 159955 159957 159961 159967 159969 159975 159979 159981 159985 159987 159991 159993 159995 159996 159997 159999 160000 160001 160003 160005 160009 160011 160015 160017 160021 160027 160029 160035 160039 160041 160045 160051 160057 160059 160065 160069 160071 160077 160081 160087 160095 203614
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:①取一支图1所示仪器,用蒸馏水洗净,即加入待测的NaOH溶液,
使尖嘴部分充满溶液,并调整液面处于“0“刻度以下的位置,记下读数;
②取锥形瓶用蒸馏水洗净,精确量取一定量的0.1000mol•L-1标准盐酸;
③加入3滴酚酞试液,摇匀;
④进行滴定实验,并记录数据.
⑤重复以上步骤2次.
回答下列问题:
(1)步骤①中应将NaOH溶液注入图中的碱式滴定管(填仪器名称)中.
(2)在步骤①中存在的明显错误是滴定管没有用待测NaOH溶液润洗,由此会使测定结果偏低(选填“偏高”、“偏低”或“无影响”).
(3)图2是某次实验中液面位置示意图,若A与B刻度间相差1mL,A处的刻度为19,滴定管中液面读数应为19.40mL.
(4)操作④中左手轻轻挤压玻璃球,右手振荡锥形瓶,眼睛注视锥形瓶内溶液颜色的变化,能确定实验终点的现象是加入最后一滴液体,溶液由无色变成浅红色,且半分钟内不褪色.
(5)根据下列数据:
| 滴定次数 | 标准盐酸体积/mL | 待测液体积/mL | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.52 | 19.42 |
| 第二次 | 20.00 | 4.07 | 23.17 |
| 第三次 | 20.00 | 1.08 | 20.08 |