6.某食用白醋是由醋酸与纯水配制而成,用0.1000mol/L NaOH溶液准确测定其中醋酸的物质的量浓度.以下为某同学列出的实验步骤(未排序),请回答下列问题.
A.分别向碱式滴定管、酸式滴定管注入NaOH标准溶液和待测醋酸至0刻度以上2~3cm
B.调节滴定管液面至0或0刻度以下,记下读数
C.用NaOH标准溶液滴定至终点,记下滴定管液面的刻度
D.用标准溶液清洗碱式滴定管2~3次;待测醋酸清洗酸式滴定管2~3次
E.用待测醋酸清洗锥形瓶2~3次
F.排气泡使滴定管尖嘴充满溶液,把滴定管固定好
G.滴定管检漏,用水清洗所有仪器,备用
H.通过酸式滴定管向锥形瓶注入20.00mL待测醋酸,并加入2-3滴指示剂
(1)用离子方程式表示该实验的原理CH3COOH+OH-=CH3COO-+H2O.
(2)从上述实验步骤中选出正确的并按操作先后排序.你的实验顺序为:(用字母表示)G→D→A→F→B→H→C.
(3)实验室常用的酸碱指示剂有甲基橙、石蕊和酚酞,你选择的指示剂是酚酞,理由是两者恰好完全中和生成醋酸钠,其水溶液呈碱性,必需选择在碱性范围变色且颜色容易判断的酚酞作指示剂判断滴定终点;滴定终点的现象是当滴加最后一滴氢氧化钠溶液时,溶液变为浅红色且30s不褪色.
(4)某同学实验后得到的数据如下:
原白醋中醋酸的物质的量浓度为0.07500mol/L(结果保留4位有效数字).
(5)分析下列操作对测定结果的影响,用“偏低”、“偏高”或“不影响”填空.
①滴定前碱式滴定管充满溶液,滴定后尖嘴处有气泡偏低;
②读取标准溶液体积时,滴定前平视,滴定后仰视偏高.
A.分别向碱式滴定管、酸式滴定管注入NaOH标准溶液和待测醋酸至0刻度以上2~3cm
B.调节滴定管液面至0或0刻度以下,记下读数
C.用NaOH标准溶液滴定至终点,记下滴定管液面的刻度
D.用标准溶液清洗碱式滴定管2~3次;待测醋酸清洗酸式滴定管2~3次
E.用待测醋酸清洗锥形瓶2~3次
F.排气泡使滴定管尖嘴充满溶液,把滴定管固定好
G.滴定管检漏,用水清洗所有仪器,备用
H.通过酸式滴定管向锥形瓶注入20.00mL待测醋酸,并加入2-3滴指示剂
(1)用离子方程式表示该实验的原理CH3COOH+OH-=CH3COO-+H2O.
(2)从上述实验步骤中选出正确的并按操作先后排序.你的实验顺序为:(用字母表示)G→D→A→F→B→H→C.
(3)实验室常用的酸碱指示剂有甲基橙、石蕊和酚酞,你选择的指示剂是酚酞,理由是两者恰好完全中和生成醋酸钠,其水溶液呈碱性,必需选择在碱性范围变色且颜色容易判断的酚酞作指示剂判断滴定终点;滴定终点的现象是当滴加最后一滴氢氧化钠溶液时,溶液变为浅红色且30s不褪色.
(4)某同学实验后得到的数据如下:
| 滴定次数 实验数据 | 1 | 2 | 3 | 4 | 5 |
| V(NaOH)/mL(初读数) | 0.00 | 0.20 | 0.00 | 0.10 | 0.05 |
| V(NaOH)/mL(终读数) | 15.75 | 15.20 | 14.98 | 15.12 | 15.05 |
(5)分析下列操作对测定结果的影响,用“偏低”、“偏高”或“不影响”填空.
①滴定前碱式滴定管充满溶液,滴定后尖嘴处有气泡偏低;
②读取标准溶液体积时,滴定前平视,滴定后仰视偏高.
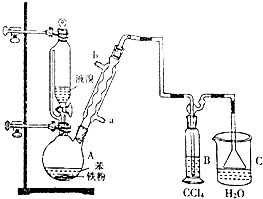
2.硅孔雀石是一种含铜矿石,含铜形态为CuCO3、Cu(OH)2和CuSiO3•2H2O,同时含有SiO2、FeCO3、Fe2O3、A12O3等杂质.以其为原料制取硫酸铜的工艺流程如下图所示:
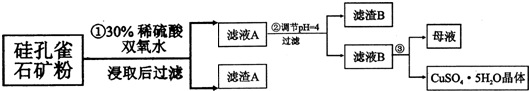
(1)步骤1中先加入足量稀硫酸,再加人双氧水.则双氧水参与该反应的离子方程式是2Fe2++H2O2+2H+═2Fe3++2H2O.
(2)步骤②调节溶液pH,可以选用的试剂是BC.(填字母编号)
A.A12O3 B.CuO C.CuCO3•Cu(OH)2
(3)有关氢氧化物开始沉淀和完全沉淀的pH如下表:
则滤液B中含有的阳离子是Al3+、H+、Cu2+.
(4)将滤液B通过蒸发浓缩、冷却结晶、过滤等操作可得到硫酸铜晶体.
(5)硫酸铜也可用硫化铜和氧气在高温、催化剂条件下化合制得,该反应的化学方程式是CuS+2O2$\frac{\underline{\;\;\;高温\;\;\;}}{催化剂}$CuSO4.取384g CuS在一定条件下和氧气完全反应,若发生2CuS+3O2=2CuO+2SO2和4CuS+5O2=2Cu2O+4SO2两个反应,在所得固体中Cu和O的物质的量之比n(Cu):n(O)=4:a,此时消耗空气的物质的量为bmol.则a=$\frac{2}{5}$b-8.(氧气占空气体积的五分之一)

(1)步骤1中先加入足量稀硫酸,再加人双氧水.则双氧水参与该反应的离子方程式是2Fe2++H2O2+2H+═2Fe3++2H2O.
(2)步骤②调节溶液pH,可以选用的试剂是BC.(填字母编号)
A.A12O3 B.CuO C.CuCO3•Cu(OH)2
(3)有关氢氧化物开始沉淀和完全沉淀的pH如下表:
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 |
(4)将滤液B通过蒸发浓缩、冷却结晶、过滤等操作可得到硫酸铜晶体.
(5)硫酸铜也可用硫化铜和氧气在高温、催化剂条件下化合制得,该反应的化学方程式是CuS+2O2$\frac{\underline{\;\;\;高温\;\;\;}}{催化剂}$CuSO4.取384g CuS在一定条件下和氧气完全反应,若发生2CuS+3O2=2CuO+2SO2和4CuS+5O2=2Cu2O+4SO2两个反应,在所得固体中Cu和O的物质的量之比n(Cu):n(O)=4:a,此时消耗空气的物质的量为bmol.则a=$\frac{2}{5}$b-8.(氧气占空气体积的五分之一)
20.某校化学兴趣小组采用酸碱中和滴定法测定学校新购入的烧碱的纯度(烧碱中含有不与酸反应的杂质),试根据实验回答.
(1)实验步骤为:①用托盘天平准确称量4.1g烧碱样品.
②将样品配成250ml待测液.
③量取10.00ml待测液,注入锥形瓶中.
④在锥形瓶中滴入2~3滴酚酞,用0.2010mol/L的标准盐酸滴定待测烧碱溶液.
(2)该小组测得如表数据
根据如表数据,计算烧碱的纯度98%.
0 159898 159906 159912 159916 159922 159924 159928 159934 159936 159942 159948 159952 159954 159958 159964 159966 159972 159976 159978 159982 159984 159988 159990 159992 159993 159994 159996 159997 159998 160000 160002 160006 160008 160012 160014 160018 160024 160026 160032 160036 160038 160042 160048 160054 160056 160062 160066 160068 160074 160078 160084 160092 203614
(1)实验步骤为:①用托盘天平准确称量4.1g烧碱样品.
②将样品配成250ml待测液.
③量取10.00ml待测液,注入锥形瓶中.
④在锥形瓶中滴入2~3滴酚酞,用0.2010mol/L的标准盐酸滴定待测烧碱溶液.
(2)该小组测得如表数据
| 滴定次数 | 待测液体积/ml | 标准盐酸体积/ml | |
| 滴定前读数/ml | 滴定后读数/ml | ||
| 第一次 | 10.00 | 0.20 | 22.90 |
| 第二次 | 10.00 | 0.50 | 20.40 |
| 第三次 | 10.00 | 4.00 | 24.10 |
| 第四次 | 10.00 | 0.00 | 20.00 |
 .
.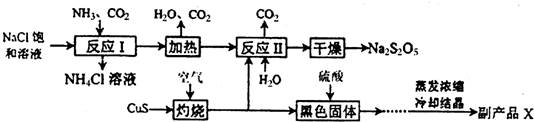
 Na2S2O3是重要的化工原料,易溶于水.在中性或碱性环境中稳定.
Na2S2O3是重要的化工原料,易溶于水.在中性或碱性环境中稳定.
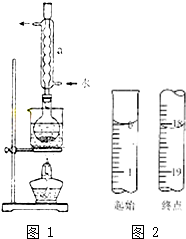
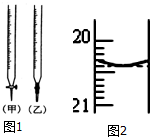 某校化学兴趣小组采用酸碱中和滴定法用0.1000mol/LNaOH溶液滴定待测盐酸溶液,试回答下面的问题:
某校化学兴趣小组采用酸碱中和滴定法用0.1000mol/LNaOH溶液滴定待测盐酸溶液,试回答下面的问题: