9.某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①碱式滴定管用蒸馏水洗净后,用待测溶液润洗2~3次后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中;
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂恰好变色,且半分钟不变化,测得所耗盐酸的体积为V1mL;
④重复以上过程,但滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.
(1)滴定终点时的现象为锥形瓶中的溶液由粉红色变为无色且在半分钟内不恢复
(2)该小组在步骤①中的错误是_待测溶液润洗锥形瓶,由此造成的测定结果偏高;(填偏高、偏低或无影响);
(3)步骤②缺少的操作是用标准液润洗滴定管2~3次;
(4)根据下列数据:
计算待测烧碱溶液的浓度为0.0800 mol/L.
①碱式滴定管用蒸馏水洗净后,用待测溶液润洗2~3次后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中;
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂恰好变色,且半分钟不变化,测得所耗盐酸的体积为V1mL;
④重复以上过程,但滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.
(1)滴定终点时的现象为锥形瓶中的溶液由粉红色变为无色且在半分钟内不恢复
(2)该小组在步骤①中的错误是_待测溶液润洗锥形瓶,由此造成的测定结果偏高;(填偏高、偏低或无影响);
(3)步骤②缺少的操作是用标准液润洗滴定管2~3次;
(4)根据下列数据:
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 0.40 | 20.38 |
| 第二次 | 25.00 | 4.00 | 24.02 |
5.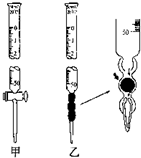 某学习小组用0.80mol/L标准浓度的烧碱溶液测定未知浓度的盐酸.
某学习小组用0.80mol/L标准浓度的烧碱溶液测定未知浓度的盐酸.
①用滴定的方法来测定盐酸的浓度,实验数据如表所示:
该未知盐酸的浓度为0.88mol•L-1(保留两位有效数字)
②滴定管如图所示,用乙滴定管盛装标准浓度的氢氧化钠溶液 (填“甲”或“乙”).
③下列操作会使所测得的盐酸的浓度偏低的是D.
A.盛装待测液的锥形瓶用水洗后未干燥
B.滴定前,碱式滴定管尖端有气泡,滴定后气泡消失
C.碱式滴定管用蒸馏水洗净后,未用标准氢氧化钠溶液润洗
D.读碱式滴定管的刻度时,滴定前仰视凹液面最低处,滴定后俯视读数.
 某学习小组用0.80mol/L标准浓度的烧碱溶液测定未知浓度的盐酸.
某学习小组用0.80mol/L标准浓度的烧碱溶液测定未知浓度的盐酸.①用滴定的方法来测定盐酸的浓度,实验数据如表所示:
| 实验编号 | 待测HCl溶液的体积/mL | 滴入NaOH溶液的体积/mL |
| 1 | 20.00 | 22.00 |
| 2 | 20.00 | 22.10 |
| 3 | 20.00 | 21.90 |
②滴定管如图所示,用乙滴定管盛装标准浓度的氢氧化钠溶液 (填“甲”或“乙”).
③下列操作会使所测得的盐酸的浓度偏低的是D.
A.盛装待测液的锥形瓶用水洗后未干燥
B.滴定前,碱式滴定管尖端有气泡,滴定后气泡消失
C.碱式滴定管用蒸馏水洗净后,未用标准氢氧化钠溶液润洗
D.读碱式滴定管的刻度时,滴定前仰视凹液面最低处,滴定后俯视读数.
2. 某研究性学习小组的学生用标准浓度的氢氧化钠溶液测定未知浓度的盐酸溶液.
某研究性学习小组的学生用标准浓度的氢氧化钠溶液测定未知浓度的盐酸溶液.
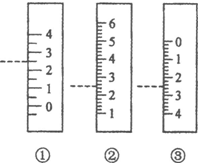
(1)该学生指示剂和装标准液的仪器选用正确的一组是D(写编号)
(2)该同学滴定操作的正确顺序是(用序号填写):
e→b→d→c→a→g→f
a.用酸式滴定管取盐酸溶液25.00mL,注入锥形瓶中,加入指示剂
b.用蒸馏水洗干净滴定管
c.用待测定的溶液润洗酸式滴定管
d.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”
以上2~3cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下
e.检查滴定管是否漏水.
f.另取锥形瓶,再重复操作一次
g.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,
记下滴定管液面所在刻度
(3)实验中用左手控制滴定管上橡胶管内的玻璃珠(填仪器及部位),眼睛注视锥形瓶中溶液的颜色变化,直至滴定终点.
判断到达终点的现象是当滴入最后一滴氢氧化钠溶液后,锥形瓶内最后溶液由无色突变为粉红色,且保持半分钟颜色不发生变化
(4)已知滴定管中装有浓度为0.1000mol/L的氢氧化钠.逐滴加入到装有盐酸溶液的锥形瓶中.开始时读数及恰好反应时氢氧化钠溶液的读数见下表.
请计算待测的盐酸的物质的量浓度0.0800mol/L
(5)下面操作会导致待测盐酸的浓度偏大的是ade(写编号)
a.其它操作均正确,滴定终点读数时,仰视滴定管的刻度
b.盛装待测液的锥形瓶用水洗后未用所装待测液润洗
c.盛装待测液的酸式滴定管未用待测液润洗
d.盛装标准液的碱式滴定管未用标准液洗
e.配制标准溶液时,称取的NaOH固体中含少量KOH.
 某研究性学习小组的学生用标准浓度的氢氧化钠溶液测定未知浓度的盐酸溶液.
某研究性学习小组的学生用标准浓度的氢氧化钠溶液测定未知浓度的盐酸溶液.| 序号 | 选用指示剂 | 选用滴定管 |
| A | 石蕊 | (乙) |
| B | 甲基橙 | (甲) |
| C | 酚酞 | (甲) |
| D | 酚酞 | (乙) |
(2)该同学滴定操作的正确顺序是(用序号填写):
e→b→d→c→a→g→f
a.用酸式滴定管取盐酸溶液25.00mL,注入锥形瓶中,加入指示剂
b.用蒸馏水洗干净滴定管
c.用待测定的溶液润洗酸式滴定管
d.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”
以上2~3cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下
e.检查滴定管是否漏水.
f.另取锥形瓶,再重复操作一次
g.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,
记下滴定管液面所在刻度
(3)实验中用左手控制滴定管上橡胶管内的玻璃珠(填仪器及部位),眼睛注视锥形瓶中溶液的颜色变化,直至滴定终点.
判断到达终点的现象是当滴入最后一滴氢氧化钠溶液后,锥形瓶内最后溶液由无色突变为粉红色,且保持半分钟颜色不发生变化
(4)已知滴定管中装有浓度为0.1000mol/L的氢氧化钠.逐滴加入到装有盐酸溶液的锥形瓶中.开始时读数及恰好反应时氢氧化钠溶液的读数见下表.
| 试验编号 | 待测盐酸溶液体积(mL) | 滴定开始读数(mL) | 滴定结束读数(mL) |
| ① | 25.00 | 0.00 | 20.00 |
| ② | 25.00 | 1.10 | 21.30 |
| ③ | 25.00 | 0.20 | 20.00 |
(5)下面操作会导致待测盐酸的浓度偏大的是ade(写编号)
a.其它操作均正确,滴定终点读数时,仰视滴定管的刻度
b.盛装待测液的锥形瓶用水洗后未用所装待测液润洗
c.盛装待测液的酸式滴定管未用待测液润洗
d.盛装标准液的碱式滴定管未用标准液洗
e.配制标准溶液时,称取的NaOH固体中含少量KOH.
6.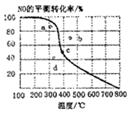 如图中曲线为一定压强下NO的平衡转化率与温度的关系,图中a、b、c、d四点表示不同温度、压强下2NO(g)+O2(g)?2NO2(g)达到平衡时NO的转化率,则压强最大的点为( )
如图中曲线为一定压强下NO的平衡转化率与温度的关系,图中a、b、c、d四点表示不同温度、压强下2NO(g)+O2(g)?2NO2(g)达到平衡时NO的转化率,则压强最大的点为( )
0 159896 159904 159910 159914 159920 159922 159926 159932 159934 159940 159946 159950 159952 159956 159962 159964 159970 159974 159976 159980 159982 159986 159988 159990 159991 159992 159994 159995 159996 159998 160000 160004 160006 160010 160012 160016 160022 160024 160030 160034 160036 160040 160046 160052 160054 160060 160064 160066 160072 160076 160082 160090 203614
 如图中曲线为一定压强下NO的平衡转化率与温度的关系,图中a、b、c、d四点表示不同温度、压强下2NO(g)+O2(g)?2NO2(g)达到平衡时NO的转化率,则压强最大的点为( )
如图中曲线为一定压强下NO的平衡转化率与温度的关系,图中a、b、c、d四点表示不同温度、压强下2NO(g)+O2(g)?2NO2(g)达到平衡时NO的转化率,则压强最大的点为( )| A. | a | B. | b | C. | c | D. | d |
 以下是我校化学兴趣小组的同学测定厨房食醋中醋酸浓度的实验,请你参与并完成相关实验:
以下是我校化学兴趣小组的同学测定厨房食醋中醋酸浓度的实验,请你参与并完成相关实验: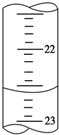 某课外活动小组欲用0.10mol/L的NaOH溶液滴定0.10mol/L的稀盐酸,其操作步骤如下:
某课外活动小组欲用0.10mol/L的NaOH溶液滴定0.10mol/L的稀盐酸,其操作步骤如下: 某同学用0.10mol/L的HCl溶液测定未知浓度的NaOH溶液,其实验操作如下:
某同学用0.10mol/L的HCl溶液测定未知浓度的NaOH溶液,其实验操作如下: