15.下列各组离子反应可用H++OH-═H2O表示的是( )
| A. | 氢氧化钡和硫酸 | B. | 氢氧化钠和醋酸 | ||
| C. | 亚硝酸和氢氧化钾 | D. | 硫酸氢钾和氢氧化钠 |
14.下表中是各组反应的反应物和反应温度,反应刚开始时,放出H2速率最快的是( )
| 编号 | 金属(粉末状)(mol) | 酸的浓度及体积 | 反应温度(℃) | ||
| A | Al | 0.1 | 0.1mol•L-1 硫酸 | 10mL | 60 |
| B | Fe | 0.1 | 0.2mol•L-1盐酸 | 10mL | 60 |
| C | Al | 0.1 | 18mol•L-1 硫酸 | 10mL | 60 |
| D | Mg | 0.1 | 0.2mol•L-1 硝酸 | 10mL | 60 |
| A. | A | B. | B | C. | C | D. | D |
10.25℃时,水的电离达到平衡:H2O?H++OH-,下列叙述正确的是( )
| A. | 将纯水加热到95℃时,Kw变大,pH不变,水仍呈中性 | |
| B. | 向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,Kw变小 | |
| C. | 向纯水中加入少量氢氧化钠固体,c(H+)减小,Kw不变 | |
| D. | 向纯水中加入盐酸,将抑制水的电离,Kw变小 |
9.己知单位体积的稀溶液中,非挥发性溶质的分子或离子数越多,该溶液的沸点就越高.则下列溶液沸点最高的是( )
| A. | 0.03mol•L-1的蔗糖溶液 | B. | 0.03mol•L-1的BaCl2溶液 | ||
| C. | 0.04mol•L-1的NaCl溶液 | D. | 0.02mol•L-1的CH3COOH溶液 |
7.25℃时加水稀释10mL pH=11的氨水,下列判断正确的是( )
| A. | 原氨水的浓度为10-3mol•L-1 | |
| B. | 溶液中$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$减小 | |
| C. | 氨水的电离程度增大,溶液中所有离子的浓度均减小 | |
| D. | 再加入10 mL pH=3的盐酸充分反应后混合液的pH值肯定大于7 |
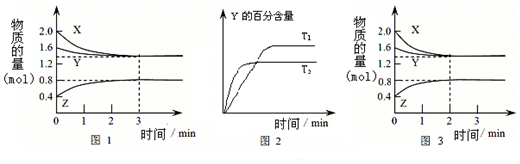
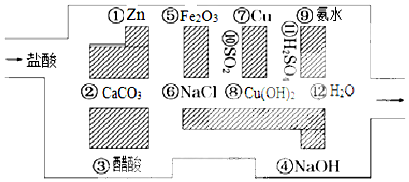
6.T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的物质的量变化如图-1所示;若保持其他条件不变,温度分别为T1和T2,Y的体积百分含量与时间的关系如图-2所示.下列分析正确的是( )
0 159894 159902 159908 159912 159918 159920 159924 159930 159932 159938 159944 159948 159950 159954 159960 159962 159968 159972 159974 159978 159980 159984 159986 159988 159989 159990 159992 159993 159994 159996 159998 160002 160004 160008 160010 160014 160020 160022 160028 160032 160034 160038 160044 160050 160052 160058 160062 160064 160070 160074 160080 160088 203614

| A. | 容器中发生的反应可表示为:2X(g)+Y(g)?2Z(g) | |
| B. | 0~3 min内,v(X)=0.2 mol•L-1•min-1 | |
| C. | 其他条件不变升高温度,v正、v逆都增大,且重新平衡前v正>v逆 | |
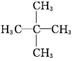
| D. | 若改变条件,使反应进程如图3所示,则改变的条件可能是增大压强 |
 2,2-二甲基丙烷,写出它和氯气发生一取代反应的方程式
2,2-二甲基丙烷,写出它和氯气发生一取代反应的方程式 +HCl
+HCl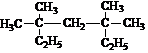 3,3,5,5-四甲基庚烷;它的一氯代物具有不同沸点的产物有4种
3,3,5,5-四甲基庚烷;它的一氯代物具有不同沸点的产物有4种 ;
; .
.