13.某次采集酸雨样品,每隔一段时间测定一次pH,得到数据如表:
(1)放置时,雨水样品pH变化的主要原因酸雨样品中的H2SO3逐渐被氧化成H2SO4,使溶液的酸性增强.
(2)pH变化的离子方程式:2H2SO3+O2=4H++SO42-.
| 时间 | 开始 | 8小时 | 16小时 | 24小时 | 32小时 | 40小时 | 48小时 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
(2)pH变化的离子方程式:2H2SO3+O2=4H++SO42-.
11.某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+m Y(g)?3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%.在此平衡体系中加入1molZ(g),恒定温度条件下,在平衡后X、Y、Z的体积分数不变.下列叙述正确的是( )
| A. | 第二次平衡时,Z的浓度为0.2 mol•L-1 | |
| B. | m=3 | |
| C. | X与Y的平衡转化率之比为1:2 | |
| D. | 加入Z后平衡没移动 |
10.下列叙述正确的是( )
| A. | 熵变小于零而焓变大于零的反应肯定不能自发发生 | |
| B. | 热化学方程式中△H的值与反应物的用量有关 | |
| C. | 化学反应中旧键断裂吸收能量,新键形成释放能量,所以化学反应伴随能量变化,但反应前后物质的总能量不变 | |
| D. | 其他条件不变,增大反应物浓度是通过增大活化分子百分数,使化学反应速率加快 |
9.甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
(1))CO(g)+2H2(g)?CH3OH(g)△H1
(2)CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
(3)CO2(g)+H2(g)?CO(g)+H2O(g)△H3
回答下列问题:
(1)已知反应①中相关的化学键键能数据如下:
由此计算△H1=-99kJ•mol-1;已知△H2=-58kJ•mol-1,则△H3=+41kJ•mol-1.
(2)反应①的化学平衡常数K表达式为K=$\frac{c(C{H}_{3}OH)}{c(CO){c}^{2}({H}_{2})}$.
0 159884 159892 159898 159902 159908 159910 159914 159920 159922 159928 159934 159938 159940 159944 159950 159952 159958 159962 159964 159968 159970 159974 159976 159978 159979 159980 159982 159983 159984 159986 159988 159992 159994 159998 160000 160004 160010 160012 160018 160022 160024 160028 160034 160040 160042 160048 160052 160054 160060 160064 160070 160078 203614
(1))CO(g)+2H2(g)?CH3OH(g)△H1
(2)CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
(3)CO2(g)+H2(g)?CO(g)+H2O(g)△H3
回答下列问题:
(1)已知反应①中相关的化学键键能数据如下:
| 化学键 | H-H | C-O | C═O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 1076 | 465 | 413 |
(2)反应①的化学平衡常数K表达式为K=$\frac{c(C{H}_{3}OH)}{c(CO){c}^{2}({H}_{2})}$.
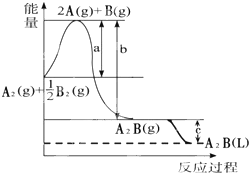 已知:A2(g)+$\frac{1}{2}$B2(g)═A2B(g),反应过程中能量变化如图,问:
已知:A2(g)+$\frac{1}{2}$B2(g)═A2B(g),反应过程中能量变化如图,问: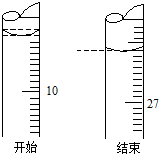 某学生欲用已知物质的量浓度的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白: