14.某溶液中含有四种离子,已知其中三种离子Na+、Mg2+、NO3-的物质的量浓度分别为0.2mol•L-1,0.1mol•L-1,0.1mol•L-1,则溶液中另一离子及其物质的量浓度可能是( )
| A. | SO42- 0.1 mol•L-1 | B. | Al3+ 0.2 mol•L-1 | ||
| C. | Cl- 0.3 mol•L-1 | D. | K+ 0.4 mol•L-1 |
13. 25℃时,三种酸的电离平衡常数如表:
25℃时,三种酸的电离平衡常数如表:
(1)常温下,若三者体积均为200mL 浓度均为0.1mol•L-1,则三者中C(H+)最小的是次氯酸(填名称).
(2)相同条件下,体积均为200mL、浓度均为0.1mol•L-1的CH3COOH(aq)和HCl(aq)分别与100mL 0.2mol•L-1NaOH溶液反应,放出热量较少的是醋酸 (填名称).
(3)下列四种离子结合质子能力由大到小的顺序是a>b>d>c(填序号).
a.CO32-b.ClO- c.CH3COO-d.HCO3-
(4)向次氯酸钠溶液中通入少量二氧化碳,写出该过程中反应的离子方程式:ClO-+CO2+H2O=HCO3-+HClO.
(5)在一定温度下,有 a.盐酸 b.硫酸 c.醋酸三种酸,当三者c(H+)相同且体积相同时,同时加入形状、密度、质量完全相同的锌粒,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为a=b=c(填序号),反应所需时间的长短关系是a=b>c(填序号).
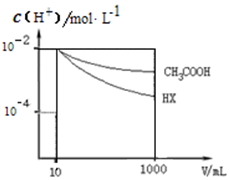
(6)相同条件下,体积均为10mL、c(H+)为0.01mol•L-1的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中c(H+)变化如图所示.
则HX的电离平衡常大于(填“大于”、“等于”或“小于”)醋酸的电离平衡常数.
 25℃时,三种酸的电离平衡常数如表:
25℃时,三种酸的电离平衡常数如表:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1 4.3×10-7 K2 5.6×10-11 | 3.0×10-8 |
(2)相同条件下,体积均为200mL、浓度均为0.1mol•L-1的CH3COOH(aq)和HCl(aq)分别与100mL 0.2mol•L-1NaOH溶液反应,放出热量较少的是醋酸 (填名称).
(3)下列四种离子结合质子能力由大到小的顺序是a>b>d>c(填序号).
a.CO32-b.ClO- c.CH3COO-d.HCO3-
(4)向次氯酸钠溶液中通入少量二氧化碳,写出该过程中反应的离子方程式:ClO-+CO2+H2O=HCO3-+HClO.
(5)在一定温度下,有 a.盐酸 b.硫酸 c.醋酸三种酸,当三者c(H+)相同且体积相同时,同时加入形状、密度、质量完全相同的锌粒,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为a=b=c(填序号),反应所需时间的长短关系是a=b>c(填序号).
(6)相同条件下,体积均为10mL、c(H+)为0.01mol•L-1的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中c(H+)变化如图所示.
则HX的电离平衡常大于(填“大于”、“等于”或“小于”)醋酸的电离平衡常数.
12.下列叙述中,不能用平衡移动原理解释的是( )
| A. | 红棕色的NO2气体,加压后颜色先变深后变浅 | |
| B. | 高压比常压有利于合成SO3的反应 | |
| C. | 氯气在水中溶解度大于饱和食盐水中的溶解度 | |
| D. | 由H2、I2蒸气、HI气体组成的平衡体系加压后颜色变深 |
11.下列关于葡萄糖的说法中,错误的是( )
| A. | 葡萄糖的分子式是C6H12O6 | |
| B. | 葡萄糖是多羟基醛,因而具有醛和多元醇的性质 | |
| C. | 葡萄糖是最简单的醛糖 | |
| D. | 葡萄糖可以通过绿色植物光合作用合成 |
10.下列生活习惯比较健康和科学的是( )
| A. | 新装修的房子应该开窗、通风一段时间后再入住 | |
| B. | 制作家具用的固化剂等化学试剂越多越好 | |
| C. | 饮用的水越纯净越健康 | |
| D. | 旧电池已不能使用,不需要回收 |
9.下列家庭化学小实验不能达到预期目的是( )
| A. | 用淀粉检验食盐中是否含碘元素 | |
| B. | 用醋、石灰水验证蛋壳中含有碳酸盐 | |
| C. | 用碘酒检验汽油中是否含有不饱和烃 | |
| D. | 用鸡蛋白、食盐、水完成蛋白质的溶解、盐析实验 |
8.唐山市曹妃甸区10月20日的空气质量日报如表:
下列情况对表中三个空气质量指标不会产生影响的是( )
| 项目 | 空气污染指数 | 空气质量级别 | 空气质量 |
| 可吸入颗粒物 | 65 | Ⅱ | 良 |
| 二氧化硫 | 6 | ||
| 二氧化氮 | 20 |
| A. | 用氢气作燃料 | B. | 露天焚烧垃圾 | ||
| C. | 大量排放汽车尾气 | D. | 用煤作燃料 |
7.请填写表格.
| 微粒 | 质子数 | 中子数 | 质量数 | 最外层电子数 | ZAX |
| Al | 27 | ||||
| S2- | 1634S2- |
6.下列叙述正确的是( )
| A. | 1 mol H2SO4的质量是98 g/mol | |
| B. | CO2的摩尔质量等于CO2的相对分子质量 | |
| C. | 摩尔质量建立了物质的物质的量与物质的质量之间的联系 | |
| D. | 1 mol任何物质的质量等于该物质的相对分子质量 |
5.下列说法不正确的是( )
0 159870 159878 159884 159888 159894 159896 159900 159906 159908 159914 159920 159924 159926 159930 159936 159938 159944 159948 159950 159954 159956 159960 159962 159964 159965 159966 159968 159969 159970 159972 159974 159978 159980 159984 159986 159990 159996 159998 160004 160008 160010 160014 160020 160026 160028 160034 160038 160040 160046 160050 160056 160064 203614
| A. | 油脂是高级脂肪酸和甘油生成的酯 | |
| B. | 米饭在嘴中越咀嚼越甜的原因是淀粉水解生成甜味物质 | |
| C. | 油脂、乙醇是人体必需的营养物质 | |
| D. | 水果因含有酯类物质而具有香味 |