6.根据如图所示的反应判断下列说法中错误的是( )
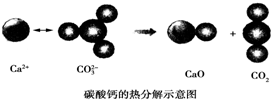

| A. | CO2(g)和CaO(s)的总能量大于CaCO3(s)的总能量 | |
| B. | 由该反应可推出凡是需要加热才发生的反应均为吸热反应 | |
| C. | 该反应的焓变大于零 | |
| D. | 该反应中有离子键断裂也有共价键断裂,化学键断裂吸收能量,化学键生成放出能量 |
5.高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=a kJ mol-1
(1)已知:①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1=+489.0kJ mol-1
②C(石墨)+CO2(g)=2CO(g)△H2=+172.5kJ mol-1
则a=-28.5kJ mol-1.
(2)冶炼铁反应的平衡常数表达式K=$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)}$,温度升高后,K值减小(填“增大”、“不变”或“减小”).
(3)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡.
①甲容器中CO的平衡转化率为60%.
②下列说法正确的是ac(填字母).
a.若容器内气体密度恒定时,标志反应达到平衡状态 b.甲容器中CO的平衡转化率大于乙的
c.甲、乙容器中,CO的平衡浓度之比为2:3 d.增加Fe2O3可以提高CO的转化率
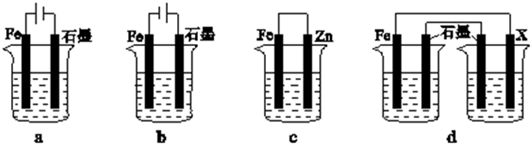
(4)采取一定措施可防止钢铁腐蚀.下列装置中的烧杯里均盛有等浓度、等体积的NaCl溶液.
①在a~c装置中,能保护铁的是bc(填字母).
②若用d装置保护铁,X极的电极材料应是锌(填名称).
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=a kJ mol-1
(1)已知:①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1=+489.0kJ mol-1
②C(石墨)+CO2(g)=2CO(g)△H2=+172.5kJ mol-1
则a=-28.5kJ mol-1.
(2)冶炼铁反应的平衡常数表达式K=$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)}$,温度升高后,K值减小(填“增大”、“不变”或“减小”).
(3)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡.
| Fe2O3 | CO | Fe | CO21 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |
②下列说法正确的是ac(填字母).
a.若容器内气体密度恒定时,标志反应达到平衡状态 b.甲容器中CO的平衡转化率大于乙的
c.甲、乙容器中,CO的平衡浓度之比为2:3 d.增加Fe2O3可以提高CO的转化率
(4)采取一定措施可防止钢铁腐蚀.下列装置中的烧杯里均盛有等浓度、等体积的NaCl溶液.
①在a~c装置中,能保护铁的是bc(填字母).
②若用d装置保护铁,X极的电极材料应是锌(填名称).

3.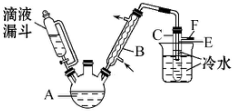 某校研究性学习小组,用乙醇与浓硫酸和溴化钠反应来制备溴乙烷,装置如下,反应需要加热,图中省去了加热装置,有关数据见表:
某校研究性学习小组,用乙醇与浓硫酸和溴化钠反应来制备溴乙烷,装置如下,反应需要加热,图中省去了加热装置,有关数据见表:
乙醇、溴乙烷、溴有关参数
(1)制备操作中,加入的浓硫酸必须进行稀释,其目的是abc( 多选 ).
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发d.水是反应的催化剂
(2)写出溴化氢与浓硫酸加热时发生反应的化学方程式2HBr+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$SO2+Br2+2H2O.
(3)加热的目的是加快反应速率,蒸馏出溴乙烷.
(4)图中试管C中的导管E的末端必须在水面以下,其原因是通过冷却得到溴乙烷,减少溴乙烷的挥发.
(5)为除去产品中的一种主要杂质,最好选择下列D(选填序号)溶液来洗涤产品.
A.氢氧化钠 B.氯化钠
C.碘化亚铁 D.亚硫酸钠
(6)第(5)题的实验所需要的玻璃仪器有分液漏斗、烧杯.
 某校研究性学习小组,用乙醇与浓硫酸和溴化钠反应来制备溴乙烷,装置如下,反应需要加热,图中省去了加热装置,有关数据见表:
某校研究性学习小组,用乙醇与浓硫酸和溴化钠反应来制备溴乙烷,装置如下,反应需要加热,图中省去了加热装置,有关数据见表:| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 深红棕色液体 |
| 密度/g•cm-3 | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
(1)制备操作中,加入的浓硫酸必须进行稀释,其目的是abc( 多选 ).
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发d.水是反应的催化剂
(2)写出溴化氢与浓硫酸加热时发生反应的化学方程式2HBr+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$SO2+Br2+2H2O.
(3)加热的目的是加快反应速率,蒸馏出溴乙烷.
(4)图中试管C中的导管E的末端必须在水面以下,其原因是通过冷却得到溴乙烷,减少溴乙烷的挥发.
(5)为除去产品中的一种主要杂质,最好选择下列D(选填序号)溶液来洗涤产品.
A.氢氧化钠 B.氯化钠
C.碘化亚铁 D.亚硫酸钠
(6)第(5)题的实验所需要的玻璃仪器有分液漏斗、烧杯.
1.对比以下几个反应式:
Cl+Cl→Cl2△H1=-243kJ/mol;
O+O→O2△H2=-497kJ/mol;
N+N→N2△H3=-946kJ/mol.
你可以得出的结论是( )
Cl+Cl→Cl2△H1=-243kJ/mol;
O+O→O2△H2=-497kJ/mol;
N+N→N2△H3=-946kJ/mol.
你可以得出的结论是( )
| A. | 在常温下氮气比氧气和氯气稳定 | |
| B. | 氮、氧和氯的单质常温下为气体 | |
| C. | 氮、氧和氯分子在反应过程中释放能量 | |
| D. | 氮气、氧气和氯气的密度不同 |
20.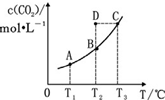 在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g).CO2(g)的平衡物质的量浓度 c(CO2)与温度 T 的关系如图所示.下列说法错误的是( )
在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g).CO2(g)的平衡物质的量浓度 c(CO2)与温度 T 的关系如图所示.下列说法错误的是( )
 在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g).CO2(g)的平衡物质的量浓度 c(CO2)与温度 T 的关系如图所示.下列说法错误的是( )
在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g).CO2(g)的平衡物质的量浓度 c(CO2)与温度 T 的关系如图所示.下列说法错误的是( )| A. | 反应 CO(g)+H2O(g)?CO2(g)+H2(g)的△H>0 | |
| B. | 在 T2时,若反应处于状态 D,则有 v 正<v 逆 | |
| C. | 平衡状态 A 与 C 相比,平衡状态 A 的 c(CO)小 | |
| D. | 若 T1、T2时的平衡常数分别为 K1、K2,则 K1<K2 |
19.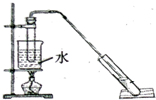 “酒是陈的香”,是因为酒在储存过程中生成了有香味的乙酸乙酯.某兴趣小组用无水乙醇和冰醋酸制备乙酸乙酯,相关物质的数据如下:
“酒是陈的香”,是因为酒在储存过程中生成了有香味的乙酸乙酯.某兴趣小组用无水乙醇和冰醋酸制备乙酸乙酯,相关物质的数据如下:
实验步骤如下:
①在试管里加入3mL乙醇;然后一边摇动,一边慢慢
加入2mL浓硫酸和2mL冰醋酸.再加入少量沸石.
②按照图示连接装置,水浴加热,使蒸气经导管通到饱和碳酸钠溶液的液面上.
③待小试管中收集约3mL产物时停止加热,撤出小试管并用力振荡,然后静置待其分层.
④分离出纯净的乙酸乙酯2.3mL.
(1)实验室制备乙酸乙酯的化学方程式为:CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O
该反应的类型为取代反应;浓硫酸在此反应中的作用是催化剂和吸水剂.
(2)步骤①中加入沸石的目的是防止暴沸;步骤②采用水浴的优点是受热均匀.长导管的作用是冷凝回流.
(3)步骤③中饱和碳酸钠的作用是BD
A、中和乙酸和乙醇
B、中和乙酸并吸收部分乙醇
C、加速酯的生成,提高酯的产率
D、乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出.
(4)步骤④中需要用到的关键仪器是分液漏斗,乙酸乙酯应该从该仪器的上部流出(选择)
A、下部流出 B、上部流出 C、都可以
(5)计算可得乙酸乙酯的产率为67.2%(产率=实际产量/理论产量,保留三位有效数字)
(6)随着科技水平的提高,工业上生产乙酸乙酯时产率可能会不断提高.请问产率是否有可能达到100%不能(填“有可能”或“不可能”),理由是该反应是可逆反应,反应物不可能完全转化成生成物.
 “酒是陈的香”,是因为酒在储存过程中生成了有香味的乙酸乙酯.某兴趣小组用无水乙醇和冰醋酸制备乙酸乙酯,相关物质的数据如下:
“酒是陈的香”,是因为酒在储存过程中生成了有香味的乙酸乙酯.某兴趣小组用无水乙醇和冰醋酸制备乙酸乙酯,相关物质的数据如下:| 物质 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 分子量 | 46 | 60 | 88 |
| 沸点(℃) | 78.5 | 117.9 | 77.1 |
| 密度(g/cm3) | 0.789 | 1.05 | 0.90 |
①在试管里加入3mL乙醇;然后一边摇动,一边慢慢
加入2mL浓硫酸和2mL冰醋酸.再加入少量沸石.
②按照图示连接装置,水浴加热,使蒸气经导管通到饱和碳酸钠溶液的液面上.
③待小试管中收集约3mL产物时停止加热,撤出小试管并用力振荡,然后静置待其分层.
④分离出纯净的乙酸乙酯2.3mL.
(1)实验室制备乙酸乙酯的化学方程式为:CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O
该反应的类型为取代反应;浓硫酸在此反应中的作用是催化剂和吸水剂.
(2)步骤①中加入沸石的目的是防止暴沸;步骤②采用水浴的优点是受热均匀.长导管的作用是冷凝回流.
(3)步骤③中饱和碳酸钠的作用是BD
A、中和乙酸和乙醇
B、中和乙酸并吸收部分乙醇
C、加速酯的生成,提高酯的产率
D、乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出.
(4)步骤④中需要用到的关键仪器是分液漏斗,乙酸乙酯应该从该仪器的上部流出(选择)
A、下部流出 B、上部流出 C、都可以
(5)计算可得乙酸乙酯的产率为67.2%(产率=实际产量/理论产量,保留三位有效数字)
(6)随着科技水平的提高,工业上生产乙酸乙酯时产率可能会不断提高.请问产率是否有可能达到100%不能(填“有可能”或“不可能”),理由是该反应是可逆反应,反应物不可能完全转化成生成物.
17.下列说法中正确的是( )
0 159840 159848 159854 159858 159864 159866 159870 159876 159878 159884 159890 159894 159896 159900 159906 159908 159914 159918 159920 159924 159926 159930 159932 159934 159935 159936 159938 159939 159940 159942 159944 159948 159950 159954 159956 159960 159966 159968 159974 159978 159980 159984 159990 159996 159998 160004 160008 160010 160016 160020 160026 160034 203614
| A. | 需要加热才能发生的反应一定是吸热反应,吸热反应的生成物总能量一定高于反应物总能量 | |
| B. | 同温同压下,H2(g)+Cl2(g)═2HCl(g) 在光照和点燃条件下的△H不同 | |
| C. | 一定条件下,0.5 mol N2和1.5 mol H2置于某密闭容器中充分反应生成NH3气,放热19.3kJ,其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ/mol | |
| D. | 一定条件下4 HCl(g)+O2(g)═2Cl2(g)+2H2O(g),当1 mol O2反应放出115.6 kJ热量,键能如下所示,则断裂1 mol H-O键与断裂1 mol H-Cl键所需能量差为31.9 kJ Cl2(g)$\stackrel{243kJ/mol}{→}$2Cl(g) O2(g)$\stackrel{498kJ/mol}{→}$2O(g) |
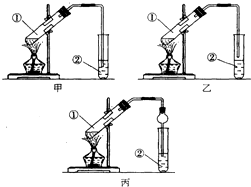 下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务.
下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务.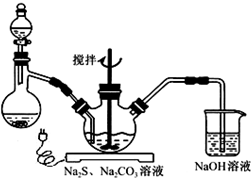 NaCN为剧毒无机物.某化学兴趣小组查阅资料得知,实验室里的氰化钠溶液可使用硫代硫酸钠溶液进行统一解毒销毁,他们开展了以下三个实验,根据要求回答问题:
NaCN为剧毒无机物.某化学兴趣小组查阅资料得知,实验室里的氰化钠溶液可使用硫代硫酸钠溶液进行统一解毒销毁,他们开展了以下三个实验,根据要求回答问题: