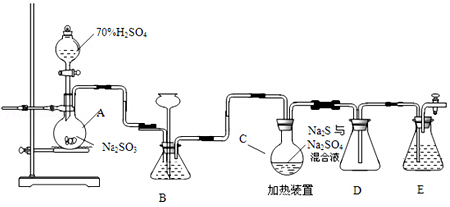
3.下列实验操作中,正确的是( )
| A. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| B. | 用蒸发的方法使NaCl从溶液中析出时,玻璃棒的作用是引流 | |
| C. | 蒸馏操作时,应使温度计水银球插入蒸馏烧瓶的液面以下 | |
| D. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
2.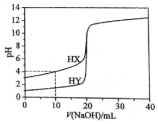 常温下,用浓度为0.1000mol•L-1的NaOH溶液分别逐滴加入到20.00mL 0.1000mol•L-1的HX、HY溶液中,pH随NaOH溶液体积的变化如图.下列说法正确( )
常温下,用浓度为0.1000mol•L-1的NaOH溶液分别逐滴加入到20.00mL 0.1000mol•L-1的HX、HY溶液中,pH随NaOH溶液体积的变化如图.下列说法正确( )
 常温下,用浓度为0.1000mol•L-1的NaOH溶液分别逐滴加入到20.00mL 0.1000mol•L-1的HX、HY溶液中,pH随NaOH溶液体积的变化如图.下列说法正确( )
常温下,用浓度为0.1000mol•L-1的NaOH溶液分别逐滴加入到20.00mL 0.1000mol•L-1的HX、HY溶液中,pH随NaOH溶液体积的变化如图.下列说法正确( )| A. | V(NaOH)=10.00 mL时,c(X-)>c(Na+)>c(H+)>c(OH-) | |
| B. | V(NaOH)=20.00 mL时,两份溶液中,c(X-)>c(Y-) | |
| C. | V(NaOH)=20.00 mL时,c(Na+)>c(X-)>c(OH-)>c(H+) | |
| D. | pH=7时,两份溶液中,c(X-)=c(Y-) |
17.下列关于能量转化的说法不正确的是( )
| A. | 生成物全部化学键形成时所释放的能量大于破坏反应物全部化学键所吸收的能量时,反应为放热反应 | |
| B. | 氢氧燃料电池使用时是将热能转化成电能 | |
| C. | 人们用氢氧焰焊接或切割金属,主要是利用了氢气和氧气化合时所放出的能量 | |
| D. | 太阳能光电池将太阳能直接转换为电能 |
16.已知热化学方程式:
S(s)+O2(g)═SO2(g)△H1
S(g)+O2(g)═SO2(g)△H2
2H2(g)+O2(g)═2H2O(g)△H3
2H2(g)+O2(g)═2H2O(l)△H4.
下列大小关系正确的是( )
S(s)+O2(g)═SO2(g)△H1
S(g)+O2(g)═SO2(g)△H2
2H2(g)+O2(g)═2H2O(g)△H3
2H2(g)+O2(g)═2H2O(l)△H4.
下列大小关系正确的是( )
| A. | △H2>△H1,△H4>△H3 | B. | △H1>△H2,△H4>△H3 | C. | △H1>△H2,△H3>△H4 | D. | △H2>△H1,△H3>△H4 |
15.己知常温常压下,N2(g)和H2(g)反应生成2molNH3(g),放出92.4kJ热量,在同温同压下向密闭容器中通入1molN2和3molH2,达平衡时放出热量为Q1kJ;向另体积相同的容器中通入0.5molN2和1.5molH2、1molNH3,相同温度下达平衡时放出热量为Q2kJ,则下列叙述正确的是( )
0 159827 159835 159841 159845 159851 159853 159857 159863 159865 159871 159877 159881 159883 159887 159893 159895 159901 159905 159907 159911 159913 159917 159919 159921 159922 159923 159925 159926 159927 159929 159931 159935 159937 159941 159943 159947 159953 159955 159961 159965 159967 159971 159977 159983 159985 159991 159995 159997 160003 160007 160013 160021 203614
| A. | Q2<Q1<92.4 | B. | 2Q2=Q1=92.4 | C. | Q1<Q2<92.4 | D. | Q2=Q1<92.4 |
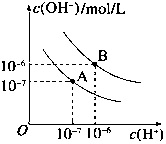 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示: