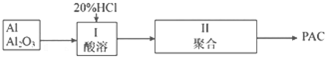
3. 乙酸正丁酯是一种水果香味的无色透明液体,常用于调制香料和药物.实验室用正丁醇和乙酸制备,反应原理如下:
乙酸正丁酯是一种水果香味的无色透明液体,常用于调制香料和药物.实验室用正丁醇和乙酸制备,反应原理如下:
CH3COOH+CH3CH2CH2CH2OH?△浓H2SO4CH3COOCH2CH2CH2CH3+H2O
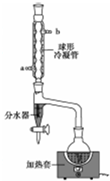
某兴趣小组拟用如图装置制备少量乙酸正丁酯:
步骤1:加料.向干燥的100ml圆底烧瓶中加入37ml正丁醇、22ml冰醋酸及10滴浓硫酸(试剂加入顺序未确定),摇匀后,加入几粒沸石.然后安装分水器(先在分水器上端小心加水至分水器支管口处,然后再放出1~2ml的水)及回流冷凝管.
步骤2:加热回流.通过活塞控制分水器中水层液面的高度.反应完毕,停止加热.
步骤3:冷却(不可以拆卸回流冷凝管).冷却至室温后,将烧瓶中的混合物与分水器中的酯层合并,转入分液漏斗中.
步骤4:依次用10ml水,10ml 10%碳酸钠溶液洗至中性(pH=7),再水洗一次,向洗涤后的有机相中加入适量的无水硫酸镁固体.放置一段时间后过滤、蒸馏、收集124~126℃馏分,得产品)
步骤5:用一干燥的小烧杯称产品,重量为29.0g.
相关物质的性质如表:
根据题意完成下列填空:
(1)加料时,三种试剂的加入顺序为正丁醇、冰醋酸、浓硫酸.
(2)该实验中,冷凝水从a(填“a”或“b”)口通入,使用分水器的目的是及时分离出产物水,使化学平衡向生成酯的方向移动,提高酯的产率.
(3)步骤2中判断反应结束的现象是分离器中水层高度不再变化.
(4)步骤3中从分液漏斗中得到酯的操作打开分液漏斗活塞,让水层从分液漏斗下口流出,酯层从上口倒出,用10% Na2CO3溶液洗涤有机相,是为了除去有机相中的H2SO4和CH3COOH(填结构简式).
(5)步骤4中加入无水硫酸镁固体的作用是除去有机相中残留的水.
(6)实验中正丁醇的转化率为65%.
 乙酸正丁酯是一种水果香味的无色透明液体,常用于调制香料和药物.实验室用正丁醇和乙酸制备,反应原理如下:
乙酸正丁酯是一种水果香味的无色透明液体,常用于调制香料和药物.实验室用正丁醇和乙酸制备,反应原理如下:CH3COOH+CH3CH2CH2CH2OH?△浓H2SO4CH3COOCH2CH2CH2CH3+H2O
某兴趣小组拟用如图装置制备少量乙酸正丁酯:
步骤1:加料.向干燥的100ml圆底烧瓶中加入37ml正丁醇、22ml冰醋酸及10滴浓硫酸(试剂加入顺序未确定),摇匀后,加入几粒沸石.然后安装分水器(先在分水器上端小心加水至分水器支管口处,然后再放出1~2ml的水)及回流冷凝管.
步骤2:加热回流.通过活塞控制分水器中水层液面的高度.反应完毕,停止加热.
步骤3:冷却(不可以拆卸回流冷凝管).冷却至室温后,将烧瓶中的混合物与分水器中的酯层合并,转入分液漏斗中.
步骤4:依次用10ml水,10ml 10%碳酸钠溶液洗至中性(pH=7),再水洗一次,向洗涤后的有机相中加入适量的无水硫酸镁固体.放置一段时间后过滤、蒸馏、收集124~126℃馏分,得产品)
步骤5:用一干燥的小烧杯称产品,重量为29.0g.
相关物质的性质如表:
| 物质名称 | 沸点/℃ | 熔点/℃ | 密度/g•cm-3 | 水中溶解度 |
| 正丁醇 | 117.3 | -89.5 | 0.80 | 7.1g/100g |
| 乙酸 | 118 | 16.6 | 1.0492 | 互溶 |
| 乙酸正丁酯 | 126.1 | -78 | 0.8826 | 1.4g/100g |
(1)加料时,三种试剂的加入顺序为正丁醇、冰醋酸、浓硫酸.
(2)该实验中,冷凝水从a(填“a”或“b”)口通入,使用分水器的目的是及时分离出产物水,使化学平衡向生成酯的方向移动,提高酯的产率.
(3)步骤2中判断反应结束的现象是分离器中水层高度不再变化.
(4)步骤3中从分液漏斗中得到酯的操作打开分液漏斗活塞,让水层从分液漏斗下口流出,酯层从上口倒出,用10% Na2CO3溶液洗涤有机相,是为了除去有机相中的H2SO4和CH3COOH(填结构简式).
(5)步骤4中加入无水硫酸镁固体的作用是除去有机相中残留的水.
(6)实验中正丁醇的转化率为65%.
1.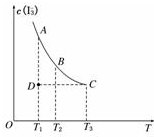 实验室将I2溶于KI溶液中,配制浓度较大的碘水,主要是因为发生了反应:I2(aq)+I-(aq)?I3-(aq),上述平衡体系中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态),下列说法不正确的是( )
实验室将I2溶于KI溶液中,配制浓度较大的碘水,主要是因为发生了反应:I2(aq)+I-(aq)?I3-(aq),上述平衡体系中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态),下列说法不正确的是( )
 实验室将I2溶于KI溶液中,配制浓度较大的碘水,主要是因为发生了反应:I2(aq)+I-(aq)?I3-(aq),上述平衡体系中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态),下列说法不正确的是( )
实验室将I2溶于KI溶液中,配制浓度较大的碘水,主要是因为发生了反应:I2(aq)+I-(aq)?I3-(aq),上述平衡体系中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态),下列说法不正确的是( )| A. | 该反应的正反应是吸热反应 | B. | A点与C点的化学反应速率vA<vC | ||
| C. | 在反应进行到D点时,v正>v逆 | D. | A点与B点相比,B点的c(I2)大 |
20.某化学小组以苯甲酸为原料,制取苯甲酸甲酯.已知有关物质的沸点如表:
Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入3mL浓硫酸、12.2g苯甲酸、20mL甲醇(密度约为0.79g/cm3).
(1)液体混合时,正确的加入顺序是先加入12.2g苯甲酸和20mL甲醇,再小心加入3mL浓硫酸.
(2)为防止圆底烧瓶中的液体在实验时发生暴沸,在加热前应采取的措施是加入沸石或碎瓷片.
(3)在该反应中反应物甲醇应过量,其理由是该反应是可逆反应,甲醇比苯甲酸价廉,且甲醇沸点低,易损失,故可增加甲醇的量,以提高苯甲酸的转化率.
Ⅱ.粗产品的精制
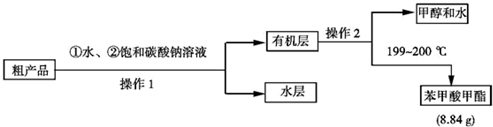
(4)现拟用下列流程精制苯甲酸甲酯,请根据流程图填入恰当操作方法的名称:操作1为分液,操作2为蒸馏.
(5)苯甲酸甲酯的产率为65%.
(6)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,某同学做了如下检验.
| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 65 | 249 | 199.6 |
在圆底烧瓶中加入3mL浓硫酸、12.2g苯甲酸、20mL甲醇(密度约为0.79g/cm3).
(1)液体混合时,正确的加入顺序是先加入12.2g苯甲酸和20mL甲醇,再小心加入3mL浓硫酸.
(2)为防止圆底烧瓶中的液体在实验时发生暴沸,在加热前应采取的措施是加入沸石或碎瓷片.
(3)在该反应中反应物甲醇应过量,其理由是该反应是可逆反应,甲醇比苯甲酸价廉,且甲醇沸点低,易损失,故可增加甲醇的量,以提高苯甲酸的转化率.
Ⅱ.粗产品的精制
(4)现拟用下列流程精制苯甲酸甲酯,请根据流程图填入恰当操作方法的名称:操作1为分液,操作2为蒸馏.

(5)苯甲酸甲酯的产率为65%.
(6)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,某同学做了如下检验.
| 检验项目 | 实验现象及结论 |
| 检验粗产品中含有水的操作是 | |
| 检验粗产品中含有硫酸的操作是 |
19.对于平衡体系mA(g)+nB(g)═pC(g)+qD(g)△H<0.下列结论中错误的是( )
| A. | 若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则m+n<p+q | |
| B. | 若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n | |
| C. | 若m+n=p+q,则往含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a | |
| D. | 若温度不变时,压强增大到原来的2倍,达到新平衡时,总体积一定比原来的$\frac{1}{2}$要小 |
17. 乙醛在催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见表:
乙醛在催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见表:
请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为(注明反应条件)2CH3CHO+O2$\stackrel{60℃-80℃}{→}$2CH3COOH;
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置.在实验开始时温度计水银球的位置应在试管A的反应液中,目的是控制反应温度为60℃~80℃;当试管A内的主要反应完成后,应进行蒸馏操作,温度计水银球的位置应在在试管A的支管口处.
(3)烧杯B内盛装的液体可以是甘油(写出一种即可).
(4)若想检验试管C中是否含有产物乙酸,在下列所提供的药品或用品中,可以使用的是ab.(填字母)
a.pH试纸 b.碳酸氢钠粉末
c.红色石蕊试纸 d.银氨溶液.
 乙醛在催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见表:
乙醛在催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见表:| 物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
| 沸点 | 20.8℃ | 117.9℃ | 290℃ | 197.2℃ | 100℃ |
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为(注明反应条件)2CH3CHO+O2$\stackrel{60℃-80℃}{→}$2CH3COOH;
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置.在实验开始时温度计水银球的位置应在试管A的反应液中,目的是控制反应温度为60℃~80℃;当试管A内的主要反应完成后,应进行蒸馏操作,温度计水银球的位置应在在试管A的支管口处.
(3)烧杯B内盛装的液体可以是甘油(写出一种即可).
(4)若想检验试管C中是否含有产物乙酸,在下列所提供的药品或用品中,可以使用的是ab.(填字母)
a.pH试纸 b.碳酸氢钠粉末
c.红色石蕊试纸 d.银氨溶液.
16.苯甲酸乙酯是一种无色透明液体、能与乙醇、乙醚混溶,不溶于水.用于配制香水香精和人造精油,其制备原理如表:
已知:
*苯甲酸在100℃会迅速升华.
(1)如图1为课本上制取乙酸乙酯的实验装置图,请回答下列问题:

①浓硫酸的作用是催化剂、吸水剂;
②实验开始前在饱和碳酸钠加入酚酞,溶液会变红,随着乙酸乙酯的蒸出,红色会变浅,但是无气体产生,请写出发生该变化的离子反应方程式CH3COOH+CO32-=CH3COO-+HCO3-;
(2)按照图2所示装置制备苯甲酸乙酯.
①制备:在圆底烧瓶中加入12.20g苯甲酸、25mL乙醇(过量)、4mL浓硫酸,混合均匀并加入沸石,按图2所示连接好仪器,其中分水器的作用是分离出反应生成的水,控制温度加热回流2h.
a.实验中使用分水器不断分离除去水的目的是分离反应过程中生的水,促进酯化反应向正反应方向进行;
b.从提供的分析实验室制取苯甲酸乙酯为什么不使用制取乙酸乙酯一样的装置?如果使用制取乙酸乙酯的装置,会使乙醇大量蒸馏出去,实验效率大大降低
②产品的提纯
将圆底烧瓶中的残液倒入盛有冷水的烧瓶中,分批加入Na2CO3溶液呈中性;用分液漏斗分出有机层得粗产品.水层用25mL乙醚萃取分液,醚层与粗产品合并;在粗产品加入无水氯化钙后,静置、过滤,过滤液进行蒸馏,蒸出乙醚后,继续升温,接收210~213℃的馏分;产品经检验合格,测得产品体积为6mL.
c.在该实验分液过程中,产物应该从分液漏斗的上口倒出 (填“上口倒出”可“下口倒出”);
d.该实验中苯甲酸乙酯的产率为42%;
e.若加入的Na2CO3溶液不足,在之后的蒸馏时烧瓶内会出现白烟生成,产生该现象的原因在苯甲酸乙酯中有未除尽的苯甲酸,受热至100℃时升华.
已知:

| 物质 | 颜色状态 | 密度/g/cm3 | 熔点/℃ | 沸点/℃ |
| 苯甲酸* | 白色固体 | 1.2659 | 122 | 249 |
| 苯甲酸乙酯 | 无色液体 | 1.05 | -34.6 | 212.6 |
| 乙酸 | 无色液体 | 1.0492 | 16.6 | 117.9 |
| 乙醇 | 无色液体 | 0.789 | -117.3 | 78.5 |
| 乙酸乙酯 | 无色液体 | 0.894-0.898 | -83.6 | 77.1 |
| 乙醚 | 无色液体 | 0.713 | -116.3 | 34.6 |
(1)如图1为课本上制取乙酸乙酯的实验装置图,请回答下列问题:

①浓硫酸的作用是催化剂、吸水剂;
②实验开始前在饱和碳酸钠加入酚酞,溶液会变红,随着乙酸乙酯的蒸出,红色会变浅,但是无气体产生,请写出发生该变化的离子反应方程式CH3COOH+CO32-=CH3COO-+HCO3-;
(2)按照图2所示装置制备苯甲酸乙酯.
①制备:在圆底烧瓶中加入12.20g苯甲酸、25mL乙醇(过量)、4mL浓硫酸,混合均匀并加入沸石,按图2所示连接好仪器,其中分水器的作用是分离出反应生成的水,控制温度加热回流2h.
a.实验中使用分水器不断分离除去水的目的是分离反应过程中生的水,促进酯化反应向正反应方向进行;
b.从提供的分析实验室制取苯甲酸乙酯为什么不使用制取乙酸乙酯一样的装置?如果使用制取乙酸乙酯的装置,会使乙醇大量蒸馏出去,实验效率大大降低
②产品的提纯
将圆底烧瓶中的残液倒入盛有冷水的烧瓶中,分批加入Na2CO3溶液呈中性;用分液漏斗分出有机层得粗产品.水层用25mL乙醚萃取分液,醚层与粗产品合并;在粗产品加入无水氯化钙后,静置、过滤,过滤液进行蒸馏,蒸出乙醚后,继续升温,接收210~213℃的馏分;产品经检验合格,测得产品体积为6mL.
c.在该实验分液过程中,产物应该从分液漏斗的上口倒出 (填“上口倒出”可“下口倒出”);
d.该实验中苯甲酸乙酯的产率为42%;
e.若加入的Na2CO3溶液不足,在之后的蒸馏时烧瓶内会出现白烟生成,产生该现象的原因在苯甲酸乙酯中有未除尽的苯甲酸,受热至100℃时升华.
14.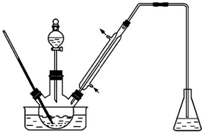 实验室以苯甲醛为原料制备间溴苯甲醛(实验装置如图,相关物质的沸点见附表).
实验室以苯甲醛为原料制备间溴苯甲醛(实验装置如图,相关物质的沸点见附表).
附表 相关物质的沸点(101kPa)
其实验步骤为:
步骤1:将三颈瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后,升温至60℃,缓慢滴加经浓H2SO4干燥过的液溴,保温反应一段时间,冷却.
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液.有机层用10%NaHCO3溶液洗涤.
步骤3:经洗涤的有机层加入适量无水MgSO4固体,放置一段时间后过滤.
步骤4:减压蒸馏有机层,收集相应馏分.
(1)实验装置中冷凝管的主要作用是冷凝回流,锥形瓶中的溶液应为NaOH.
(2)步骤1所加入的物质中,有一种物质是催化剂,其化学式为AlCl3.
(3)步骤2中用10%NaHCO3溶液洗涤有机层,是为了除去溶于有机层的Br2、HCl(填化学式).
(4)步骤3中加入无水MgSO4固体的作用是除去有机相的水.
(5)步骤4中采用减压蒸馏技术,是为了防止间溴苯甲醛被氧化.
0 159825 159833 159839 159843 159849 159851 159855 159861 159863 159869 159875 159879 159881 159885 159891 159893 159899 159903 159905 159909 159911 159915 159917 159919 159920 159921 159923 159924 159925 159927 159929 159933 159935 159939 159941 159945 159951 159953 159959 159963 159965 159969 159975 159981 159983 159989 159993 159995 160001 160005 160011 160019 203614
 实验室以苯甲醛为原料制备间溴苯甲醛(实验装置如图,相关物质的沸点见附表).
实验室以苯甲醛为原料制备间溴苯甲醛(实验装置如图,相关物质的沸点见附表).附表 相关物质的沸点(101kPa)
| 物质 | 沸点/℃ | 物质 | 沸点/℃ |
| 溴 | 58.8 | 1,2-二氯乙烷 | 83.5 |
| 苯甲醛 | 179 | 间溴苯甲醛 | 229 |
步骤1:将三颈瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后,升温至60℃,缓慢滴加经浓H2SO4干燥过的液溴,保温反应一段时间,冷却.
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液.有机层用10%NaHCO3溶液洗涤.
步骤3:经洗涤的有机层加入适量无水MgSO4固体,放置一段时间后过滤.
步骤4:减压蒸馏有机层,收集相应馏分.
(1)实验装置中冷凝管的主要作用是冷凝回流,锥形瓶中的溶液应为NaOH.
(2)步骤1所加入的物质中,有一种物质是催化剂,其化学式为AlCl3.
(3)步骤2中用10%NaHCO3溶液洗涤有机层,是为了除去溶于有机层的Br2、HCl(填化学式).
(4)步骤3中加入无水MgSO4固体的作用是除去有机相的水.
(5)步骤4中采用减压蒸馏技术,是为了防止间溴苯甲醛被氧化.

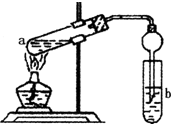 如图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀.在右试管中加入5mL饱和Na2CO3溶液.按图连接好装置,用酒精灯对左试管小火加热3~5min后,改用大火加热,当观察到右试管中有明显现象时停止实验.
如图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀.在右试管中加入5mL饱和Na2CO3溶液.按图连接好装置,用酒精灯对左试管小火加热3~5min后,改用大火加热,当观察到右试管中有明显现象时停止实验.