3.金属钛及钛的合金被认为是21世纪重要的金属材料.常温下钛不和非金属、强酸反应.TiO2既是制备其他含钛化合物的原料,又是一种性能优异的白色颜料.
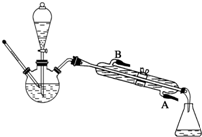
(1)实验室利用反应TiO2(s)+CCl4(g)$\frac{\underline{\;△\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下,制取TiCl4实验装置示意图如图:
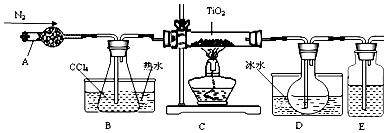
有关物质性质如表:
①仪器A的名称是干燥管,装置E中的试剂是浓硫酸.
②欲分离D中的液态混合物,所采用操作的名称是蒸馏.
(2)工业上可以由钛铁矿(FeTiO3)(含Fe2O3等杂质)制备金属Ti.
工业制备过程由钛铁矿经过酸溶解、过滤以及后续一系列化学变化和物理变化,可以将不溶于水的H2TiO3从溶液中过滤出来,再对H2TiO3进行洗涤,最后对H2TiO3进行煅烧得到TiO2,最终获得金属Ti.过程简化如下:
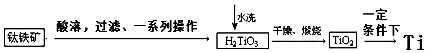
①水洗H2TiO3后,向洗涤液中加滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是Fe2+.
用离子方程式解释“出现微红色”的原因2Fe2++H2O2+2H+=2Fe3++2H2O,Fe3++3SCN-=Fe(SCN)3
②以TiO2为原料制取金属钛的其中一步反应为TiO2、氯气和焦炭反应生成TiCl4,己知该反应中氧化剂与还原剂的物质的量之比为1:1,则另一生成物为CO.
③用Mg还原TiCl4制金属钛取过程中必须在1070K的温度下进行,你认为还应该控制的反应条件是隔绝空气(或惰性气氛中);
所得到的金属钛中混有少量杂质,可加入稀盐酸或稀硫酸溶解后除去.
(1)实验室利用反应TiO2(s)+CCl4(g)$\frac{\underline{\;△\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下,制取TiCl4实验装置示意图如图:

有关物质性质如表:
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
②欲分离D中的液态混合物,所采用操作的名称是蒸馏.
(2)工业上可以由钛铁矿(FeTiO3)(含Fe2O3等杂质)制备金属Ti.
工业制备过程由钛铁矿经过酸溶解、过滤以及后续一系列化学变化和物理变化,可以将不溶于水的H2TiO3从溶液中过滤出来,再对H2TiO3进行洗涤,最后对H2TiO3进行煅烧得到TiO2,最终获得金属Ti.过程简化如下:

①水洗H2TiO3后,向洗涤液中加滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是Fe2+.
用离子方程式解释“出现微红色”的原因2Fe2++H2O2+2H+=2Fe3++2H2O,Fe3++3SCN-=Fe(SCN)3
②以TiO2为原料制取金属钛的其中一步反应为TiO2、氯气和焦炭反应生成TiCl4,己知该反应中氧化剂与还原剂的物质的量之比为1:1,则另一生成物为CO.
③用Mg还原TiCl4制金属钛取过程中必须在1070K的温度下进行,你认为还应该控制的反应条件是隔绝空气(或惰性气氛中);
所得到的金属钛中混有少量杂质,可加入稀盐酸或稀硫酸溶解后除去.
17.氯化铁是常见的水处理剂,利用废铁屑可制备无水氯化铁.实验室制备装置和工业制备流程图如下:
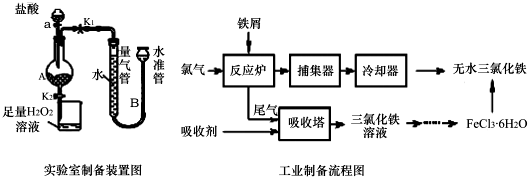
已知:(1)无水FeCl3熔点为555K、沸点为588K.(2)废铁屑中的杂质不与盐酸反应
(3)不同温度下六水合氯化铁在水中的溶解度如下:
实验室制备操作步骤如下:
Ⅰ.打开弹簧夹K1,关闭活塞K2,并打开活塞a,缓慢滴加盐酸.
Ⅱ.当…时,关闭弹簧夹K1,打开弹簧夹K2,当A中溶液完全进入烧杯后关闭活塞a.
Ⅲ.将烧杯中溶液经过一系列操作后得到FeCl3•6H2O晶体.请回答:
(1)烧杯中足量的H2O2溶液的作用是把亚铁离子全部氧化成三价铁离子.
(2)为了测定废铁屑中铁的质量分数,操作Ⅱ中“…”的内容是装置A中不产生气泡或量气管和水准管液面不变.
(3)从FeCl3溶液制得FeCl3•6H2O晶体的操作步骤是:加入 盐酸后、蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(4)试写出吸收塔中反应的离子方程式:2Fe2++Cl2=2Fe3++2Cl-.
(5)捕集器温度超过673K时,存在相对分子质量为325的铁的氯化物,该物质的分子式为Fe2Cl6.
(6)FeCl3的质量分数通常可用碘量法测定:称取m g无水氯化铁样品,溶于稀盐酸,配制成100mL溶液;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入几滴淀粉溶液,并用c mol•L-1Na2S2O3溶液滴定,消耗VmL(已知:I2+2S2O32-═2I-+S4O62-).
样品中氯化铁的质量分数$\frac{162.5cV}{m}$%.
0 159813 159821 159827 159831 159837 159839 159843 159849 159851 159857 159863 159867 159869 159873 159879 159881 159887 159891 159893 159897 159899 159903 159905 159907 159908 159909 159911 159912 159913 159915 159917 159921 159923 159927 159929 159933 159939 159941 159947 159951 159953 159957 159963 159969 159971 159977 159981 159983 159989 159993 159999 160007 203614

已知:(1)无水FeCl3熔点为555K、沸点为588K.(2)废铁屑中的杂质不与盐酸反应
(3)不同温度下六水合氯化铁在水中的溶解度如下:
| 温度/℃ | 0 | 20 | 80 | 100 |
| 溶解度(g/100g H2O) | 74.4 | 91.8 | 525.8 | 535.7 |
Ⅰ.打开弹簧夹K1,关闭活塞K2,并打开活塞a,缓慢滴加盐酸.
Ⅱ.当…时,关闭弹簧夹K1,打开弹簧夹K2,当A中溶液完全进入烧杯后关闭活塞a.
Ⅲ.将烧杯中溶液经过一系列操作后得到FeCl3•6H2O晶体.请回答:
(1)烧杯中足量的H2O2溶液的作用是把亚铁离子全部氧化成三价铁离子.
(2)为了测定废铁屑中铁的质量分数,操作Ⅱ中“…”的内容是装置A中不产生气泡或量气管和水准管液面不变.
(3)从FeCl3溶液制得FeCl3•6H2O晶体的操作步骤是:加入 盐酸后、蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(4)试写出吸收塔中反应的离子方程式:2Fe2++Cl2=2Fe3++2Cl-.
(5)捕集器温度超过673K时,存在相对分子质量为325的铁的氯化物,该物质的分子式为Fe2Cl6.
(6)FeCl3的质量分数通常可用碘量法测定:称取m g无水氯化铁样品,溶于稀盐酸,配制成100mL溶液;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入几滴淀粉溶液,并用c mol•L-1Na2S2O3溶液滴定,消耗VmL(已知:I2+2S2O32-═2I-+S4O62-).
样品中氯化铁的质量分数$\frac{162.5cV}{m}$%.
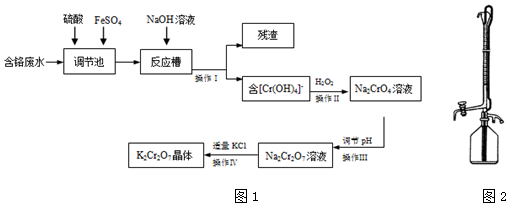
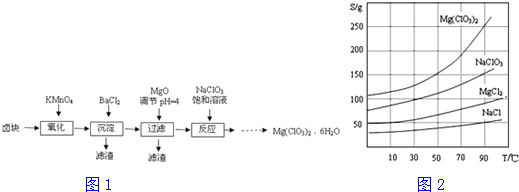
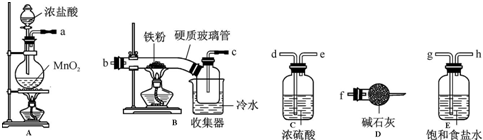
 已知乙酸和乙醇在浓硫酸催化下会发生下列反应:
已知乙酸和乙醇在浓硫酸催化下会发生下列反应: