1.氢气和氟气混合在黑暗处即可发生爆炸而释放出大量的热量.在反应过程中,断裂1molH2中的化学键消耗的能量为Q1kJ,断裂1molF2中的化学键消耗的能量为Q2kJ,形成1molHF中的化学键释放的能量为Q3kJ.下列关系式中正确的是( )
| A. | Q1+Q2<2Q3 | B. | Q1+Q2>2Q3 | C. | Q1+Q2<Q3 | D. | Q1+Q2>Q3 |
20.下列说法正确的是( )
| A. | 中和热一定是强酸跟强碱反应放出的热量 | |
| B. | 1 mol酸与1 mol碱完全反应放出的热量是中和热 | |
| C. | 在稀溶液中,酸与碱发生中和反应生成1 mol H2O(l)时的反应热叫做中和热 | |
| D. | 表示中和热的离子方程式为:H+(aq)+OH-(aq)=H2O(l)△H=57.3KJ/mol |
19.通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.现给出化学键的键能(见表):
请计算N2(g)+3H2(g)═2NH3(g)的反应热( )
| 化学键 | H-H | N三N | N-H |
| 键能/(kJ•mol-1) | 436 | 945.6 | 391 |
| A. | +192.4 kJ•mol-1 | B. | +92.4kJ•mol-1 | C. | -92.4kJ•mol-1 | D. | -192.4kJ•mol-1 |
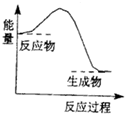
18.下列反应中,属于氧化还原反应且反应前后能量变化如图所示的是( )

| A. | 生石灰溶于水 | |
| B. | 高温条件下铝与氧化铁的反应 | |
| C. | 高温条件下碳粉与二氧化碳的反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4C1固体的反应 |
17.对于一个放热反应,已知产物的总能量为90KJ,那么反应物的总能量可能是( )
| A. | 20KJ | B. | 40KJ | C. | 90KJ | D. | 100KJ |
16.在密闭容器中充入4molSO2和3molO2,一定条件下建立如下平衡:2SO2(g)+O2(g)?2SO3(g)△H=-QKJ/mol,测得SO2的转化率为90%,则在此条件下反应放出的热量为(KJ)( )
0 159792 159800 159806 159810 159816 159818 159822 159828 159830 159836 159842 159846 159848 159852 159858 159860 159866 159870 159872 159876 159878 159882 159884 159886 159887 159888 159890 159891 159892 159894 159896 159900 159902 159906 159908 159912 159918 159920 159926 159930 159932 159936 159942 159948 159950 159956 159960 159962 159968 159972 159978 159986 203614
| A. | 2Q | B. | Q | C. | 1.8Q | D. | 0.9Q |