9.用纤维素为主要原料制备乙酸乙酯的路线如下:
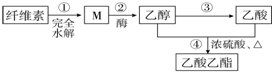
下列说法正确的是( )

下列说法正确的是( )
| A. | ③和④都发生了氧化还原反应 | |
| B. | M虽然分子结构中无醛基,但仍然可以发生银镜反应 | |
| C. | 步骤②,1molM完全反应可以生成3mol乙醇 | |
| D. | 若用淀粉替代纤维素,一定条件下也能按照此路线制备乙酸乙酯 |
8.某实验小组在制取乙酸乙酯的过程中用了过量的乙酸与乙醇反应,没有发现有副产物生成,装置气密性良好,产物也被充分冷凝,但乙醇的转化率始终不是很高,其主要原因是( )
| A. | 该反应为可逆反应,不可能进行到底,即乙醇的转化率一定达不到100% | |
| B. | 乙酸挥发,导致其量减少,乙醇过量,不能充分转化为乙酸乙酯 | |
| C. | 产物不稳定,易被氧化为其他物质而影响乙醇的转化率 | |
| D. | 馏出物导入饱和碳酸钠溶液液面上,有较多的乙酸乙酯溶解于水溶液中 |
7.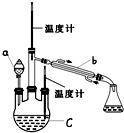 某实验小组用如图所示装置(略去加热装置)制备 乙酸乙酯.
某实验小组用如图所示装置(略去加热装置)制备 乙酸乙酯.
(1)仪器C的名称是三颈烧瓶,要向C中加4mL浓硫酸、6mL乙醇、4mL乙酸,
其操作顺序是乙醇、浓硫酸、乙酸.
(2)硫酸分子结构式: 浓硫酸溶于乙醇不是简单的物理溶解,而是伴随着化学变化,生成硫酸乙酯和硫酸二乙酯,请写出乙醇和硫酸反应生成硫酸二乙酯的方程式2C2H5OH+H2SO4→(OC2H5)2SO2+2H2O.
浓硫酸溶于乙醇不是简单的物理溶解,而是伴随着化学变化,生成硫酸乙酯和硫酸二乙酯,请写出乙醇和硫酸反应生成硫酸二乙酯的方程式2C2H5OH+H2SO4→(OC2H5)2SO2+2H2O.
(3)合成乙酸乙酯的反应为放热反应.实验研究表明,反应温度应控制在85℃左右为宜.请根据反应原理分析温度控制的原因:温度低,反应速率低,达不到催化剂活性温度,温度过高;温度过高,利于平衡逆向移动,酯产率降低.
(4)反应完成后,得到粗产品进行除杂.
①把锥形瓶中的粗产品转移到分液漏斗中,加适量的饱和Na2CO3溶液,充分振荡静置,分离时,乙酸乙酯应该从仪器上口倒出(填“下口放出”或“上口倒出”).查阅资料,
相关物质的部分性质:
根据表数据有同学提出可用水替代饱和Na2CO3溶液,你认为可行吗?说明理由:不可行;乙酸乙酯在乙醇、乙酸在水的混合溶液中溶解度比较大.
②为了得到纯度高的产品,一般在①中得到的乙酸乙酯用氯化钙除去其中少量的乙醇,最后用b(选填序号)进行干燥.
a、浓硫酸b、无水硫酸钠c、碱石灰.
 某实验小组用如图所示装置(略去加热装置)制备 乙酸乙酯.
某实验小组用如图所示装置(略去加热装置)制备 乙酸乙酯.(1)仪器C的名称是三颈烧瓶,要向C中加4mL浓硫酸、6mL乙醇、4mL乙酸,
其操作顺序是乙醇、浓硫酸、乙酸.
(2)硫酸分子结构式:
 浓硫酸溶于乙醇不是简单的物理溶解,而是伴随着化学变化,生成硫酸乙酯和硫酸二乙酯,请写出乙醇和硫酸反应生成硫酸二乙酯的方程式2C2H5OH+H2SO4→(OC2H5)2SO2+2H2O.
浓硫酸溶于乙醇不是简单的物理溶解,而是伴随着化学变化,生成硫酸乙酯和硫酸二乙酯,请写出乙醇和硫酸反应生成硫酸二乙酯的方程式2C2H5OH+H2SO4→(OC2H5)2SO2+2H2O.(3)合成乙酸乙酯的反应为放热反应.实验研究表明,反应温度应控制在85℃左右为宜.请根据反应原理分析温度控制的原因:温度低,反应速率低,达不到催化剂活性温度,温度过高;温度过高,利于平衡逆向移动,酯产率降低.
(4)反应完成后,得到粗产品进行除杂.
①把锥形瓶中的粗产品转移到分液漏斗中,加适量的饱和Na2CO3溶液,充分振荡静置,分离时,乙酸乙酯应该从仪器上口倒出(填“下口放出”或“上口倒出”).查阅资料,
相关物质的部分性质:
| 乙醇 | 乙酸 | 乙酸乙酯 | |
| 沸点 | 78.0℃ | 117.9℃ | 77.5℃ |
| 水溶性 | 易溶 | 易溶 | 难溶 |
②为了得到纯度高的产品,一般在①中得到的乙酸乙酯用氯化钙除去其中少量的乙醇,最后用b(选填序号)进行干燥.
a、浓硫酸b、无水硫酸钠c、碱石灰.
6.实验室制乙酸乙酯得主要装置如图A所示,主要步骤①在a试管中按2:3:2的体积比配制浓硫酸、乙醇、乙酸的混合物;②按A图连接装置,使产生的蒸气经导管通到b试管所盛的饱和碳酸钠溶液(加入几滴酚酞试液)中;③小火加热a试管中的混合液;④等b试管中收集到约2mL产物时停止加热.撤下b试管并用力振荡,然后静置待其中液体分层;⑤分离出纯净的乙酸乙酯.
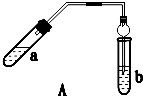
请回答下列问题:
(1)步骤④中可观察到b试管中有细小的气泡冒出,写出该反应的离子方程式:2CH3COOH+CO32-=2CH3COO-+H2O+CO2↑.
(2)A装置中使用球形管除起到冷凝作用外,另一重要作用是防止倒吸,步骤⑤中分离乙酸乙酯必须使用的一种仪器是分液漏斗.
(3)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图A所示装置进行了以下4个实验.实验开始先用酒精灯微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管b再测有机层的厚度,实验记录如下:
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用.实验D中应加入盐酸的体积和浓度分别是6mL和6mol•L-1.
②分析实验AC(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率.浓硫酸的吸水性能够提高乙酸乙酯产率的原因是浓硫酸可以吸收酯化反应中生成的水,降低了生成物浓度使平衡向生成乙酸乙酯的方向移动.
③加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,可能的原因是大量乙酸、乙醇未经反应就脱离反应体系(或温度过高发生其他反应).
④分离出乙酸乙酯层后,经过洗涤,为了干燥乙酸乙酯可选用的干燥剂为B(填字母).
A.P2O5 B.无水Na2SO4 C.碱石灰 D.NaOH固体.

请回答下列问题:
(1)步骤④中可观察到b试管中有细小的气泡冒出,写出该反应的离子方程式:2CH3COOH+CO32-=2CH3COO-+H2O+CO2↑.
(2)A装置中使用球形管除起到冷凝作用外,另一重要作用是防止倒吸,步骤⑤中分离乙酸乙酯必须使用的一种仪器是分液漏斗.
(3)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图A所示装置进行了以下4个实验.实验开始先用酒精灯微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管b再测有机层的厚度,实验记录如下:
| 实验 编号 | 试管a中试剂 | 试管b中试剂 | 测得有机层的厚度/cm |
| A | 3 mL乙醇、2 mL乙酸、1mL 18mol•L-1 浓硫酸 | 饱和Na2CO3溶液 | 5.0 |
| B | 3 mL乙醇、2 mL乙酸 | 0.1 | |
| C | 3 mL乙醇、2 mL乙酸、6 mL 3mol•L-1 H2SO4 | 1.2 | |
| D | 3 mL乙醇、2 mL乙酸、盐酸 | 1.2 |
②分析实验AC(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率.浓硫酸的吸水性能够提高乙酸乙酯产率的原因是浓硫酸可以吸收酯化反应中生成的水,降低了生成物浓度使平衡向生成乙酸乙酯的方向移动.
③加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,可能的原因是大量乙酸、乙醇未经反应就脱离反应体系(或温度过高发生其他反应).
④分离出乙酸乙酯层后,经过洗涤,为了干燥乙酸乙酯可选用的干燥剂为B(填字母).
A.P2O5 B.无水Na2SO4 C.碱石灰 D.NaOH固体.
5.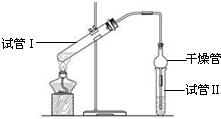 乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室利用如图的装置制备乙酸乙酯.
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室利用如图的装置制备乙酸乙酯.
(1)与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是:冷凝和防止倒吸.
(2)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验.实验开始先用酒精灯微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如下:
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用.实验D中应加入盐酸的体积和浓度分别是3mL和4mol•L-1.
②分析实验A C(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率.
(3)若现有乙酸90g,乙醇138g发生酯化反应得到80g乙酸乙酯,试计算该反应的产率为60.6%.
0 159785 159793 159799 159803 159809 159811 159815 159821 159823 159829 159835 159839 159841 159845 159851 159853 159859 159863 159865 159869 159871 159875 159877 159879 159880 159881 159883 159884 159885 159887 159889 159893 159895 159899 159901 159905 159911 159913 159919 159923 159925 159929 159935 159941 159943 159949 159953 159955 159961 159965 159971 159979 203614
 乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室利用如图的装置制备乙酸乙酯.
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室利用如图的装置制备乙酸乙酯.(1)与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是:冷凝和防止倒吸.
(2)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验.实验开始先用酒精灯微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如下:
| 实验编号 | 试管Ⅰ中试剂 | 试管Ⅱ中试剂 | 有机层的 厚度/cm |
| A | 2mL乙醇、1mL乙酸、 1mL18mol•L-1 浓硫酸 | 饱和Na2CO3 溶液 | 3.0 |
| B | 2mL乙醇、1mL乙酸 | 0.1 | |
| C | 2mL乙醇、1mL乙酸、 3mL 2mol•L-1 H2SO4 | 0.6 | |
| D | 2mL乙醇、1mL乙酸、盐酸 | 0.6 |
②分析实验A C(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率.
(3)若现有乙酸90g,乙醇138g发生酯化反应得到80g乙酸乙酯,试计算该反应的产率为60.6%.
 如右图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀.在右试管中加入5mL饱和Na2CO3溶液.按图连接好装置,用酒精灯对右试管小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.
如右图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀.在右试管中加入5mL饱和Na2CO3溶液.按图连接好装置,用酒精灯对右试管小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.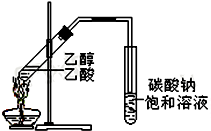 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯.回答下列问题: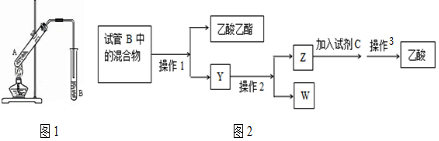
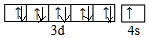 .
.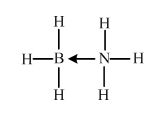 (必须标明配位键).
(必须标明配位键).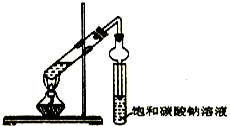 某同学用下列所示实验装置制取乙酸乙酯.回答以下问题:
某同学用下列所示实验装置制取乙酸乙酯.回答以下问题: