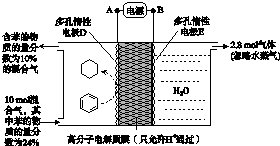
13.已知A(g)+B(g)?C (g)+D(g)反应的平衡常数和温度的关系如表:
回答下列问题:
(1)该反应的平衡常数表达式K=$\frac{c(C)c(D)}{c(A)c(B)}$,△H<0(填“<”“>”“=”);
(2)830°C时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003mol•L-1•s-1,则6s时c(A)=0.022mol•L-1,C的物质的量为0.09mol;若反应经一段时间后,达到平衡时A的转化率为80%
(3)判断该反应是否达到平衡的依据为c(填正确选项前的字母);
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时间改变 d.单位时间里生成C和D的物质的量相等
(4)1200°C时反应C(g)+D(g)?A(g)+B(g)的平衡常数的值为2.5.
| 温度/°C | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的平衡常数表达式K=$\frac{c(C)c(D)}{c(A)c(B)}$,△H<0(填“<”“>”“=”);
(2)830°C时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003mol•L-1•s-1,则6s时c(A)=0.022mol•L-1,C的物质的量为0.09mol;若反应经一段时间后,达到平衡时A的转化率为80%
(3)判断该反应是否达到平衡的依据为c(填正确选项前的字母);
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时间改变 d.单位时间里生成C和D的物质的量相等
(4)1200°C时反应C(g)+D(g)?A(g)+B(g)的平衡常数的值为2.5.
12.MnO2是-种重要的无机功能材料,工业上从锰结核中制取纯净的MnO2工艺流程如图所示:
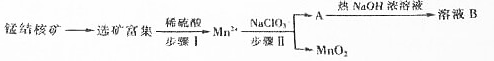
部分难容的电解质浓度积常数(Ksp)如下表:
已知,一定条件下.MnO4-可与Mn2+反应生成MnO2
(1)步骤Ⅱ中消耗0.5molMn2+时,用去1mol•L-1的NaClO3溶液200mL.该反应离子方程式为2ClO3-+5Mn2++4H2O=5MnO2+8H++Cl2↑
(2)已知溶液B的溶质之一可循环用于上述生产,此物质的名称是氯酸钠
(3)MnO2是碱性锌锰电池的正极材料.放电过程产生MnOOH,该电池正极的电极反应式是MnO2+H2O+e-═MnOOH+OH-.如果维持电流强度为5A,电池工作5分钟,理论消耗锌0.5g(已知F=96500C/mol)
(4)向废旧锌锰电池内的混合物(主要成分MnOOH,Zn(OH)2)中加入一定量的稀硫酸和稀草酸(H2C2O4),并不断搅拌至无CO2产生为止,写出MnOOH参与反应的离子方程式为2MnOOH+H2C2O4+2H2SO4=2CO2↑+2MnSO4+4H2O.向所的溶液中滴加高锰酸钾溶液产生黑色沉淀,设计实验证明黑色陈定成分为MnO2取少量黑色固体放入试管中,加入少量浓盐酸并加热,产生黄绿色气体,说明黑色固体为MnO2
(5)用废旧电池的锌皮制作ZnSO4•7H2O的过程中,需除去锌皮中少量的杂质铁,其方法是:加入稀H2SO4和H2O2,铁溶解变为Fe3+,加碱调pH为2.7时,铁刚好沉淀完全(离子浓度小于1×10-5mol•L-1时,即可认为该离子沉淀完全).继续调节pH为6时,锌开始沉淀(假定Zn2+浓度为0.1mol•L-1).若上述过程不加H2O2,其后果和原因是Zn(OH)2、Fe(OH)2的Ksp相近,Zn2+和Fe2+分离不开.
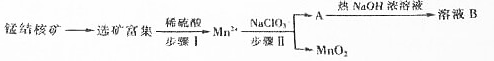
部分难容的电解质浓度积常数(Ksp)如下表:
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
(1)步骤Ⅱ中消耗0.5molMn2+时,用去1mol•L-1的NaClO3溶液200mL.该反应离子方程式为2ClO3-+5Mn2++4H2O=5MnO2+8H++Cl2↑
(2)已知溶液B的溶质之一可循环用于上述生产,此物质的名称是氯酸钠
(3)MnO2是碱性锌锰电池的正极材料.放电过程产生MnOOH,该电池正极的电极反应式是MnO2+H2O+e-═MnOOH+OH-.如果维持电流强度为5A,电池工作5分钟,理论消耗锌0.5g(已知F=96500C/mol)
(4)向废旧锌锰电池内的混合物(主要成分MnOOH,Zn(OH)2)中加入一定量的稀硫酸和稀草酸(H2C2O4),并不断搅拌至无CO2产生为止,写出MnOOH参与反应的离子方程式为2MnOOH+H2C2O4+2H2SO4=2CO2↑+2MnSO4+4H2O.向所的溶液中滴加高锰酸钾溶液产生黑色沉淀,设计实验证明黑色陈定成分为MnO2取少量黑色固体放入试管中,加入少量浓盐酸并加热,产生黄绿色气体,说明黑色固体为MnO2
(5)用废旧电池的锌皮制作ZnSO4•7H2O的过程中,需除去锌皮中少量的杂质铁,其方法是:加入稀H2SO4和H2O2,铁溶解变为Fe3+,加碱调pH为2.7时,铁刚好沉淀完全(离子浓度小于1×10-5mol•L-1时,即可认为该离子沉淀完全).继续调节pH为6时,锌开始沉淀(假定Zn2+浓度为0.1mol•L-1).若上述过程不加H2O2,其后果和原因是Zn(OH)2、Fe(OH)2的Ksp相近,Zn2+和Fe2+分离不开.
10.某研究性学习小组做铜与浓硫酸反应的探究实验:
①加热过程中发现试管底部有黑色颗粒状物质,后来逐渐转变为灰白色固体;
②倒去试管中的液体后,将残余固体(表面含有少量浓硫酸)倒入少量水中,发现溶液变蓝;并有黑色固体残余;③将②残余黑色固体过滤、洗涤后,向黑色固体中加入过量浓硝酸并加热,固体溶解,溶液变蓝;
④向③所得溶液中加入BaCl2溶液有白色沉淀产生.
下列结论不正确的是( )
0 159755 159763 159769 159773 159779 159781 159785 159791 159793 159799 159805 159809 159811 159815 159821 159823 159829 159833 159835 159839 159841 159845 159847 159849 159850 159851 159853 159854 159855 159857 159859 159863 159865 159869 159871 159875 159881 159883 159889 159893 159895 159899 159905 159911 159913 159919 159923 159925 159931 159935 159941 159949 203614
①加热过程中发现试管底部有黑色颗粒状物质,后来逐渐转变为灰白色固体;
②倒去试管中的液体后,将残余固体(表面含有少量浓硫酸)倒入少量水中,发现溶液变蓝;并有黑色固体残余;③将②残余黑色固体过滤、洗涤后,向黑色固体中加入过量浓硝酸并加热,固体溶解,溶液变蓝;
④向③所得溶液中加入BaCl2溶液有白色沉淀产生.
下列结论不正确的是( )
| A. | 铜与浓硫酸反应生成的白色固体是CuSO4 | |
| B. | ①中灰白色固体不可能含有CuO | |
| C. | ②中的黑色固体可能含有CuS或Cu2S | |
| D. | ④中所得的白色沉淀是BaSO3 |
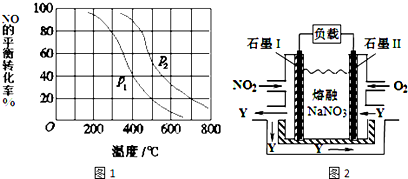

 氮化铝(AlN)是一种人工合成的非氧化物陶瓷材料,可在温度高于1500℃时,通过碳热还原法制得.实验研究认为,该碳热还原反应分两步进行:
氮化铝(AlN)是一种人工合成的非氧化物陶瓷材料,可在温度高于1500℃时,通过碳热还原法制得.实验研究认为,该碳热还原反应分两步进行: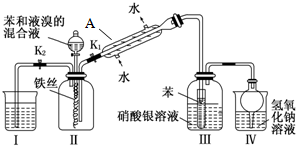
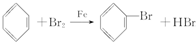
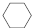 (g)$?_{高温}^{Pt-Sn/Al_{2}O_{3}}$
(g)$?_{高温}^{Pt-Sn/Al_{2}O_{3}}$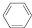 (g)+3H2(g).
(g)+3H2(g).