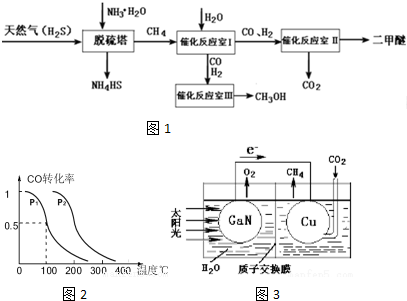
14. 图象法是研究化学反应的焓变的一种常用方法.已知化学反应A2(g)+B2(g)═2AB(g)的能量变化曲线如图所示,则下列叙述中正确的是( )
图象法是研究化学反应的焓变的一种常用方法.已知化学反应A2(g)+B2(g)═2AB(g)的能量变化曲线如图所示,则下列叙述中正确的是( )
 图象法是研究化学反应的焓变的一种常用方法.已知化学反应A2(g)+B2(g)═2AB(g)的能量变化曲线如图所示,则下列叙述中正确的是( )
图象法是研究化学反应的焓变的一种常用方法.已知化学反应A2(g)+B2(g)═2AB(g)的能量变化曲线如图所示,则下列叙述中正确的是( )| A. | 每生成2 mol AB时吸收(a-b) kJ能量 | |
| B. | 该反应热△H=+(a-b) kJ•mol-1 | |
| C. | 该反应中反应物的总能量高于生成物的总能量 | |
| D. | 断裂1 mol A-A和1 mol B-B键时放出a kJ能量 |
12.“材料“的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有里程碑式划时代的意义.请回答下列问题:
Ⅰ.(1)石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其组成为CaO•3MgO•4SiO2.
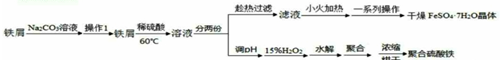
(2)高分子材料可以分成无机高分子材料和有机高分子材料.[AlFe(OH)nCl6-n]m属于无机高分子材料,是一种新型高效净水剂,它广泛应用于生活用水和工业污水的处理,其中铁元素的化合价为+3.
Ⅱ.高纯二氧化硅可用来制造光纤.某稻壳灰的成分如下表:
通过如下流程可由稻壳灰制备较纯净的二氧化硅: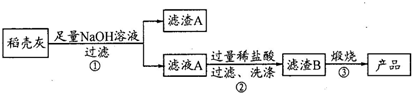
请回答下列问题:
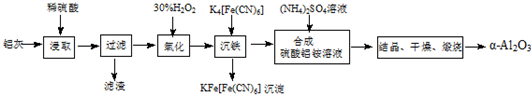
(1)根据氧化物的性质进行分类,稻壳灰中涉及的氧化物的种类最多有3类,其中SiO2为酸性氧化物(填氧化物的类别)
(2)滤渣A的成分有C和Fe2O3填化学式)
(3)步骤②洗涤沉淀的方法是向漏斗中加水至浸没沉淀,待水自然流下后,再重复2-3次
(4)步骤③反应的化学方程式为:H2SiO3$\frac{\underline{\;\;△\;\;}}{\;}$SiO2+H2O;实验室进行步骤③用到的仪器有坩埚、泥三角、酒精灯、坩埚钳和三脚架.
Ⅰ.(1)石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其组成为CaO•3MgO•4SiO2.
(2)高分子材料可以分成无机高分子材料和有机高分子材料.[AlFe(OH)nCl6-n]m属于无机高分子材料,是一种新型高效净水剂,它广泛应用于生活用水和工业污水的处理,其中铁元素的化合价为+3.
Ⅱ.高纯二氧化硅可用来制造光纤.某稻壳灰的成分如下表:
| 组分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
| 质量分数/% | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.61 |

请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中涉及的氧化物的种类最多有3类,其中SiO2为酸性氧化物(填氧化物的类别)
(2)滤渣A的成分有C和Fe2O3填化学式)
(3)步骤②洗涤沉淀的方法是向漏斗中加水至浸没沉淀,待水自然流下后,再重复2-3次
(4)步骤③反应的化学方程式为:H2SiO3$\frac{\underline{\;\;△\;\;}}{\;}$SiO2+H2O;实验室进行步骤③用到的仪器有坩埚、泥三角、酒精灯、坩埚钳和三脚架.
10. 实验室制备1,2二溴乙烷的反应原理如下:
实验室制备1,2二溴乙烷的反应原理如下:
CH3CH2OH$→_{170℃}^{H_{2}SO_{4}(浓)}$CH2═CH2
CH2═CH2+Br2-→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如图所示:
有关数据列表如下:
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是d;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
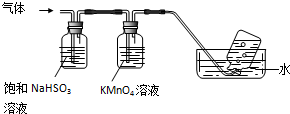
(2)在装置C中应加入c,其目的是吸收反应中可能生成的酸性气体;(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去;
(4)将1,2二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”或“下”);
(5)若产物中有少量未反应的Br2,最好用b洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚,可用蒸馏的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是1,2二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.
 实验室制备1,2二溴乙烷的反应原理如下:
实验室制备1,2二溴乙烷的反应原理如下:CH3CH2OH$→_{170℃}^{H_{2}SO_{4}(浓)}$CH2═CH2
CH2═CH2+Br2-→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如图所示:
有关数据列表如下:
| 乙醇 | 1,2二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是d;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入c,其目的是吸收反应中可能生成的酸性气体;(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去;
(4)将1,2二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”或“下”);
(5)若产物中有少量未反应的Br2,最好用b洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚,可用蒸馏的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是1,2二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.
5.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K和温度T的关系如表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$.
(2)该反应为吸热反应(选填“吸热”、“放热”).
(3)能判断该反应是否达到化学平衡状态的依据是cd(多选扣分).
a.容器中压强不变
b.c(CO2)=c(CO)
c.υ正(H2)=υ逆(H2O)
d.混合气体中c(CO)不变
(4)830K时,各物质浓度符合下式:c(CO2)•c(H2)=2c(CO)•c(H2O),此时该反应正反应方向进行(填“正反应方向进行”、“逆反应方向进行”或“处于平衡状态”).
0 159733 159741 159747 159751 159757 159759 159763 159769 159771 159777 159783 159787 159789 159793 159799 159801 159807 159811 159813 159817 159819 159823 159825 159827 159828 159829 159831 159832 159833 159835 159837 159841 159843 159847 159849 159853 159859 159861 159867 159871 159873 159877 159883 159889 159891 159897 159901 159903 159909 159913 159919 159927 203614
| T(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$.
(2)该反应为吸热反应(选填“吸热”、“放热”).
(3)能判断该反应是否达到化学平衡状态的依据是cd(多选扣分).
a.容器中压强不变
b.c(CO2)=c(CO)
c.υ正(H2)=υ逆(H2O)
d.混合气体中c(CO)不变
(4)830K时,各物质浓度符合下式:c(CO2)•c(H2)=2c(CO)•c(H2O),此时该反应正反应方向进行(填“正反应方向进行”、“逆反应方向进行”或“处于平衡状态”).