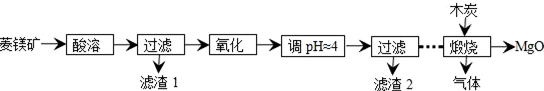
14.下列图象(如图)分别表示有关反应的反应过程与能量变化的关系.( )
| A. |  由如图知,石墨转变为金刚石是放热反应 | |
| B. |  由如图知,S(g)+O2(g)═SO2(g)△H1,S(s)+O2(g)═SO2(g)△H2则△H1<△H2 | |
| C. |  由如图知,白磷比红磷稳定 | |
| D. |  如由图知,CO(g)+H2O(g)═CO2(g)+H2(g)△H>0 |
13.乙酸环己酯具有香蕉及苹果气味,主要用于配制各种饮料、冰淇淋等,实验室制备乙酸环己酯的反应装置示意图和有关数据如图1:
实验步骤:
将12.0g(0.2mol)乙酸、10.0g(0.1mol)环已醇和15mL 环已烷加入装有温度计、恒压滴液漏斗和球形冷凝管的四颈烧瓶中,在搅拌下,慢慢滴加15mL98% 浓硫酸,恒压滴液漏斗换成分水器装置,加热回流90min,将反应液依次加水、10%的NaHCO3溶液、水洗涤,然后加无水MgSO4,放置过夜,加热蒸馏,收集168~174℃的馏分,得到无色透明有香味的液体,得产品6.9g
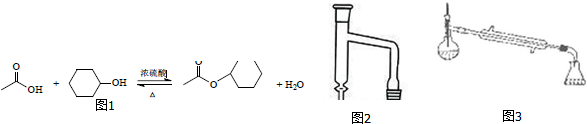
(1)上述反应装置图2中存在的一处错误是冷凝水应从下口进上口出.
(2)实验中控制乙酸的物质的量是环已醇的2 倍,其目的是提高环已醇的转化率.
(3)使用分水器(图3)的目的是将生成的水及时从体系中分离出来,提高反应物的转化率.
(4)用10%的NaHCO3溶液目的是洗去硫酸和醋酸;第二次水洗 的目的是洗去碳酸氢钠;加入无水MgSO4的目的是干燥.
(5)本次实验产率为48.6%.
(6)若在进行蒸馏操作时,采用图3装置,会使实验的产率偏高 (填“偏高”“偏低”“无影响”),其原因是产品中会收集到未反应的环己醇.
 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 水中溶解性 | |
| 乙酸 | 60 | 1.051 | 118.0 | 溶 | |
| 环己醇 | 100 | 0.982 | 160.8 | 微溶 | |
| 乙酸环己酯 | 142 | 0.969 | 173.5 | 难溶 |
将12.0g(0.2mol)乙酸、10.0g(0.1mol)环已醇和15mL 环已烷加入装有温度计、恒压滴液漏斗和球形冷凝管的四颈烧瓶中,在搅拌下,慢慢滴加15mL98% 浓硫酸,恒压滴液漏斗换成分水器装置,加热回流90min,将反应液依次加水、10%的NaHCO3溶液、水洗涤,然后加无水MgSO4,放置过夜,加热蒸馏,收集168~174℃的馏分,得到无色透明有香味的液体,得产品6.9g

(1)上述反应装置图2中存在的一处错误是冷凝水应从下口进上口出.
(2)实验中控制乙酸的物质的量是环已醇的2 倍,其目的是提高环已醇的转化率.
(3)使用分水器(图3)的目的是将生成的水及时从体系中分离出来,提高反应物的转化率.
(4)用10%的NaHCO3溶液目的是洗去硫酸和醋酸;第二次水洗 的目的是洗去碳酸氢钠;加入无水MgSO4的目的是干燥.
(5)本次实验产率为48.6%.
(6)若在进行蒸馏操作时,采用图3装置,会使实验的产率偏高 (填“偏高”“偏低”“无影响”),其原因是产品中会收集到未反应的环己醇.
8.某化学小组以苯甲酸( )为原料,制取苯甲酸甲酯.已知有关物质的沸点如表:
)为原料,制取苯甲酸甲酯.已知有关物质的沸点如表:
Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入12.2g苯甲酸(M=122g/mol)和20ml甲醇(密度约0.79g•mL-1 ),再小心加入3mL浓硫酸,混匀后,投入几粒碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品.
(1)若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式C6H5CO18OH+CH3OH $\frac{\underline{\;浓硫酸\;}}{△}$C6H5COOCH3+H218O;浓硫酸的作用是:催化剂、吸水剂.
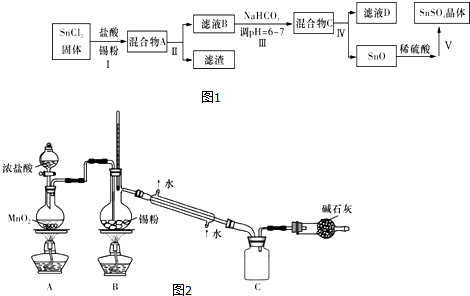
(2)甲、乙、丙三位同学分别设计了如图三套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去).根据有机物的沸点,最好采用乙装置(填“甲”或“乙”或“丙”).
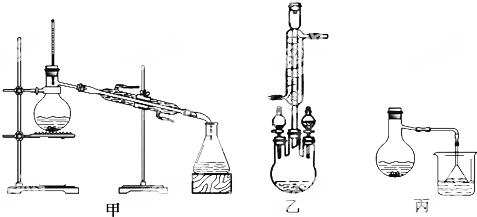
Ⅱ.粗产品的精制
(3)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用下列流程进行精制,请根据流程图写出操作方法的名称.操作Ⅰ分液 操作Ⅱ蒸馏.

(4)能否用NaOH溶液代替饱和碳酸钠溶液?否(填“能”或“否”),并简述原因氢氧化钠是强碱,促进苯甲酸甲酯的水解,导致产品损失.
(5)通过计算,苯甲酸甲酯的产率是65% .
 )为原料,制取苯甲酸甲酯.已知有关物质的沸点如表:
)为原料,制取苯甲酸甲酯.已知有关物质的沸点如表:| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 64.7 | 249 | 199.6 |
在圆底烧瓶中加入12.2g苯甲酸(M=122g/mol)和20ml甲醇(密度约0.79g•mL-1 ),再小心加入3mL浓硫酸,混匀后,投入几粒碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品.
(1)若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式C6H5CO18OH+CH3OH $\frac{\underline{\;浓硫酸\;}}{△}$C6H5COOCH3+H218O;浓硫酸的作用是:催化剂、吸水剂.
(2)甲、乙、丙三位同学分别设计了如图三套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去).根据有机物的沸点,最好采用乙装置(填“甲”或“乙”或“丙”).

Ⅱ.粗产品的精制
(3)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用下列流程进行精制,请根据流程图写出操作方法的名称.操作Ⅰ分液 操作Ⅱ蒸馏.

(4)能否用NaOH溶液代替饱和碳酸钠溶液?否(填“能”或“否”),并简述原因氢氧化钠是强碱,促进苯甲酸甲酯的水解,导致产品损失.
(5)通过计算,苯甲酸甲酯的产率是65% .
7.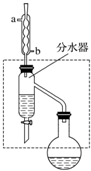 乙酸丁酯是重要的化工原料,具有水果香味.实验室制备乙酸丁酯的反应、装置示意图和有关信息如下:
乙酸丁酯是重要的化工原料,具有水果香味.实验室制备乙酸丁酯的反应、装置示意图和有关信息如下:
CH3COOH+CH3CH2CH2CH2OH$?_{浓H_{2}SO_{4}}^{△}$ CH3COOCH2CH2CH2CH3+H2O
(1)乙酸丁酯粗产品的制备
在干燥的50mL圆底烧瓶中,装入沸石,加入12.0mL正丁醇和16.0mL冰醋酸(过量),再加3~4滴浓硫酸.然后再安装分水器(作用:实验过程中不断分离除去反应生成的水)、冷凝管,然后小火加热.将烧瓶中反应后的混合物冷却与分水器的酯层合并.装置中冷水应从b(填“a”或“b”)口通入;通过分水器不断分离除去反应生成的水的目的是分离生成的水,使平衡正向移动,提高反应产率.
(2)乙酸丁酯的精制
将乙酸丁酯粗产品用如下的操作进行精制:①水洗、②蒸馏、③用无水MgSO4干燥、④用10%碳酸钠洗涤.
①正确的操作步骤是c(填标号).
A.①②③④B.③①④②C.④①③②D.③④①②
②在乙酸丁酯的精制中,用10%碳酸钠洗涤的主要目的是除去产品中含有的乙酸、硫酸等杂质.
③在洗涤、分液操作中,应充分振荡,然后静置,待分层后d(填标号).
a.直接将乙酸丁酯从分液漏斗的上口倒出
b.直接将乙酸丁酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸丁酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸丁酯从上口倒出
(3)计算产率
测量分水器内由乙酸与丁醇反应生成的水体积为1.8mL,假设在制取乙酸丁酯过程中反应物和生成物没有损失,且忽略副反应,乙酸丁酯的产率为77.1%.
 乙酸丁酯是重要的化工原料,具有水果香味.实验室制备乙酸丁酯的反应、装置示意图和有关信息如下:
乙酸丁酯是重要的化工原料,具有水果香味.实验室制备乙酸丁酯的反应、装置示意图和有关信息如下:CH3COOH+CH3CH2CH2CH2OH$?_{浓H_{2}SO_{4}}^{△}$ CH3COOCH2CH2CH2CH3+H2O
| 乙酸 | 正丁醇 | 乙酸丁酯 | |
| 熔点/℃ | 16.6 | -89.5 | -73.5 |
| 沸点/℃ | 117.9 | 117 | 126.0 |
| 密度/g•cm-3 | 1.1 | 0.80 | 0.88 |
在干燥的50mL圆底烧瓶中,装入沸石,加入12.0mL正丁醇和16.0mL冰醋酸(过量),再加3~4滴浓硫酸.然后再安装分水器(作用:实验过程中不断分离除去反应生成的水)、冷凝管,然后小火加热.将烧瓶中反应后的混合物冷却与分水器的酯层合并.装置中冷水应从b(填“a”或“b”)口通入;通过分水器不断分离除去反应生成的水的目的是分离生成的水,使平衡正向移动,提高反应产率.
(2)乙酸丁酯的精制
将乙酸丁酯粗产品用如下的操作进行精制:①水洗、②蒸馏、③用无水MgSO4干燥、④用10%碳酸钠洗涤.
①正确的操作步骤是c(填标号).
A.①②③④B.③①④②C.④①③②D.③④①②
②在乙酸丁酯的精制中,用10%碳酸钠洗涤的主要目的是除去产品中含有的乙酸、硫酸等杂质.
③在洗涤、分液操作中,应充分振荡,然后静置,待分层后d(填标号).
a.直接将乙酸丁酯从分液漏斗的上口倒出
b.直接将乙酸丁酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸丁酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸丁酯从上口倒出
(3)计算产率
测量分水器内由乙酸与丁醇反应生成的水体积为1.8mL,假设在制取乙酸丁酯过程中反应物和生成物没有损失,且忽略副反应,乙酸丁酯的产率为77.1%.
6.实验室以含有Ca2+、Mg2+、Cl-、SO42-、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,流程如下:

(1)操作Ⅰ使用的试剂是CCl4,所用主要仪器的名称是分液漏斗.
(2)加入溶液W的目的是除去溶液中的SO42-.
用CaO调节溶液Y的pH,可以除去Mg2+.由表中数据可知,理论上可选择pH最大范围是11.0≤pH<12.2.
酸化溶液Z时,使用的试剂为盐酸.
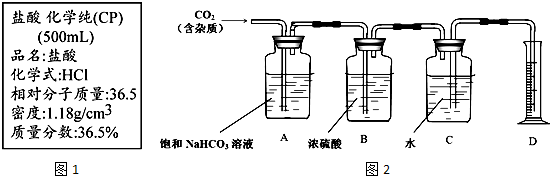
(3)实验室用贝壳与稀盐酸反应制备并收集CO2气体,下列装置中合理的是bd.
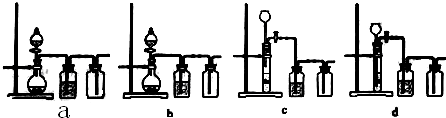
(4)工业上由熔融MgCl2制Mg,写出化学方程式MgCl2$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑.
(5)化学使生活更美好,下列做法不可行的是AF.
A.用活性炭检验软、硬水 B.用食醋除铁锈
C.用小苏打片治疗胃酸过多 D.用生石灰作食品干燥剂
E.乙烯可以作水果催熟剂 F.福尔马林可以作食品保鲜剂.
0 159731 159739 159745 159749 159755 159757 159761 159767 159769 159775 159781 159785 159787 159791 159797 159799 159805 159809 159811 159815 159817 159821 159823 159825 159826 159827 159829 159830 159831 159833 159835 159839 159841 159845 159847 159851 159857 159859 159865 159869 159871 159875 159881 159887 159889 159895 159899 159901 159907 159911 159917 159925 203614

(1)操作Ⅰ使用的试剂是CCl4,所用主要仪器的名称是分液漏斗.
(2)加入溶液W的目的是除去溶液中的SO42-.
用CaO调节溶液Y的pH,可以除去Mg2+.由表中数据可知,理论上可选择pH最大范围是11.0≤pH<12.2.
酸化溶液Z时,使用的试剂为盐酸.
| 开始沉淀时的pH | 沉淀完全时的pH | |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OH-)=1.8mol•L-1 |

(4)工业上由熔融MgCl2制Mg,写出化学方程式MgCl2$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑.
(5)化学使生活更美好,下列做法不可行的是AF.
A.用活性炭检验软、硬水 B.用食醋除铁锈
C.用小苏打片治疗胃酸过多 D.用生石灰作食品干燥剂
E.乙烯可以作水果催熟剂 F.福尔马林可以作食品保鲜剂.