3. 甲醚作为一种基本化工原料,由于其良好的易压缩、冷凝、汽化特性,使甲醚在制药、燃料、农药等化学工业中有许多独特的用途.
甲醚作为一种基本化工原料,由于其良好的易压缩、冷凝、汽化特性,使甲醚在制药、燃料、农药等化学工业中有许多独特的用途.
已知:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-25kJ•mol-1,某温度下的平衡常数为400.此温度下,在1L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
①平衡时,c(CH3OCH3)等于1.6 mol•L-1,反应混合物的总能量减少40 kJ.
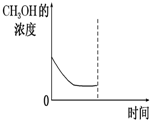
②若在平衡后的容器中再加入与起始时等量的CH3OH,请在下图中画出CH3OH的浓度的曲线示意图.
 甲醚作为一种基本化工原料,由于其良好的易压缩、冷凝、汽化特性,使甲醚在制药、燃料、农药等化学工业中有许多独特的用途.
甲醚作为一种基本化工原料,由于其良好的易压缩、冷凝、汽化特性,使甲醚在制药、燃料、农药等化学工业中有许多独特的用途.已知:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-25kJ•mol-1,某温度下的平衡常数为400.此温度下,在1L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| c(mol•L-1) | 0.8 | 1.24 | ? |
②若在平衡后的容器中再加入与起始时等量的CH3OH,请在下图中画出CH3OH的浓度的曲线示意图.
2.己知反应A(g)+B(g)?C(g)+D(g)的平衡常数K值与温度的关系如表所示.830℃时,向一个2L的密闭容器中充入0.20molA和0.80molB,4s内v(A)=0.005mol•L-1•S-1.下列说法正确的是( )
| 温度/℃ | 700 | 830 | 1200 |
| K值 | 1.7 | 1.0 | 0.4 |
| A. | 4s时,c(B)为0.76 mol•L-1 | |
| B. | 830℃到平衡时,A的转化率为80% | |
| C. | 达平衡时,升高温度,平衡正向移动 | |
| D. | 1200℃时反应C(g)+D(g)?A(g)+B(g)的平衡常数的值为0.4 |
1.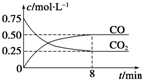 某温度下,在一密闭容器中充入一定量CO2,并加入足量铁粉,发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g),测得CO2和CO浓度随时间的变化如图所示:
某温度下,在一密闭容器中充入一定量CO2,并加入足量铁粉,发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g),测得CO2和CO浓度随时间的变化如图所示:
(1)0~8min,v(CO)=0.0625mol•L-1•min-1.
(2)下列措施中,能够改变平衡时c(CO)/c(CO2)的比值的是AD(填序号).
A.温度B.铁粉的量(足量)C.压强D.CO的量
(3)已知:反应Fe(s)+CO2(g)?FeO(s)+CO(g)的平衡常数为K1;
反应Fe(s)+H2O(g)?FeO(s)+H2(g)的平衡常数为K2.不同温度时K1、K2的值如下表:
根据表中数据,计算反应CO2(g)+H2(g)?CO(g)+H2O(g)的K.
①温度为973K时:K=0.62;
②温度为1173K时:K=1.29;
③反应CO2(g)+H2(g)?CO(g)+H2O(g)是吸热反应(填“吸热”或“放热”).
 某温度下,在一密闭容器中充入一定量CO2,并加入足量铁粉,发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g),测得CO2和CO浓度随时间的变化如图所示:
某温度下,在一密闭容器中充入一定量CO2,并加入足量铁粉,发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g),测得CO2和CO浓度随时间的变化如图所示:(1)0~8min,v(CO)=0.0625mol•L-1•min-1.
(2)下列措施中,能够改变平衡时c(CO)/c(CO2)的比值的是AD(填序号).
A.温度B.铁粉的量(足量)C.压强D.CO的量
(3)已知:反应Fe(s)+CO2(g)?FeO(s)+CO(g)的平衡常数为K1;
反应Fe(s)+H2O(g)?FeO(s)+H2(g)的平衡常数为K2.不同温度时K1、K2的值如下表:
| 温度/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
①温度为973K时:K=0.62;
②温度为1173K时:K=1.29;
③反应CO2(g)+H2(g)?CO(g)+H2O(g)是吸热反应(填“吸热”或“放热”).
20.化学在能源开发与利用中起着重要的作用,如甲醇、乙醇、二甲醚(CH3OCH3)等都是新型燃料.
(1)乙醇是重要的化工产品和液体燃料,可以利用下列反应制取乙醇.
2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)△H=a kJ/mol
在一定压强下,测得上述反应的实验数据如表.
根据表中数据分析:
①上述反应的a小于0(填“大于”或“小于”).
②在一定温度下,提高氢碳(即$\frac{n({H}_{2})}{n(C{O}_{2})}$)比,平衡常数K值不变(填“增大”、“减小”、或“不变”).
(2)催化剂存在的条件下,在固定容积的密闭容器中投入一定量的CO和H2,同样可制得乙醇(可逆反应).该反应过程中能量变化如图所示:
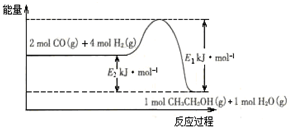
在一定温度下,向上述密闭容器中加入1mol CO、3mol H2及固体催化剂,使之反应.平衡时,反应产生的热量为Q kJ,若温度不变的条件下,向上述密闭容器中加入4mol CO、12mol H2及固体催化剂,平衡时,反应产生的热量为w kJ,则w的范围为4Q<w<2 (E2-E1).
(3)以乙醇蒸气、空气、氢氧化钠溶液为原料,石墨为电极可构成燃料电池,其工作原理与甲烷燃料电池原理相类似.该电池中负极上的电极反应式是CH3CH2OH-12e-+16OH-=2CO32-+11H2O.使用上述乙醇燃料电池电解(Pt电极)一定浓度的硫酸铜溶液通电一段时间后,向所得的溶液中加入0.1mol Cu(OH)2后恰好恢复到电解前的浓度和pH,则乙醇燃料电池在电解过程中转移电子数是0.4NA.
0 159730 159738 159744 159748 159754 159756 159760 159766 159768 159774 159780 159784 159786 159790 159796 159798 159804 159808 159810 159814 159816 159820 159822 159824 159825 159826 159828 159829 159830 159832 159834 159838 159840 159844 159846 159850 159856 159858 159864 159868 159870 159874 159880 159886 159888 159894 159898 159900 159906 159910 159916 159924 203614
(1)乙醇是重要的化工产品和液体燃料,可以利用下列反应制取乙醇.
2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)△H=a kJ/mol
在一定压强下,测得上述反应的实验数据如表.
| 温度/K CO2转化率% $\frac{n({H}_{2})}{n(C{O}_{2})}$ | 500 | 600 | 700 | 800 |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |
①上述反应的a小于0(填“大于”或“小于”).
②在一定温度下,提高氢碳(即$\frac{n({H}_{2})}{n(C{O}_{2})}$)比,平衡常数K值不变(填“增大”、“减小”、或“不变”).
(2)催化剂存在的条件下,在固定容积的密闭容器中投入一定量的CO和H2,同样可制得乙醇(可逆反应).该反应过程中能量变化如图所示:

在一定温度下,向上述密闭容器中加入1mol CO、3mol H2及固体催化剂,使之反应.平衡时,反应产生的热量为Q kJ,若温度不变的条件下,向上述密闭容器中加入4mol CO、12mol H2及固体催化剂,平衡时,反应产生的热量为w kJ,则w的范围为4Q<w<2 (E2-E1).
(3)以乙醇蒸气、空气、氢氧化钠溶液为原料,石墨为电极可构成燃料电池,其工作原理与甲烷燃料电池原理相类似.该电池中负极上的电极反应式是CH3CH2OH-12e-+16OH-=2CO32-+11H2O.使用上述乙醇燃料电池电解(Pt电极)一定浓度的硫酸铜溶液通电一段时间后,向所得的溶液中加入0.1mol Cu(OH)2后恰好恢复到电解前的浓度和pH,则乙醇燃料电池在电解过程中转移电子数是0.4NA.
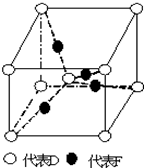 在周期表中1~36号之间的A、B、C、D、E、F六种元素,它们的原子序数依次增大,已知A与其余五种元素既不同周期也不同主族,B的一种核素在考古时常用来鉴定一些文物的年代,C元素原子的最外层有3个自旋方向相同的未成对电子,D原子核外电子有8种不同的运动状态,E元素在第四周期,E的基态原子中未成对电子数是核外电子总数的$\frac{1}{4}$,F元素位于周期表的ds区,其基态原子最外能层只有一个电子.
在周期表中1~36号之间的A、B、C、D、E、F六种元素,它们的原子序数依次增大,已知A与其余五种元素既不同周期也不同主族,B的一种核素在考古时常用来鉴定一些文物的年代,C元素原子的最外层有3个自旋方向相同的未成对电子,D原子核外电子有8种不同的运动状态,E元素在第四周期,E的基态原子中未成对电子数是核外电子总数的$\frac{1}{4}$,F元素位于周期表的ds区,其基态原子最外能层只有一个电子. .
.