17.某反应过程中能量变化如图,则该反应的△H值为( )


| A. | △H>0 | B. | △H<0 | C. | △H=0 | D. | 无法判断 |
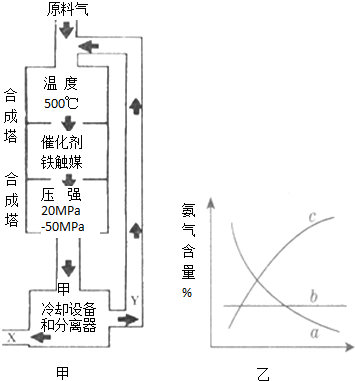
12.已知N2(g)+3H2(g)$?_{催化剂}^{高温高压}$2NH3(g)△H=-92.22kJ•mol-1.下列对该反应的说法正确的是.
| A. | 可利用该反应进行人工固氮 | |
| B. | 将3mol N2(g)和3mol H2(g)混合,在高温、高压和催化条件下充分反应,放出热量92.22kJ | |
| C. | 因为反应需要加热,所以反应放出热量 | |
| D. | 其他条件相同时,采用更高效的正催化剂,既能提高反应速率,又能增大反应放热量 |
11.下列说法中不正确的是( )
| A. | 在一定条件下,某可逆反应正向是吸热反应,则其逆向必是放热反应 | |
| B. | 1 mol A(强酸)与1 mol B(强碱)发生中和反应所放出的热量叫做中和热 | |
| C. | 二次电池充电时将电能转化为化学能 | |
| D. | 需要加热才能发生的反应可能是吸热反应也可能是放热反应 |
10.下列说法正确的是( )
| A. | 等质量的硫蒸气和硫固体分别在氧气中完全燃烧,后者放出的热量多 | |
| B. | 热化学方程式C2H2(g)+$\frac{5}{2}$O2(g)═2CO2(g)+H2O(g)△H=-1256 kJ•mol-1,可知乙炔的燃烧热为1256 kJ•mol-1 | |
| C. | 在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ•mol-1 | |
| D. | 稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,若将含0.5 molH2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ |
9.2014年初全国各地多个城市都遭遇“十面霾伏”,造成“阴霾天”的主要根源之一是汽车尾气和燃煤尾气排放出来的固体小颗粒.将汽车尾气通过排气管加装催化装置,可有效减少CO和NO的排放,催化装置内发生的反应为:2NO+2CO$\stackrel{催化剂}{?}$2CO2+N2,已知该反应属于放热反应.下列关于此反应的说法不正确的是( )
| A. | 该反应会放出热量 | |
| B. | 每生成1mol N2,转化电子数为4mol | |
| C. | 等物质的量N2和CO质量相同 | |
| D. | 该反应不需要催化剂常温下也能发生 |
8.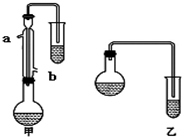 某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如下表:
某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如下表:
(1)甲和乙两位同学分别设计了如下图所示的两套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去).根据有机物的沸点,最好采用甲(填“甲”或“乙”)装置.理由是甲中有冷凝回流装置.
(2)实验中浓硫酸的作用是催化剂、吸水剂.
(3)反应物CH3OH应过量,理由是反应物CH3OH过量,使平衡向右移动,有利于提高苯甲酸的转化率.
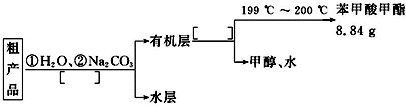
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图进行精制,请在流程图中方括号内填入操作方法的名称.
0 159697 159705 159711 159715 159721 159723 159727 159733 159735 159741 159747 159751 159753 159757 159763 159765 159771 159775 159777 159781 159783 159787 159789 159791 159792 159793 159795 159796 159797 159799 159801 159805 159807 159811 159813 159817 159823 159825 159831 159835 159837 159841 159847 159853 159855 159861 159865 159867 159873 159877 159883 159891 203614
 某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如下表:
某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如下表:| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 64.7 | 249 | 199.6 |
(2)实验中浓硫酸的作用是催化剂、吸水剂.
(3)反应物CH3OH应过量,理由是反应物CH3OH过量,使平衡向右移动,有利于提高苯甲酸的转化率.
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图进行精制,请在流程图中方括号内填入操作方法的名称.



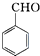 +KOH→
+KOH→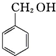 +
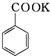
+
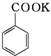 +HCl→
+HCl→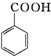 +KCl
+KCl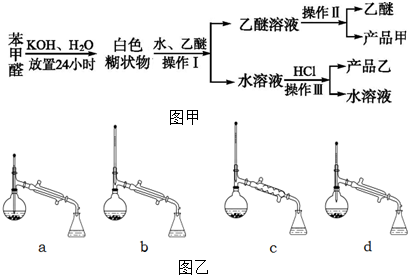
 利用所学化学知识解答问题:
利用所学化学知识解答问题: