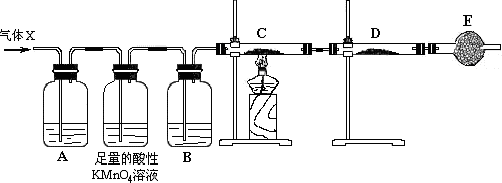
7.FeCl3是常见的水处理剂,实验室用铁屑制备无水FeCl3,制备步骤如下:
Ⅰ.称取一定量的铁屑于锥形瓶中,加入过量的6mol•L-1的盐酸,在通风橱中充分反应;
Ⅱ.根据FeCl2的理论产量,加入足量的氧化剂X;
Ⅲ.FeCl3溶液通过一系列操作制得无水FeCl3.
已知:不同温度下六水合FeCl3在水中的溶解度如下:
请回答:
(1)请选择本实验中合适的氧化剂XCD.
A.KMnO4(H+) B.稀硝酸 C.H2O2 D.Cl2
(2)从FeCl3溶液制得FeCl3•6H2O晶体的操作步骤是:
①加入盐酸后,②蒸发浓缩、冷却结晶,③过滤、洗涤,④干燥.
(3)过滤后用少量乙醇洗涤FeCl3•6H2O晶体,选用乙醇的原因是洗去晶体表面的水,减少氯化铁晶体的溶解损耗.
(4)FeCl3的质量分数通常可用碘量法测定:
称取m g无水FeCl3样品,溶于稀盐酸,配制成100mL溶液;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入几滴淀粉溶液,并用cmol•L-1Na2S2O3溶液滴定,消耗VmL(已知:I2+2S2O32-═2I-+S4O62-).
①配制FeCl3溶液所需的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还需100mL容量瓶;
②在FeCl3质量分数测定的实验过程中,下列说法正确的是CD.
A.润洗滴定管时,应从滴定管上口加满所需的酸或碱液,使滴定管内壁充分润洗
B.若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中FeCl3的质量分数的测量结果偏高
C.滴定时,左手轻轻向内扣住活塞,手心空握以免碰到活塞使其松动漏出溶液
D.滴定终点读取滴定管刻度时,仰视标准液液面,会使实验误差偏高
③滴定终点的现象是:溶液由蓝色变无色,且半分钟内不变色,样品中FeCl3的质量分数$\frac{162.5cV}{m}%$.
Ⅰ.称取一定量的铁屑于锥形瓶中,加入过量的6mol•L-1的盐酸,在通风橱中充分反应;
Ⅱ.根据FeCl2的理论产量,加入足量的氧化剂X;
Ⅲ.FeCl3溶液通过一系列操作制得无水FeCl3.
已知:不同温度下六水合FeCl3在水中的溶解度如下:
| 温度/℃ | 0 | 20 | 80 | 100 |
| 溶解度(g/100g H2O) | 74.4 | 91.8 | 525.8 | 535.7 |
(1)请选择本实验中合适的氧化剂XCD.
A.KMnO4(H+) B.稀硝酸 C.H2O2 D.Cl2
(2)从FeCl3溶液制得FeCl3•6H2O晶体的操作步骤是:
①加入盐酸后,②蒸发浓缩、冷却结晶,③过滤、洗涤,④干燥.
(3)过滤后用少量乙醇洗涤FeCl3•6H2O晶体,选用乙醇的原因是洗去晶体表面的水,减少氯化铁晶体的溶解损耗.
(4)FeCl3的质量分数通常可用碘量法测定:
称取m g无水FeCl3样品,溶于稀盐酸,配制成100mL溶液;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入几滴淀粉溶液,并用cmol•L-1Na2S2O3溶液滴定,消耗VmL(已知:I2+2S2O32-═2I-+S4O62-).
①配制FeCl3溶液所需的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还需100mL容量瓶;
②在FeCl3质量分数测定的实验过程中,下列说法正确的是CD.
A.润洗滴定管时,应从滴定管上口加满所需的酸或碱液,使滴定管内壁充分润洗
B.若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中FeCl3的质量分数的测量结果偏高
C.滴定时,左手轻轻向内扣住活塞,手心空握以免碰到活塞使其松动漏出溶液
D.滴定终点读取滴定管刻度时,仰视标准液液面,会使实验误差偏高
③滴定终点的现象是:溶液由蓝色变无色,且半分钟内不变色,样品中FeCl3的质量分数$\frac{162.5cV}{m}%$.
6.下列过程中△H小于零的是( )
| A. | 炽热的碳与二氧化碳的反应 | B. | 氯化铵分解得氨气 | ||
| C. | 碳酸钙分解得二氧化碳 | D. | Zn与硫酸的反应 |
5.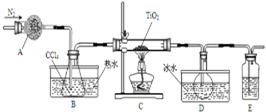 实验室利用反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下,有关物质性质如表.
实验室利用反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下,有关物质性质如表.
(1)仪器A的名称是干燥管,装置E中的试剂是浓硫酸.反应开始前依次进行如下操作:组装仪器、检验气密性、加装药品、通N2一段时间后点燃酒精灯.
(2)反应结束后的操作包括:a停止通N2 b熄灭酒精灯 c冷却至室温.正确的顺序为bca(填序号).选择这种顺序的理由是防止倒吸或避免生成的产物在受热情况下与氧气反应(二者任写其一均给分);欲分离D中的液态混合物,所采用操作的名称是蒸馏.
 实验室利用反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下,有关物质性质如表.
实验室利用反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下,有关物质性质如表.| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产白雾 |
(2)反应结束后的操作包括:a停止通N2 b熄灭酒精灯 c冷却至室温.正确的顺序为bca(填序号).选择这种顺序的理由是防止倒吸或避免生成的产物在受热情况下与氧气反应(二者任写其一均给分);欲分离D中的液态混合物,所采用操作的名称是蒸馏.
4.已知:CO(g)+2H2(g)?CH3OH(g)△H<0.其它条件不变的情况下,下列有关该反应的说法中正确的是( )
| A. | 升高温度可以提高CO的转化率 | |
| B. | 加入催化剂能提高CO的转化率 | |
| C. | 缩小反应器容积可以使平衡正向移动 | |
| D. | 再充入适量H2,该反应平衡常数的数值会增大 |
2.低温脱硝技术可用于处理废气中的氮氧化物,
发生的化学反应为:2NH3(g)+NO(g)+NO2(g)$?_{催化剂}^{180℃}$2N2(g)+3H2O(g) 正反应放热在恒容的密闭容器中,下列有关说法正确的是( )
发生的化学反应为:2NH3(g)+NO(g)+NO2(g)$?_{催化剂}^{180℃}$2N2(g)+3H2O(g) 正反应放热在恒容的密闭容器中,下列有关说法正确的是( )
| A. | 平衡时,其他条件不变,升高温度平衡正向移动 | |
| B. | 平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小 | |
| C. | 其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 | |
| D. | 单位时间内消耗NO和N2的物质的量比为1:2时,反应达到平衡 |
1.一定温度下,在一定容积固定的密闭容器中,建立了下列平衡:2NO2?N2O4,在此温度下,再向容器通入一定量NO2,重新建立平衡后,容器中NO2的体积分数( )
| A. | 减少 | B. | 增大 | ||
| C. | 不变 | D. | 无法判断变化情况 |
20.一定温度时,在容积可变的密闭容器中发生反应:X(g)+Y(g)?Z(?)+W(g),达到平衡后容积为V,压缩容积至0.5V,并保持容积不变,再次达到平衡时,X的浓度为原平衡状态的1.8倍,下列叙述正确是( )
| A. | 该条件下Z是气态 | B. | 平衡常数K=$\frac{c(Z)•c(W)}{c(X)•c(Y)}$ | ||
| C. | 增加Z平衡逆向移动 | D. | 上述过程中X的转化率变大 |
19.下列说法中正确的是( )
| A. | 改变外界条件不能改变化学反应的限度 | |
| B. | 当某反应在一定条件下达到反应限度时即达到化学平衡状态 | |
| C. | 浓度、压强、催化剂、温度等均能改变活化分子的百分数 | |
| D. | 能自发进行的反应其速率都很大 |
18.可逆反应2A(s)?C(g)+D(g)正向建立平衡后,维持其它条件不变,压缩容器的体积,下列说法正确的是( )
0 159694 159702 159708 159712 159718 159720 159724 159730 159732 159738 159744 159748 159750 159754 159760 159762 159768 159772 159774 159778 159780 159784 159786 159788 159789 159790 159792 159793 159794 159796 159798 159802 159804 159808 159810 159814 159820 159822 159828 159832 159834 159838 159844 159850 159852 159858 159862 159864 159870 159874 159880 159888 203614
| A. | 正逆反应速率都增大 | |
| B. | 平衡不移动 | |
| C. | 再次平衡时c(D) 不变 | |
| D. | C的体积分数不再变化说明再次达到平衡 |