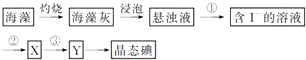
10.某元素X的气态氢化物的化学式为XH3,则X的最高价氧化物的水化物的化学式为( )
| A. | H2XO3 | B. | HXO3 | C. | HXO4 | D. | H2X |
9.下列有关元素周期律的叙述中,正确的是( )
| A. | 氧化性强弱:F2<Cl2 | B. | 金属性强弱:Al<Na | ||
| C. | 酸性强弱:H2CO3<HNO3 | D. | 碱性强弱:NaOH<Mg(OH)2 |
8.对发现元素周期律贡献最大的化学家是( )
| A. | 阿佛加德罗 | B. | 道尔顿 | C. | 牛顿 | D. | 门捷列夫 |
7.反应X(g)+Y(g)?2Z(g)△H<0,达到平衡时,下列说法正确的是( )
| A. | 减小容器体积,平衡向右移动 | |
| B. | 加入催化剂,平衡不移动故正逆反应速率不变 | |
| C. | 增大c(X),X的转化率增大 | |
| D. | 降低温度,Y的转化率增大 |
6.下列说法正确的是( )
| A. | 任何化学反应都伴随着能量的变化 | |
| B. | 升高温度或加入催化剂,可以改变化学反应的反应热 | |
| C. | 化学反应中的能量变化都是以热量的形式体现 | |
| D. | 2CO(g)+O2(g)═2CO2(g)△H<0,则56g CO和32g O2所具有的总能量小于88g CO2所具有的总能量 |
5.在恒温恒压下,向密闭容器中充入4mol SO2和2mol O2,发生如下反应:2SO2(g)+O2(g)?2SO3(g)△H<0.2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量Q kJ,则下列分析正确的是( )
| A. | 在该条件下,反应前后的压强之比为6:5.3 | |
| B. | 若反应开始时容器体积为2 L,则0~2 min内v(SO3)=0.35 mol/(L•min) | |
| C. | 若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)<1.4 mol | |
| D. | 若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出的热量大于Q kJ |
4.在容积固定的密闭容器中,对于反应2SO2(g)+O2(g)?2SO3(g)△H<0.下列判断正确的是( )
| A. | 增大反应体系的压强,平衡后SO2的浓度、转化率、体积分数都增加 | |
| B. | 当单位时间内消耗SO2的物质的量和生成SO3的物质的量相同时,反应达到平衡状态 | |
| C. | 充入SO3气体,体系压强增大,平衡向右移动 | |
| D. | 升高温度,平衡向左移动 |
3.向CH3COONa稀溶液中分别加入少量下列物质或改变如下条件,$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$一定减小的是( )
①NaOH固体②NaHSO4固体 ③氯化钠水溶液④CH3COONa固体 ⑤冰醋酸⑥降低温度.
0 159679 159687 159693 159697 159703 159705 159709 159715 159717 159723 159729 159733 159735 159739 159745 159747 159753 159757 159759 159763 159765 159769 159771 159773 159774 159775 159777 159778 159779 159781 159783 159787 159789 159793 159795 159799 159805 159807 159813 159817 159819 159823 159829 159835 159837 159843 159847 159849 159855 159859 159865 159873 203614
①NaOH固体②NaHSO4固体 ③氯化钠水溶液④CH3COONa固体 ⑤冰醋酸⑥降低温度.
| A. | ①③④ | B. | ②③⑤ | C. | ②⑤⑥ | D. | ①④⑥ |
 ,(3)MgO
,(3)MgO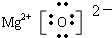 .
.