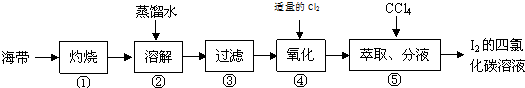
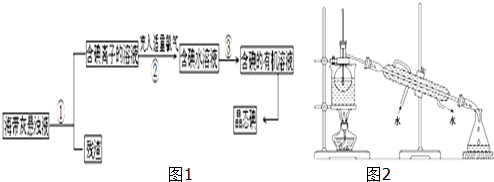
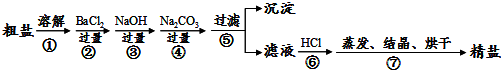
19.关于粗盐提纯下列说法中正确的是( )
| A. | 溶解粗盐时,应尽量让溶液稀些,防止食盐不完全溶解 | |
| B. | 滤去不溶性杂质后,将滤液移至坩埚内加热浓缩 | |
| C. | 将制得的晶体转移到新制过滤器中用大量水进行洗涤 | |
| D. | 当蒸发到剩余少量液体时,停止加热,利用余热将液体蒸干 |
18.为除去粗盐中的Ca2+、Mg2+、SO${\;}_{4}^{2-}$以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,(用于沉淀的试剂一般过量),其中所加试剂顺序不正确的一组是.( )
0 159668 159676 159682 159686 159692 159694 159698 159704 159706 159712 159718 159722 159724 159728 159734 159736 159742 159746 159748 159752 159754 159758 159760 159762 159763 159764 159766 159767 159768 159770 159772 159776 159778 159782 159784 159788 159794 159796 159802 159806 159808 159812 159818 159824 159826 159832 159836 159838 159844 159848 159854 159862 203614
| A. | BaCl2、Na2CO3、NaOH、盐酸 | B. | NaOH、BaCl2、Na2CO3、盐酸 | ||
| C. | Na2CO3、NaOH、BaCl2、盐酸 | D. | BaCl2、NaOH、Na2CO3、盐酸 |