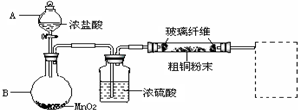
1.进行硫酸铜晶体结晶水含量的测定实验中需要进行多次加热、冷却、称量,其中称量操作至少进行( )
| A. | 5次 | B. | 4次 | C. | 3次 | D. | 2次 |
20. 工业上常用CO2和NH3通过如下反应合成尿素[CO(NH2)2].
工业上常用CO2和NH3通过如下反应合成尿素[CO(NH2)2].
2NH3(g)+C02(g)$\stackrel{一定条件}{?}$C0(NH2)2 (g)+H20(g)△H<0
t℃时,向容积恒定为2L的密闭容器中加入0.10molCO2和0.40molNH3,70min开始达到平衡.反应中CO2(g)的物质的量随时间变化如下表所示:
①70min 时,平均反应速率(CO2 )=5.7×10-4mol/(L•min)mol/(L min).
②在100min时,保持其它条件不变,再向容器中充入0.050mo1CO和0.20molNH3,重新建立平衡后CO2的转化率与原平衡相比将增大 (填“增大”、“不变”或“减小”).
③上述可逆反应的平衡常数为277.8(保留一位小数).
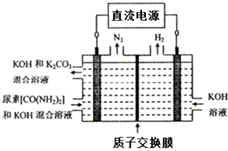
④如图所示装置(阴、阳极均为惰性电极)可用于电解尿素〔CO(NH2)2〕的碱性溶液制取氢气.该装置中阳极的电极反应式为CO(NH2)2+8OH--6e-=CO32-+N2↑+6H2O.
 工业上常用CO2和NH3通过如下反应合成尿素[CO(NH2)2].
工业上常用CO2和NH3通过如下反应合成尿素[CO(NH2)2].2NH3(g)+C02(g)$\stackrel{一定条件}{?}$C0(NH2)2 (g)+H20(g)△H<0
t℃时,向容积恒定为2L的密闭容器中加入0.10molCO2和0.40molNH3,70min开始达到平衡.反应中CO2(g)的物质的量随时间变化如下表所示:
| 时间/min | 0 | 20 | 70 | 80 | 100 |
| 万(CO2)/mol | 0.10 | 0.060 | 0.020 | 0.020 | 0.020 |
②在100min时,保持其它条件不变,再向容器中充入0.050mo1CO和0.20molNH3,重新建立平衡后CO2的转化率与原平衡相比将增大 (填“增大”、“不变”或“减小”).
③上述可逆反应的平衡常数为277.8(保留一位小数).
④如图所示装置(阴、阳极均为惰性电极)可用于电解尿素〔CO(NH2)2〕的碱性溶液制取氢气.该装置中阳极的电极反应式为CO(NH2)2+8OH--6e-=CO32-+N2↑+6H2O.
16.为了除去粗盐中的Ca2+、Mg2+、SO42-和泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤 ②加过量的NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液,正确的操作顺序是( )
0 159637 159645 159651 159655 159661 159663 159667 159673 159675 159681 159687 159691 159693 159697 159703 159705 159711 159715 159717 159721 159723 159727 159729 159731 159732 159733 159735 159736 159737 159739 159741 159745 159747 159751 159753 159757 159763 159765 159771 159775 159777 159781 159787 159793 159795 159801 159805 159807 159813 159817 159823 159831 203614
| A. | ①④②⑤③ | B. | ④①②⑤③ | C. | ②⑤④①③ | D. | ④⑤②①③ |

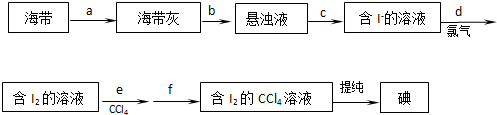
 某小组欲探究Cl2与KI溶液的反应,设计实验装置如下图.
某小组欲探究Cl2与KI溶液的反应,设计实验装置如下图.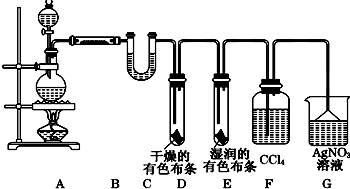

 ①盐泥a除泥沙外,还含有的物质是Mg(OH)2.
①盐泥a除泥沙外,还含有的物质是Mg(OH)2.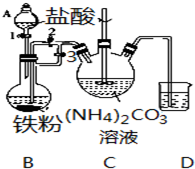 乳酸亚铁{[CH3CH(OH)COO]2Fe}是一种很好的食品铁强化剂,易溶于水,吸收效果比无机铁好,可由乳酸与FeCO3反应制得.
乳酸亚铁{[CH3CH(OH)COO]2Fe}是一种很好的食品铁强化剂,易溶于水,吸收效果比无机铁好,可由乳酸与FeCO3反应制得.