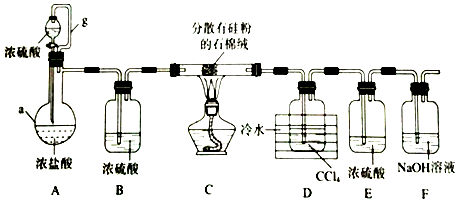
3.电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质,工业上通过下述流程回收Na2Cr2O7等物质.
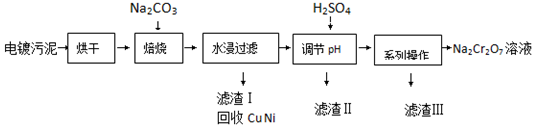
已知:
①Cr(OH)3、ZnO和Al2O3一样均为两性化合物;
②Na2Cr2O7、Na2SO4在不同温度下的溶解度如表:
(1)焙烧过程中生成Na2CrO4的化学方程式为4Cr(OH)3+4Na2CO3+3O2$\frac{\underline{\;高温\;}}{\;}$4Na2CrO4+6H2O+4CO2;水浸后溶液中除Na2CrO4还存在的溶质有NaAlO2和Na2ZnO2;
(2)加入H2SO4调节pH的目的为除去溶液中NaAlO2、Na2ZnO2杂质,并将CrO42-转化为Cr2O72-;
(3)得到滤渣Ⅲ的“系列操作”的步骤为蒸发浓缩、冷却结晶 过滤;
(4)若1L加入H2SO4后所得溶液中含铬元素质量为23.4g,CrO42-有8/9转化为Cr2O72-,求转化后所得溶液中c(Cr2O72-)=0.2mol•L-1;
(5)向Na2Cr2O7与H2SO4混合液中加入H2O2,再加入乙醚并摇动,乙醚层为蓝色.乙醚中溶有CrO5,则发生反应的化学方程式为Na2Cr2O7+4H2O2+H2SO4═2CrO5+Na2SO4+5H2O.

已知:
①Cr(OH)3、ZnO和Al2O3一样均为两性化合物;
②Na2Cr2O7、Na2SO4在不同温度下的溶解度如表:
| 20℃ | 60℃ | 100℃ | |
| Na2SO4 | 19.5 | 45.3 | 42.5 |
| Na2Cr2O7 | 183 | 269 | 415 |
(2)加入H2SO4调节pH的目的为除去溶液中NaAlO2、Na2ZnO2杂质,并将CrO42-转化为Cr2O72-;
(3)得到滤渣Ⅲ的“系列操作”的步骤为蒸发浓缩、冷却结晶 过滤;
(4)若1L加入H2SO4后所得溶液中含铬元素质量为23.4g,CrO42-有8/9转化为Cr2O72-,求转化后所得溶液中c(Cr2O72-)=0.2mol•L-1;
(5)向Na2Cr2O7与H2SO4混合液中加入H2O2,再加入乙醚并摇动,乙醚层为蓝色.乙醚中溶有CrO5,则发生反应的化学方程式为Na2Cr2O7+4H2O2+H2SO4═2CrO5+Na2SO4+5H2O.
1.类比法是化学学习过程中一种重要方法,以下类比关系正确的是( )
| A. | 工业上可以电解熔融的氯化镁或氯化铝制得相应的金属单质 | |
| B. | Cl2、Br2、I2都具有强氧化性,都能将铁氧化成+3价的铁盐 | |
| C. | 二氧化碳和二氧化硫都是氧化物,两者都不能和氯化钙溶液反应 | |
| D. | 氧化铁和氧化亚铁都是碱性氧化物,和硝酸反应都只生成盐和水 |
20.一定温度下,将a mol PCl5通入一个容积不变的密闭容器中,发生反应:PCl5(g)?PCl3(g)+Cl2(g),平衡时测得混合气体的压强为p1,此时向容器中再通入a mol PCl5,在相同温度下再次达到平衡时,测得压强为p2,下列判断正确的是( )
| A. | 2p1>p2 | B. | PCl5的分解率增大 | ||
| C. | p1>p2 | D. | Cl2的体积分数增大 |
19.已知2SO2(g)+O2(g)?2SO3(g)△H=-198.0 kJ•mol-1.若在500℃和催化剂的作用下,反应在容积固定的密闭容器中进行,下列有关说法正确的是( )
| A. | 该反应条件下,初始时向容器中充入2molSO2和1molO2,反应平衡时,可以释放198.0 kJ的热量 | |
| B. | 达到平衡时,SO2和SO3的浓度一定相等 | |
| C. | 反应体系中,当混合物的密度保持不变,反应达到平衡 | |
| D. | 增大压强和升高温度有利于加快反应速率,但升高温度对平衡转化率不利 |
18.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 3.2g S在反应中转移电子数为0.2NA | |
| B. | 0.1mol Fe在反应中转移电子数为0.3NA | |
| C. | 6.5g Zn在反应中转移电子数为0.2NA | |
| D. | 11.2L O2在反应中转移电子数为0.2NA |
17.在密闭容器里,发生反应2A(g)+B(g)?2C(g),下列不能说明该反应达到化学平衡的是( )
| A. | 2v正(B)=v逆(C) | B. | 该体系的密度都不随时间变化 | ||
| C. | 1molA断裂,同时1molC也断裂 | D. | 该体系的温度不随时间而变化 |
16.KMnO4能将草酸(H2C2O4)氧化.在25℃下,某同学欲通过对比实验探究初始pH和草酸浓度对该反应速率的影响.完成实验设计表,表中不要留空格.
(2)某同学欲利用高锰酸钾法测定碳酸钙样品中钙的含量.过程如下:
步骤Ⅰ称取2.50g碳酸钙试样,溶解于稀盐酸,以CaC2O4形式沉淀钙.
沉淀Ⅱ将沉淀过滤洗涤,溶于稀硫酸后定容在250mL容量瓶中.
步骤Ⅲ每次取20.00mL溶液,用0.020mol/L KMnO4标准溶液滴定,三次滴定消耗标准液的平均体积为36.42mL.
①滴定过程中用到的玻璃仪器有酸式滴定管、锥形瓶,滴定终点的现象是加入最后一滴KMnO4溶液,溶液变为浅红色,浅红色30s内不褪去,说明滴定到终点.
②步骤Ⅱ中若将沉淀溶于稀盐酸,会使测定结果偏高(填“偏高”“偏低”或“无影响”).
③试样中钙的质量分数是91.05%.
 | 初始pH | V(KMnO4)/mL | V(H2C2O4)/mL | V(H2O)/mL |
| ① | 4 | 20 | 10 | |
| ② | 5 | 10 | 5 | |
| ③ | 20 | 10 |
步骤Ⅰ称取2.50g碳酸钙试样,溶解于稀盐酸,以CaC2O4形式沉淀钙.
沉淀Ⅱ将沉淀过滤洗涤,溶于稀硫酸后定容在250mL容量瓶中.
步骤Ⅲ每次取20.00mL溶液,用0.020mol/L KMnO4标准溶液滴定,三次滴定消耗标准液的平均体积为36.42mL.
①滴定过程中用到的玻璃仪器有酸式滴定管、锥形瓶,滴定终点的现象是加入最后一滴KMnO4溶液,溶液变为浅红色,浅红色30s内不褪去,说明滴定到终点.
②步骤Ⅱ中若将沉淀溶于稀盐酸,会使测定结果偏高(填“偏高”“偏低”或“无影响”).
③试样中钙的质量分数是91.05%.
15.常温下有如下四种溶液:①pH=11的NaOH溶液,②pH=11的NaCN溶液,③pH=3的盐酸,④0.001mol•L-1的NH4NO3溶液.下列推断正确的是( )
| A. | ②中水的电离程度的是①的8倍 | |
| B. | ①和③中水的电离程度相等 | |
| C. | 等体积的①和④混合后所得溶液中:c(NH3•H2O)<c(NH4+) | |
| D. | ②中水的电离程度等于④ |
14.与氢氧根具有相同的质子数和电子数的微粒是( )
0 159609 159617 159623 159627 159633 159635 159639 159645 159647 159653 159659 159663 159665 159669 159675 159677 159683 159687 159689 159693 159695 159699 159701 159703 159704 159705 159707 159708 159709 159711 159713 159717 159719 159723 159725 159729 159735 159737 159743 159747 159749 159753 159759 159765 159767 159773 159777 159779 159785 159789 159795 159803 203614
| A. | CH4 | B. | NH4+ | C. | Cl- | D. | NH2- |